-
中华民族的发明创造为人类文明进步做出了巨大贡献。下列古代发明及应用中,不涉及化学变化的是
A.
 活字印刷 B.
活字印刷 B.  陶瓷烧制
陶瓷烧制C.
 火药使用 D.
火药使用 D.  粮食酿醋
粮食酿醋难度: 简单查看答案及解析
-
下列有关水的说法不正确的是
A. 区别硬水与软水常用肥皂水 B. 蒸馏可使海水淡化,但用活性炭不行
C. 矿泉水标签上的Na、Ca、K等成分是指各元素 D. 明矾可以使硬水转化为软水
难度: 简单查看答案及解析
-
我国自2015年1月1日起,对地级及以上城市执行空气质量监测新标准,监测数据包括可吸入颗粒(PM10)、细微粒物(PM2.5)、SO2、NO2、O3和CO等6项指标.某同学对SO2、NO2、O3和CO四种物质的认识,不正确的是
A. O3属于单质
B. SO2、NO2和CO都属于氧化物
C. SO2、NO2中都含有氧分子
D. SO2、NO2、O3和CO中都含有氧元素
难度: 简单查看答案及解析
-
新华社合肥2017年12月25日报道,泾县湛岭钼矿中伴生稀有“超级金属”铼,现已探明铼储量达30吨,实属罕见。金属铼硬度大,熔点很高,铼及其合金被广泛应用到航空航天领域。下列说法不正确的是
A. 铼原子的质量是186.2 B. 铼元素的质子数是75
C. 伴生铼的钼矿属混合物 D. Re2O7和ReO4- 中铼的化合价都是+7价
难度: 简单查看答案及解析
-
“桃花潭水深千尺,不及汪伦送我情”,泾县桃花潭酒由此闻名。其独特的酒香主要来自于酿造和陈化过程中产生的乙酸乙酯,其分子结构如下图。下列关于乙酸乙酯说法正确的是

A. 乙酸乙酯含有4个碳原子、8个氢原子、2个氧原子
B. 乙酸乙酯属于氧化物
C. 乙酸乙酯中碳、氢、氧元素的质量比为2:4:1
D. 乙酸乙酯充分燃烧的产物只有CO2和H2O
难度: 简单查看答案及解析
-
下列符号中对“2”所表示的含义,说法不正确的是
A. 2H:表示个氢原子 B. Fe2+:表示一个铁离子带2个单位正电荷
C.
:表示氧化镁中镁元素的化合价为+2价 D. CO2:表示一个二氧化碳分子中含有2个氧原子
难度: 简单查看答案及解析
-
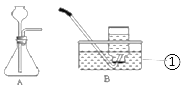
下列实验操作不规范、不符合要求的是

A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列叙述正确的是
A. 由同种元素组成的物质是单质 B. 混合物中可能只含一种元素
C. 某物质不是化合物就是单质 D. 某物质含有氧元素,它一定是氧化物
难度: 中等查看答案及解析
-
等电子体具有原子数目相同、电子数目相同的特征。下列各组中的物质属于等电子体的是
A. NO和O2+ B. CO2和O3 C. NH3和CH4 D. SO2和ClO2
难度: 中等查看答案及解析
-
实验室测定蜡烛在盛有一定体积空气的密闭容器内燃烧至熄灭过程中,O2和CO的含量随时间变化曲线如图,通过分析该图可推理出的结论是
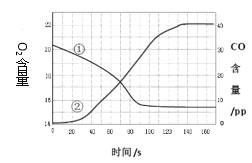
A. 曲线①表示CO含量的变化
B. 蜡烛燃烧过程中产生了CO
C. 蜡烛由碳、氢元素组成
D. 蜡烛熄灭时,容器内氧气耗尽
难度: 简单查看答案及解析