-
化学与生产、生活、社会密切相关,下列有关说法中正确的是
A. 用“地沟油“纯化生产“生物燃油”的过程发生的是化学变化
B. 节日燃放的焰火是某些金属元素发生焰色反应所呈现出来的色彩,焰色反应是物理变化
C. 向牛奶中加入果汁会产生沉淀,这是因为发生了酸碱中和反应
D. 钢铁制品和铜制品既可发生吸氧腐蚀又可发生析氢腐蚀
难度: 简单查看答案及解析
-
以NA代表阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,22.4LHF中含有的氟原子数目为NA
B. 12g石墨烯(单层石墨)中含有的六元环个数为NA
C. 标准状况下,6.0gNO和2.24LO2混合,所得气体的分子数目为0.2NA
D. 反应N2(g)+3H2(g)
2NH3(g) △H=-92.4kJ/mol,若放出热量4.62kJ,则转移的电子数目为0.3NA
难度: 中等查看答案及解析
-
下列关于有机化合物的说法正确的是
A. 乙烯和聚乙烯互为同系物
B. 丙烯和苯分子内所有原子均在同一平面内
C. 分子式为C5H12O且可与金属钠反应放出氢气的有机物(不考虑立体异构)有8种
D. 乙醇中含乙酸杂质,可加人碳酸钠溶液洗涤、分液除去
难度: 中等查看答案及解析
-
下列实验操作能达到实验目的的是
选项
实验操作
实验目的
A
向盛有2mL0.1mo/LAgNO3溶液的试管中滴加一定量0.1mo/LNaCl溶液,再向其中滴加一定量0.1mol/LKI溶液
证明相同温度下的溶度积常数Ksp(AgCl)>Ksp(AgI)
B
取两支试管,分别加入4mL0.01mol/LKMnO4酸性溶液,然后向一支试管中加入0.1mol/LH2C2O4液2mL,向另一支试管中加入0.1mol/L H2C2O4液4mL,记录褪色时间
证明草酸浓度越大,反应速率越大
C
向盛有1mL浓硫酸的试管中加入5mL0.01mol/LK2Cr2O7溶液
证明增大生成物的浓度,使平衡Cr2O72-(橙色)+H2O
2CrO42-+2H+逆向移动
D
向混有BaCO3沉淀的NaOH溶液中满入已知浓度的盐酸(用酚酞作指示剂)
滴定其中的NaOH含量
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
据外媒报道,Wirth Research公司公布了其用轻型氢燃料电池作为主要能源的无人空中系统(UAS)的设计,该轻型氢燃料电池比普通理离子电池具有更高的能量密度(能量密度是指单位体积或重量可以存储的能量多少)。用吸附了H2的碳纳米管等材料制作的二次电池的原理如下图所示。该电池的总反应为H2+2NiO(OH)
2Ni(OH)2,已知:6NiO(OH)+NH3+H2O+OH-=6Ni(OH)2+NO2-。下列说法不正确的是
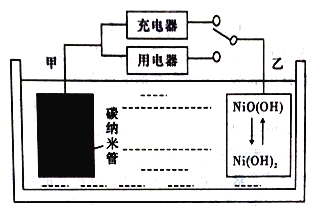
A. 碳纳米管吸附H2的密度越大,电池的能量密度越高
B. 电池可以用KOH溶液、氨水等作为电解质溶液
C. 放电时.乙电极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH-
D. 充电时,电池的碳电极与直流电源的负极相连
难度: 中等查看答案及解析
-
短周期元素X、Y、Z、Q、W、R的原子序数与其常见化合价关系如下图所示。下列说法正确的是
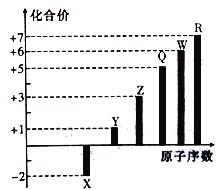
A. X、Y、R形成的某种化合物可以用于漂白、消毒
B. Q元素形成的可溶性盐的溶液不可能显酸性
C. X、Y、Z、W、R的简单离子半径大小顺序为R>W>Z>Y>X
D. Y、Z和W三者最高价氧化物对应的水化物间不能两两相互反应
难度: 中等查看答案及解析
-
下列说法正确的是
A. 等物质的量浓度的NH4HSO4溶液和NaOH溶液等体积混合,溶液中各离子浓度大小关系为c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-)
B. 常温下电离常数为Ka的酸HA的溶液中c(H+)=
mol/L
C. 常温下同浓度的强酸和强碱溶液等体积混合后,由水电离出的c(H+)=10-7mol/L
D. 已知298K时氢氰酸(HCN)的Ka=4.9×10-10,碳酸的Ka1=4.4×10-7、Ka2=4.7×10-11,据此可推测出将氢氰酸加入到碳酸钠溶液中能观察到有气泡产生
难度: 中等查看答案及解析
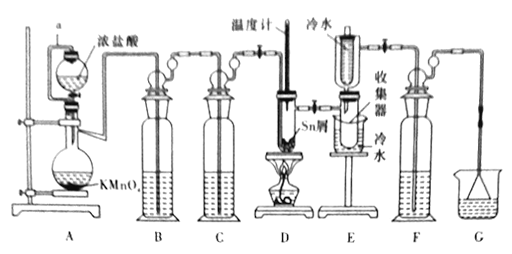
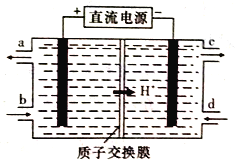

 )__________________________
)__________________________