-
下列有关化学用语正确的是
A.N2的电子式:N⋮⋮N
B.质子数为53,中子数为78的碘原子:153I
C.S2-的结构示意图:
D.硫酸铁的电离方程式:Fe2(SO4)3=Fe3++SO42-
难度: 中等查看答案及解析
-
某元素的天然同位素有510X和511X两种,如果该元素的相对原子质量为10.8,那么元素X的天然同位素中510X和511X的原子个数之比为
A、3∶1 B、1∶3 C、4∶1 D、1∶4
难度: 中等查看答案及解析
-
为了除去铁粉中的少量铝粉,可以选取下列哪种溶液
A.浓盐酸 B.浓硝酸 C.浓硫酸 D.浓氢氧化钠溶液
难度: 中等查看答案及解析
-
下列各组物质反应后,滴入KSCN溶液,显红色的是
A.过量的铁与稀盐酸反应 B.过量的铁粉与氯化铜溶液反应
C.过量氯水与氯化亚铁溶液反应 D.过量铁粉与三氯化铁溶液反应
难度: 中等查看答案及解析
-
下列物质中既能与盐酸反应,又能与NaOH溶液反应的是
①Na2CO3、 ②Al(OH)3、 ③NH4HCO3、 ④Al2O3
A.①②④ B.②③④ C.②④ D.全部
难度: 中等查看答案及解析
-
除去CO2中混有的少量SO2气体,最好选用的试剂是
A.澄清石灰水 B.品红溶液
C.饱和NaHCO3溶液 D.饱和Na2CO3溶液
难度: 中等查看答案及解析
-
高炉炼铁用于还原氧化铁的还原剂是
A.一氧化碳 B.焦炭 C.石灰石 D.空气
难度: 简单查看答案及解析
-
实验室为了妥善保存硫酸亚铁溶液,常加入少量的
A.锌粉 B.铜片 C.铁片 D.镁粉
难度: 中等查看答案及解析
-
下列离子方程式书写正确的是
A.FeCl2溶液中通入Cl2:Fe2++Cl2=Fe3++2Cl-
B.Ba(OH) 2溶液与稀硫酸的反应:OH-+H+ =H2O
C.Al(OH)3沉淀中滴加盐酸:Al(OH) 3+3H+ = Al3++3H2O
D.AlCl3溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O
难度: 中等查看答案及解析
-
为检验Na2SO3溶液中是否含有Na2SO4应选用的试剂是
A.BaCl2溶液 B.稀盐酸、BaCl2溶液
C.稀硝酸、BaCl2溶液 D.稀硫酸、BaCl2
难度: 中等查看答案及解析
-
下列各组离子能大量共存的是
A.H+、Na+、HCO3-、Cl- B.Fe3+、SCN-、Cl-、NO3-
C.Mg2+、Fe2+、SO42-、NO3- D.Fe3+、SO42-、OH-、NO3-、
难度: 中等查看答案及解析
-
向某溶液中加入含Fe2+的溶液后,无明显变化。当再滴入几滴新制氯水后,混合溶液变成红色,则下列结论错误的是
A.该溶液中一定含有SCN- B.氧化性:Fe2+>Cl2
C.Fe2+与SCN-不能形成红色物质 D.Fe2+被氧化为Fe3+
难度: 中等查看答案及解析
-
将氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液,通过一步实验就能加以区别,并只用一种试剂,这种试剂是
A.KSCN B.BaCl2 C.NaOH D.HCl
难度: 中等查看答案及解析
-
取三张湿润的蓝色石蕊试纸放在玻璃片上,然后按顺序分别滴加98.3%的硫酸、新制氯水、浓氨水,三张试纸最后呈现的颜色是
A.红、白、蓝 B.黑、白、蓝 C.白、白、蓝 D.黑、红、蓝
难度: 中等查看答案及解析
-
在某溶液中滴加HNO3酸化的BaCl2溶液,产生白色沉淀,该溶液中
A.一定含有SO42- B.一定含有Ag+
C.一定含有SO32— D.可能会有SO42—或Ag+或SO32-
难度: 中等查看答案及解析
-
有一充有20mL NO和NO2混合气体的试管,倒置于盛有水的水槽中,充分反应后,仍有12mL无色气体,则原混合气体中NO和NO2体积比为
A.2∶3 B.3∶2 C.1∶4 D.4∶1
难度: 中等查看答案及解析
-
下列推断合理的是
A.明矾[KAl(SO4)2·12H2O]在水中能形成Al(OH)3胶体,可用作净水剂
B.向50mL 18mol/L 硫酸中加入足量铜片并加热,被还原硫酸的物质的量是0.45mol
C.浓硫酸溅到皮肤上,立即用碳酸钠稀溶液冲洗
D.将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水色后加热也能恢复原色
难度: 困难查看答案及解析
-
对下列事实的解释正确的是
A.浓硝酸通常保存在棕色的试剂瓶中,说明浓硝酸不稳定
B.不用浓硝酸与铜屑反应来制取硝酸铜,说明浓硝酸具有挥发性
C.足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
D.锌与稀硝酸反应得不到氢气,说明稀硝酸能使锌钝化
难度: 困难查看答案及解析
-
在如图所示的装置中,干燥烧瓶内盛有某种气体,烧杯和滴定管内盛放某种液体。挤压滴管的胶头,下列与实验事实不相符的是
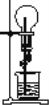
A.NO(H2O含石蕊) /红色喷泉 B.NH3(H2O含酚酞)/红色喷泉
C.SO2(NaOH溶液)/无色喷泉 D.HCl(AgNO3溶液)/白色喷泉
难度: 中等查看答案及解析
-
现有三种制取硝酸铜的实验方案可供选用:下列有关说法正确的是
①铜与稀硝酸反应制取:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
②铜与浓硝酸反应制取:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
③首先将铜屑在空气中加热生成氧化铜,氧化铜与稀硝酸反应制取:
2Cu+O2
2CuO,CuO+2HNO3==Cu(NO3)2+H2O
A.制取等量硝酸铜,需硝酸的量②最少
B.制取等量的硝酸铜,②产生的有毒气体比①少
C.三种方案中,第③方案最经济环保
D.三种方案的反应都可以在铁质容器中进行
难度: 极难查看答案及解析
-
下列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
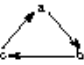
a
b
c
A
Al
AlCl3
Al(OH)3
B
HNO3
NO
NO2
C
Si
SiO2
H2SiO3
D
NH3
NO2
NO
难度: 困难查看答案及解析
-
已知X、Y、Z、W是原子序数依次增大的短周期主族元素,X元素的最高正价与最低负价代数和为2,Y的核电荷数是X的2倍,Z原子的K层和M层电子数之和与L层的电子数相等。下列说法不正确的是
A.原子半径:Y>Z>W B.Y的氧化物属于酸性氧化物
C.对应氢化物的热稳定性:W>Z D.X的最高价氧化物对应水化物是弱酸
难度: 困难查看答案及解析
-
将Al2(SO4)3和(NH4)2SO4的混合溶液a L分为两等份,其中一份加入bmol的BaCl2,恰好使溶液中的SO42-完全沉淀;另一份加入足量强碱并加热可得到cmolNH3,则原溶液中的Al3+的浓度(mol/L)为
A.(2b-c)/2a B.(2b-c)/a C.(2b-c)/3a D.(4b-2c)/3a
难度: 极难查看答案及解析
