-
金属镁可与热水反应生成一种碱和一种气体.某同学将镁条放在热水中煮沸,趁热取出部分溶液,滴加酚酞试液,溶液变为红色,放置在空气中一段时间后,发现溶液的红色褪去了.请根据以上信息回答:
(1)镁条与热水反应的化学方程式为______;
(2)反应后溶液滴加酚酞试液变红色,说明______;
(3)请你对放置一段时间后溶液红色褪去这种现象进行探究.(只要提出假设、方案,不需要说出方案实施的具体结果)
假设一:热的Mg(OH)2溶液与空气的CO2反应,生成盐,溶液褪色.
方案一:向热的Mg(OH)2溶液中滴加酚酞试液,再通入CO2,观察溶液颜色变化.
假设二:______.
方案二:______.难度: 中等查看答案及解析
-
欲在室温和1.01×105Pa条件下测定镁的相对分子质量,请利用下图给定的仪器(盛放镁条的隔板有小孔)组装成一套实验装置(每种仪器只允许用一次).请回答下列问题:
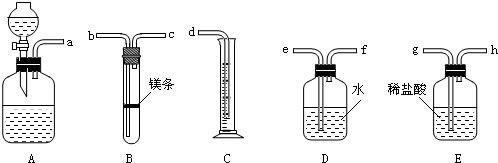
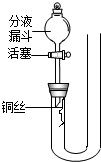
(1)装置A中的分液漏斗中盛放的液体是______,其作用是______;
(2)假设气流方向由左向右,则各仪器的接口连接的先后顺序为(填小字母)______;
(3)连接好仪器后,要进行的操作有以下几步:①待仪器B中的物质恢复到室温时,测得量筒C中水的体积(若假设将测定的体积换算为标准状况下为VmL);②擦掉镁条表面的氧化膜,将其置于天平上称量(假定其质量为mg),并将其投入试管B中;③检查各装置的气密性;④旋开仪器A上分液漏斗的活塞,当镁条完全溶解时再关闭活塞.上述几步操作的先后顺序为______;
(4)若未将试管B冷却至室温就测量量筒C中水的体积,这将会使所得镁的相对原子质量数据(选填“偏高”或“偏低”或“无影响”)______;
(5)若未擦净镁条表面氧化膜就进行实验,这将会使所测镁的相对原子质量数据(选填“偏高”或“偏低”或“无影响”)______.难度: 中等查看答案及解析
-
铁是人体必需的微量元素之一,没有铁,血红蛋白就不能结合氧分子进行输氧,所以缺少铁元素,人体易患的疾病为______,医学上经常用硫酸亚铁糖衣片给这种病人补铁.小陈对这种糖衣片产生了兴趣,打算进行探究.
提出问题:
这种糖衣片中是否含有硫酸亚铁,若有,含量是多少?
查阅资料:
①亚铁离子遇具有氧化性的物质时易被氧化.如氢氧化亚铁为白色沉淀,在空气中会迅速被氧化成红褐色的氢氧化铁沉淀,这是氢氧化亚铁的典型特征.
②亚铁盐溶于水时,会产生少量氢氧根离子而产生沉淀(溶液浑浊).
实验验证:
(1)鉴定硫酸亚铁的成分时需加水溶解,加1滴稀盐酸的作用是什么?______,能否用稀硫酸代替?______(填“能”或“不能”).
(2)为了不影响后续检验亚铁盐,检验硫酸盐可用的试剂是______(选填“A”或“B”).
A、用硝酸酸化的硝酸钡溶液B、用盐酸酸化的氯化钡溶液
检验亚铁盐可用的试剂是______,现象为______.
(3)含量测定:
①取十粒糖衣片,称其质量为5g,溶于20g水中;溶解药品时要用到玻璃棒,其作用是______.
②向所配溶液中滴加氯化钡溶液至略过量;
证明溶液过量的操作为:静置,向上层清液中滴加______溶液,若现象为______,则溶液已过量.
③过滤、洗涤、干燥;
洗涤沉淀的操作为:用玻璃棒______(填一操作名),向过滤器中加入蒸馏水至淹没沉淀,待液体滤出.重复操作2~3次.
如何证明沉淀已洗净?______.
④称量得,沉淀质量为4.66g,试列式计算该糖衣片中硫酸亚铁的质量分数.
总结反思:对硫酸亚铁来说,药片的糖衣可以起到______的作用.难度: 中等查看答案及解析
-
绿矾(FeSO4•7H2O)、硫酸亚铁铵(FeSO4•(NH4)2SO4•6H2O)是重要的化学化工试剂.工业上常利用机械加工行业产生的废铁屑为原料制备.这种废铁屑中常混有FeS(其它杂质忽略不计),与稀硫酸反应为:FeS+H2SO4=FeSO4+H2S↑,H2S有毒,水溶液名称为氢硫酸.
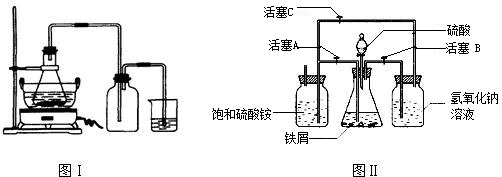
请回答下列问题:
(1)图Ⅰ用于制备绿矾.锥形瓶中反应产生绿矾,其中盛放的药品或原料是______,发生的反应除前述化学方程式外,还一定有 (写化学方程式):______.
若知集气瓶的作用是作安全瓶,烧杯中发生的反应是:CuSO4+H2S=CuS↓+H2SO4,则烧杯中盛放的试剂是______,其作用为______.
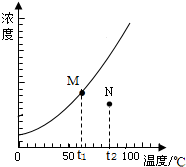
(2)图Ⅱ用于制备硫酸亚铁铵(已知亚铁盐容易被氧化).在0~60℃的温度范围内,硫酸亚铁铵在水中的溶解度比硫酸铵、硫酸亚铁的溶解度小,所以硫酸亚铁与硫酸铵的混合溶液冷却至室温便析出硫酸亚铁铵.
具体操作:①打开活塞______,关闭活塞______,从______(填仪器名称)中滴下稀H2SO4到250mL规格的锥形瓶中,充分反应.②待锥形瓶中的铁屑快反应完时,关闭活塞______,打开活塞______.③放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵.
实验中氢气的作用是______,
氢氧化钠溶液的作用是______.
(3)在制备硫酸亚铁的过程中,理论上控制铁过量或酸过量均有利于防止Fe2+被氧化.设计两个实验:实验一,控制酸过量;实验二,控制铁过量;其余步骤同,制得硫酸亚铁铵,并对产品质量进行检测.检测结果如下:
已知产品质量标准:Fe3+的质量分数等于0.005%,产品质量定为Ⅰ级;Fe3+的质量分数等于0.01%,产品质量定为Ⅱ级,从实验结果中,可得出制备硫酸亚铁溶液时,反应控制______过量为最佳.序号 反应物用量(n表示微粒个数) 产品质量 1 n(H2SO4):n(Fe)>1:1 介于1级~Ⅱ级之间 2 n(H2SO4):n(Fe)<1:1 优于1级
(4)处理胶片的废液中含大量AgNO3、Zn(NO3)2和Fe(NO3)2,若随意排放不仅会造成严重的污染,而且造成资源浪费.某同学从上述的废液中回收金属银并得到副产品绿矾(FeSO4•7H2O),其回收流程如下: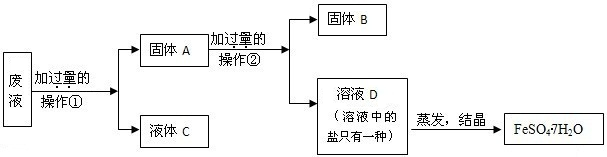
操作②是______,固体A中含______,固体B是______,
x是______,y是______,x、y过量的共同作用是______.
(5)硫酸最古老的生产方法是:把绿矾(FeSO4•7H2O)装入反应器中加强热,会流出油状液体,并放出有刺激性气味的气体(SO2),反应器中的固体变为红色.这个变化的过程可用两个化学方式表示.
①______ Fe2O3+SO2↑+SO3↑+14H2O难度: 中等查看答案及解析