-
下列我国古代的技术应用中,其工作原理不涉及化学变化的是( )
A.粮食酿酒 B.棉线织布 C.冶炼金属 D.烧制陶瓷
难度: 中等查看答案及解析
-
厕所清洁剂的主要成分是盐酸,炉具清洁剂的主要成分是氢氧化钠.关于这两种清洁剂的叙述正确的是( )
A.测得厕所清洁剂的pH=13
B.测得炉具清洁剂的pH=1
C.厕所清洁剂能使紫色石蕊溶液变蓝
D.炉具清洁剂能使无色酚酞溶液变红
难度: 中等查看答案及解析
-
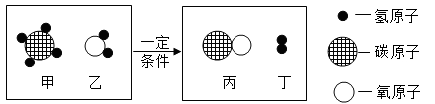
将O2、C、CO、CuO、Na2CO3、稀硫酸六种物质两两混合,在一定条件下能发生的化学反应有( )
A.4个 B.5个 C.6个 D.7个
难度: 困难查看答案及解析
-
储运乙醇的包装箱上应贴的标识是( )

难度: 简单查看答案及解析
-
有机合成材料的出现是对自然资源的一种补充,下列材料中不属于有机合成材料的是( )
A.塑料 B.涤纶 C.合金 D.合成橡胶
难度: 中等查看答案及解析
-
规范的实验操作是实验成功的保证,下列实验操作正确的是( )
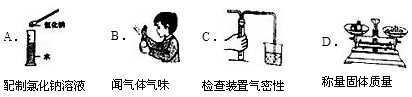
难度: 中等查看答案及解析
-
青蒿素能有效治疗疟疾,其化学式C15H23O5,下列说法正确的是( )
A.青蒿素属于氧化物
B.青蒿素由42个原子构成
C.青蒿素中氢元素的质量分数最大
D.青蒿素中碳、氧元素的质量比为9:4
难度: 中等查看答案及解析
-
根据你的生活经验和所学的化学知识判断,下列说法错误的是( )
A.铁、碘、钙是人体必需的微量元素
B.焚烧秸秆或增加空气中的PM2.5
C.服用含Al(OH)3的药物可治疗胃酸过多
D.洗涤剂具有乳化作用能去除油污
难度: 简单查看答案及解析
-
溴元素在元素周期表中的信息与溴原子结构示意图如图所示,下列说法正确的是( )
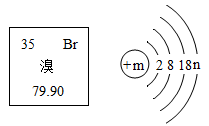
A.1个溴原子的质量是79.90g
B.溴原子的质量由构成其原子的质子和电子决定
C.m=35,n=7
D.溴化镁的化学式为MgBr
难度: 中等查看答案及解析
-
下列实验方法能达到实验目的是( )
选项
实验目的
实验方法
A
鉴别NaCl、NH4NO3、CuSO4、三种白色固体
加水溶解
B
除去KCl固体中的杂质KClO3
加入少量MnO2,加热
C
稀释浓硫酸
将水沿器壁慢慢注入浓硫酸中,并不断搅拌
D
探究稀硫酸与NaOH溶液是否恰好完全反应
向稀硫酸与NaOH溶液反应后所得的溶液中滴加Ba(NO3)2溶液
A.A B.B C.C D.D
难度: 困难查看答案及解析
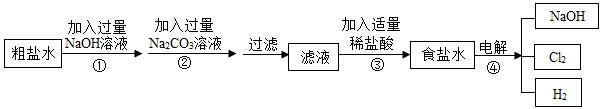

 ,过滤所用的玻璃仪器出烧杯外,还有_____________
,过滤所用的玻璃仪器出烧杯外,还有_____________