-
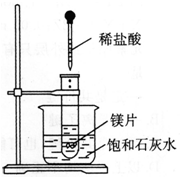
下列反应既属于氧化还原反应,又是吸热反应的是( )
A.铝片与稀盐酸的反应
B.灼热的炭与CO2的反应
C.Ba(OH)2•8H2O与NH4Cl的反应
D.甲烷在氧气中的燃烧反应难度: 中等查看答案及解析
-
下列关于物质性质的比较,不正确的是( )
A.酸性强弱:HIO4>HBrO4>HClO4
B.原子半径大小:Na>S>O
C.碱性强弱:KOH>NaOH>LiOH
D.金属性强弱:Na>Mg>Al难度: 中等查看答案及解析
-
把铝条放入盛有过量稀盐酸的试管中,不影响产生H2速率的因素是( )
A.盐酸的浓度
B.铝条的表面积
C.溶液的温度
D.加少量Na2SO4固体难度: 中等查看答案及解析
-
一定温度下,反应N2(g)+3H2(g)⇌2NH3(g)达到化学平衡状态的标志是( )
A.N2、H2和NH3的浓度不再改变
B.c(N2):c(H2):c(NH3)=1:3:2
C.N2与H2的物质的量之和是NH3的物质的量2倍
D.单位时间里每增加1molN2,同时增加3molH2难度: 中等查看答案及解析
-
下列说法正确的是( )
A.离子化合物只能由金属元素和非金属元素组成
B.离子化合物只能存在离子键
C.盐酸能电离出氢离子和氯离子,所以HCl存在离子键
D.共价化合物中不可能存在离子键难度: 中等查看答案及解析
-
下列各组物质发生状态变化所克服的微粒间的相互作用属于同种类型的是( )
A.食盐和蔗糖溶于水
B.钠和硫熔化
C.碘和干冰升华
D.二氧化硅和氧化钠熔化难度: 中等查看答案及解析
-
下列变化是因原电池反应而引起的是( )
A.在空气中金属铝表面迅速氧化形成保护膜
B.常温下,铁被浓硫酸“钝化”形成保护膜
C.在潮湿的空气中钢铁易生锈
D.在潮湿的空气中过氧化钠易变质难度: 中等查看答案及解析
-
下列关于物质性质的比较,正确的是( )
A.相同温度下,水中的溶解度:NaHCO3>Na2CO3
B.熔点:铯>钾>钠>钠和钾的合金
C.熔沸点:HI>HBr>HCl>HF
D.热稳定性:HF>HCl>HBr>HI难度: 中等查看答案及解析
-
下列化学用语书写正确的是( )
A.氯原子的结构示意图:
B.作为相对原子质量测定标准的碳核素:614C
C.氯化镁的电子式:
D.用电子式表示氯化氢分子的形成过程:难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.P4和NO2都是共价化合物
B.CCl4和NH4Cl都是以共价键结合的分子
C.在CaO和SiO2晶体中,都不存在单个小分子
D.甲烷的结构式:,是对称的平面结构难度: 中等查看答案及解析
-
元素周期表是一座开放的“元素大厦”,元素大厦尚未客满.若发现119号元素,请您在元素大厦中安排好它的“房间”( )
A.第七周期第0族
B.第六周期ⅡA族
C.第八周期第ⅠA族
D.第七周期第ⅦA族难度: 中等查看答案及解析
-
普通干电池负极的电极反应式是( )
A.Zn-2e-=Zn2+
B.Zn2++2e-=Zn
C.4OH--4e-=O2↑+2H2O
D.2H++2e-=H2↑难度: 中等查看答案及解析
-
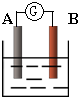
已知空气-锌电池的电极反应为:锌片:Zn+2OH--2e-=ZnO+H2O;碳棒:
O2+H2O+2e-=2OH-,据此判断,锌片是( )
A.正极并被还原
B.正极并被氧化
C.负极并被还原
D.负极并被氧化难度: 中等查看答案及解析
-
将锌片和铜片用导线连接后放入稀硫酸溶液中发生原电池反应,下列叙述正确的是( )
A.负极附近的SO42-浓度逐渐减小
B.正极有O2逸出
C.电子通过导线由铜片流向锌片
D.铜片上有H2逸出难度: 中等查看答案及解析
-
100mL 6mol•L-1 H2SO4 跟足量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
A.碳酸钠固体
B.硝酸钠
C.硫酸钾固体
D.醋酸钠固体难度: 中等查看答案及解析
-
C、CO、CH4、C2H5OH是常用的燃料,它们每1mol 分别完全燃烧生成CO2(g)及H2O(l)时,放出的热量依次为393.5kJ、283.0kJ、890.3kJ、1366.8kJ.相同质量的这4种燃料,完全燃烧时放出热量最多的是( )
A.C
B.CO
C.CH4
D.C2H5OH难度: 中等查看答案及解析