-
重水(D2O)是重要的核工业原料,下列说法错误的是( )
A.氘(D)原子核外有1个电子
B.1H与D互称同位素
C.H2O与D2O互称同素异形体
D.1H218O与D216O的相对分子质量相同
难度: 中等查看答案及解析
-
230Th和232Th是钍的两种同位素,232Th可以转化成233U。下列有关Th的说法正确的是( )
A.Th 元素的质量数是232
B.Th 元素的相对原子质量是231
C.232Th 转换成233U是化学变化
D.230Th和232Th的化学性质相同
难度: 中等查看答案及解析
-
下列除杂的方法错误的是( )
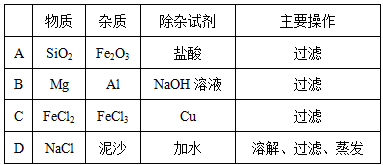
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.SiO2不能与HNO3、H2SO4等所有的酸反应
B.CO2和SiO2的对应水化物都是酸,碳酸酸性比硅酸弱
C.CO2与SiO2均是酸性氧化物,溶于水均得到相应的酸
D.硅胶常用于做干燥剂
难度: 中等查看答案及解析
-
下列物质中既能跟稀H2SO4反应, 又能跟氢氧化钠溶液反应的是( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤NaHSO4 ⑥AlCl3 ⑦Na[Al(OH)4]
A.①⑤ B.②③④⑥⑦ C.①②③④ D.全部
难度: 中等查看答案及解析
-
50g镁、锌、铝的混合物与适量的稀硫酸反应,得三种盐的混合物,然后加热、蒸发、结晶得晶体(不含结晶水)218g,则反应中得H2的质量为( )
A.2g B.3g C. 4.5g D.3.5g
难度: 中等查看答案及解析
-
某溶液中加入铝粉能产生氢气,在该溶液中一定能大量共存的离子组是( )
A.K+、NH4+、Cl﹣、SO42﹣ B.Cu2+、Fe2+、NO3﹣、SO42﹣
C.Na+、Ca2+、Cl﹣、ClO﹣ D.Na+、K+、Cl﹣、SO42﹣
难度: 中等查看答案及解析
-
下列两种物质发生反应 ①Na和O2 ②AlCl3与氨水 ③水玻璃与CO2 ④Fe与Cl2 ⑤Fe和稀HNO3,因反应物用量或反应条件的不同而生成不同产物的是( )
A.①②③④⑤ B. ①②③⑤ C. ①②⑤ D. ①③⑤
难度: 中等查看答案及解析
-
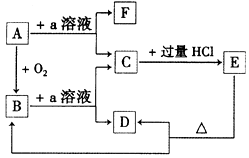
下表各组物质中,满足右图物质一步转化关系的选项是( )
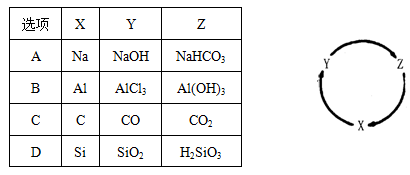
难度: 中等查看答案及解析
-
下列有关Al(OH)3的图像不正确的是( )
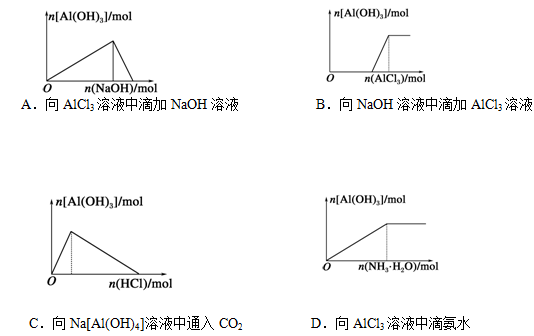
难度: 中等查看答案及解析
-
以下物质间的每步转化通过一步反应就能实现的是( )
A.Al--Al2O3--Al(OH)3-- Na[Al(OH)4]
B.Mg--MgCl2--Mg(OH)2—MgO
C.S--SO3-- H2SO4-- MgSO4
D.Si--SiO2--H2SiO3--Na2SiO3
难度: 中等查看答案及解析
-
16O和18O是氧元素的两种核素,NA表示阿伏加德罗常数,下列说法正确的是( )
A.16O与18O互为同素异形体
B.16O与18O核外电子排布方式不同
C.通过化学变化可以实现16O与18O间的相互转化
D.标准状况下,11.2L16O2和11.2L18O2均含NA个氧原子
难度: 简单查看答案及解析
-
已知A的原子序数是x,B2-与A3+具有相同的电子层结构,则B元素的原子序数为 ( )
A.x+5 B.x-5 C.x+1 D.x-1
难度: 中等查看答案及解析
-
某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子。在a g HmX中所含质子的物质的量是( )
A.
(A-N+m) mol B.
(A-N) mol
C.
(A-N) mol D.
(A-N+m) mol
难度: 中等查看答案及解析
-
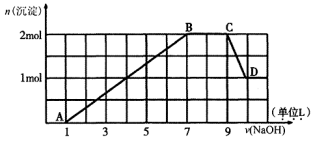
将一定质量的Mg和Al混合物投入到200mL稀硫酸中,固体全部溶解后,向所得溶液中滴加NaOH溶液至过量,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法不正确的是( )
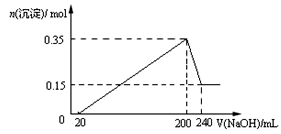
A.Mg和Al的总质量为9g
B.最初20mLNaOH溶液用于中和过量的稀硫酸
C.NaOH溶液物质的量浓度为5mol·L-1
D.生成的氢气在标准状况下的体积为11.2L
难度: 中等查看答案及解析
-
下列反应的离子方程式正确的是( )
A.铝片跟氢氧化钠溶液反应2H2O+2Al+2OH¯=2[Al(OH)4]¯+3H2↑
B.明矾溶液中加入过量的氨水Al3++4NH3·H2O==[Al(OH)4]¯+4NH4+
C.碳酸氢钙溶液中加入过量的氢氧化钠溶液HCO3¯+OH¯==CO32-+H2O
D.铜片跟稀硝酸反应Cu+NO3¯+4H+==Cu2++NO↑+2H2O
难度: 中等查看答案及解析