-
下列反应的离子方程式不正确的是
A. 铁与稀盐酸反应:2Fe + 6H+ =2Fe3 ++ 3H2↑
B. 氢氧化钠溶液与盐酸反应:OH—+ H+ = H2O
C. 锌与硫酸铜溶液反应:Zn + Cu2+ = Zn2+ + Cu
D. 氯化钡溶液与稀硫酸反应:Ba2+ + SO42- = BaSO4↓
难度: 中等查看答案及解析
-
下列叙述中,正确的是
A. 两种粒子,若核外电子排布完全相同,则其化学性质一定相同[
B. 凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布式
C. 两原子,如果核外电子排布相同,则一定属于同种元素
D. 阴离子的核外电子排布与上一周期稀有气体元素原子核外电子排布相同
难度: 中等查看答案及解析
-
下列装置所示的实验中,能达到实验目的是 ( )
A.
分离碘酒中的碘和酒精 B.
 除去Cl2中的HCl
除去Cl2中的HClC.
 排水集气法收集NO D.
排水集气法收集NO D.  实验室制氨气
实验室制氨气难度: 中等查看答案及解析
-
已知反应A+B= C+D的能量变化如下图所示,下列说法正确的是
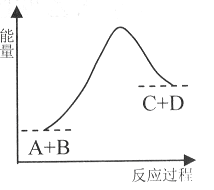
A. 该反应是放热反应
B. 只有在加热条件下才能进行
C. 反应物的总能量高于生成物的总能量
D. 反应中断开化学键吸收的总能量高于形成化学键放出的总能量
难度: 简单查看答案及解析
-
下列化学用语的书写,正确的是
A. 氯原子的结构示意图:
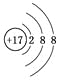
B. 6个质子8个中子的碳元素的核素符号:12C
C. 氯化镁的电子式:
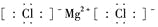
D. 用电子式表示氯化氢的形成过程:
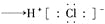
难度: 困难查看答案及解析
-
下列说法正确的是
A. 氯化铵受热固体消失和干冰升华只需克服分子间作用力
B. NaF、H2SO4中所含化学键类型相同
C. HCl气体溶于水和NaOH熔化破坏的化学键类型相同
D. I2、Br2、Cl2、F2的熔沸点逐渐降低
难度: 中等查看答案及解析
-
X、Y、Z、W是原子序数依次增大的四种短周期元素,X的最高价氧化物对应的水化物的化学式为H2XO3,Y的最外层电子数是电子层数的3倍,Z是地壳中含量最高的金属元素,W的一种核素的质量数为28,中子数为14。下列说法正确的是
A. 原子半径由大到小的顺序是Z>W>Y>X
B. 元素的非金属性W>Y>X
C. X、Z、W的最高价氧化物都是酸性氧化物
D. Z2Y3、WX分别是离子化合物、共价化合物
难度: 中等查看答案及解析
-
下图中,R、W、X、Y、Z为元素周期表中前四周期的部分元素,下列有关叙述正确的是
A. 五种元素中,只有Z为金属元素
B. W位于ⅥA族,有+6、-2两种常见化合价
C. X和Y的最高价氧化物对应水化物都是强酸
D. X、Y、Z的气态氢化物的稳定性:Y>X>Z
难度: 简单查看答案及解析
-
25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( )
A. 2H2(g)+O2(g) == 2H2O(1) △H= ―285.8kJ/mol
B. 2H2(g)+ O2(g) == 2H2O(1) △H= +571.6 kJ/mol
C. 2H2(g)+O2(g) == 2H2O(g) △H= ―571.6 kJ/mol
D. H2(g)+1/2O2(g) == H2O(1) △H= ―285.8kJ/mol
难度: 中等查看答案及解析
-
下列叙述中错误的是
A. 13C和14C属于同一种元素,它们互为同位素
B. 6Li和7Li的电子数相等,中子数也相等
C. 14C和14N的质量数相等,它们的中子数不等
D. 1H和2H是不同的核素,它们的化学性质基本相同
难度: 简单查看答案及解析
-
下列性质的递变规律不正确的是
A. HCl、HBr、HI稳定性依次减弱
B. Na、Mg、Al的原子半径依次增大
C. NaOH、KOH、CsOH碱性依次增强
D. Li、Na、K、Rb、Cs单质的失电子能力依次增强
难度: 简单查看答案及解析

 。
。