-
类推是一种重要的学习方法,下列类推结论正确的是( )
A. CO能与Fe2O3反应生成Fe,CO也能与CuO反应生成Cu
B. 有机化合物含碳元素,则含碳元素的化合物一定是有机化合物
C. 燃烧都伴随发光、发热的现象,则伴随发光、发热现象的变化一定是燃烧
D. 稀盐酸能与金属锌反应生成氢气,稀盐酸也能与金属银反应生成氢气
难度: 中等查看答案及解析
-
某些食物的近似pH为:牛奶6.3~6.6,葡萄3.5~4.5,玉米粥6.8~8.0,苹果2.9~3.3,其中酸性最强的是( )
A. 葡萄 B. 牛奶 C. 苹果 D. 玉米粥
难度: 简单查看答案及解析
-
10月16日至25日,第七届全国城市运动会在江西省南昌市举行,在开幕式上的精彩表演中,发生化学变化的是( )
A. 焰火表演 B. 霓虹灯表演 C. 音乐喷泉 D. 气球升空
难度: 简单查看答案及解析
-
小静同学用连线的方式对学过的知识进行主题归纳,其中有错误的是( )
A. 元素与人体健康

B. 环保与物质的利用

C. 性质与用途

D. 生活常识

难度: 中等查看答案及解析
-
下列关于氧气的叙述正确的是( )
A. 空气中氧气的质量分数约为21%
B. 氧气的含量越高,物质的燃烧越剧烈
C. 红磷在氧气中燃烧,有大量白色烟雾生成
D. 不加二氧化锰,加热氯酸钾固体不会产生氧气
难度: 中等查看答案及解析
-
如图所示实验操作规范正确的是( )
A.
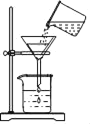 过滤 B.
过滤 B. 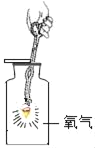 铁丝燃烧
铁丝燃烧C.
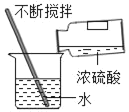 稀释浓硫酸 D.
稀释浓硫酸 D. 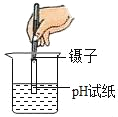 测溶液的pH
测溶液的pH难度: 简单查看答案及解析
-
按照一定的依据把物质进行分类,是我们认识物质的组成、结构、性质和用途的便捷途径。现有下列物质:①纯碱;②生石灰;③盐酸;④熟石灰;⑤甲烷;⑥铁;⑦石墨;对上述物质的分类正确的是 ( )
A. 属于有机物的有③⑤ B. 属于单质的有②⑥⑦
C. 属于碱的有①④ D. 属于氧化物的有②
难度: 简单查看答案及解析
-
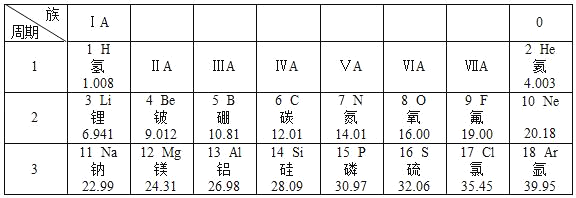
南昌汉代海昏侯墓出土的文物中,保存完好的玉器非常罕见.对玉石主要成分(化学式为NaAlSi2O6)的描述正确的是( )
A. 含有3个氧分子
B. 相对分子质量为94
C. 其中硅元素的化合价为+3价
D. 钠元素与铝元素的质量比为23:27
难度: 中等查看答案及解析
-
如图是三种物质的溶解度曲线。下列说法正确的是( )

A. t1℃时,将a的不饱和溶液升高温度变为饱和溶液
B. t1℃时,三种物质的溶解度c>b>a
C. t2℃时,a、c溶液的溶质质量分数都是20%
D. 将等质量t3℃的三种物质的饱和溶液都降温到t2℃后,溶液的溶质质量分数b>a=c
难度: 简单查看答案及解析
-
下列实验不能达到实验目的是( )
A.
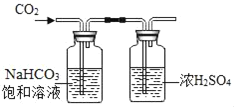 除去实验室制得二氧化碳气体中的氯化氢和水蒸气,得到纯净、干燥的二氧化碳
除去实验室制得二氧化碳气体中的氯化氢和水蒸气,得到纯净、干燥的二氧化碳B.
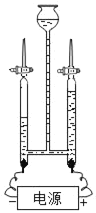 验证水是由氢元素和氧元素组成的
验证水是由氢元素和氧元素组成的C.
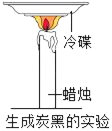 探究蜡烛中含有碳元素
探究蜡烛中含有碳元素D.
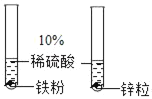 证明锌的金属活动性比铁活泼
证明锌的金属活动性比铁活泼难度: 中等查看答案及解析