-
苹果主要能为人体提供的营养素是( )
A. 油脂 B. 维生素 C. 蛋白质 D. 无机盐
难度: 简单查看答案及解析
-
属于化学变化的是( )
A. 冰块熔化 B. 蜡烛燃烧 C. 黄金铸币 D. 海水晒盐
难度: 简单查看答案及解析
-
下列有关叙述、对应方程式、基本反应类型都正确的是( )
A. 硝铵不能和熟石灰混用:2NH4NO3+Ca(OH)2=Ca(NO3)2+2H2O+2NH3↑复分解反应
B. 赤铁矿炼铁:
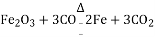 置换反应
置换反应C. 葡萄糖在人体中氧化:
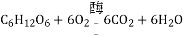 氧化反应
氧化反应D. 比较铁和银的金属活动性:Fe+2AgCl=FeCl2+2Ag置换反应
难度: 中等查看答案及解析
-
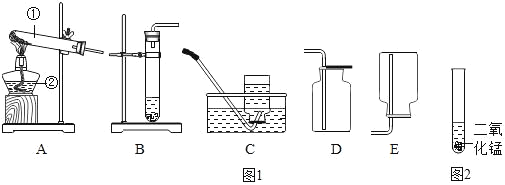
下列实验操作中,正确的是( )
A.
 滴加液体 B.
滴加液体 B.  过滤液体
过滤液体C.
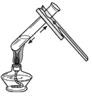 加热液体 D.
加热液体 D.  加热固体
加热固体难度: 简单查看答案及解析
-
只用下列鉴别方法不能把待鉴别物质区分开的是( )
选项
待鉴别物质
鉴别方法
A
软水、硬水
分别滴加肥皂水,搅拌,观察产生泡沫多少
B
棉纤维、羊毛纤维
分别点燃,闻燃烧产生的气味
C
淀粉、葡萄糖
分别滴加碘水,观察颜色的变化
D
氢氧化钠溶液、碳酸钠溶液
分别滴加酚酞溶液,观察溶液颜色变化
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
化学实验过程中要规范操作,注意实验安全.下列做法中正确的是( )
A. 加热后的试管立即用水冲洗
B. 为提高实验操作效率,没有毒性的化学药品可以直接用手抓取
C. 实验药液溅进眼睛立即用纸巾擦拭
D. 洒在实验台上的酒精失火立即用湿布覆盖
难度: 简单查看答案及解析
-
化学与生活密切相关.下列说法不正确的是( )
A.人体缺铁会导致甲状腺肿大
B.食用牛奶可为人体补充蛋白质
C.电器起火时应立即切断电源
D.蒸馏可以将硬水转化为软水
难度: 简单查看答案及解析
-
2008年1月我国南方普降大雪,为尽快恢复交通,使用了大量融雪剂。有一种融雪剂中含有硅酸钠(Na2SiO3),Na2SiO3中Si元素的化合价为( )
A. +2 B. +3 C. +4 D. +6
难度: 简单查看答案及解析
-
黑火药是我国古代四大发明之一。黑火药爆炸的原理可以用下式表示:2KNO3+3C+S
K2S+N2↑+3X↑,根据质量守恒定律推断X的化学式为( )
A. CO2 B. CO C. NO D. SO2
难度: 中等查看答案及解析
-
在一个密闭容器里放入四种物质,使其充分反应,测得数据如下:
四种物质
甲
乙
丙
丁
应前质量/g
25
15
1
5
应后质量/g
11
未测
1
22
则下列表述正确的是( )
A. 未测值3g
B. 丙一定是催化剂
C. 乙全部发生了反应
D. 甲与乙反应的质量比为14:3
难度: 简单查看答案及解析
-
有X,Y两元素,使12g X2与XY3反应生成24gC,化学方程式为:X2+XY3=3C,则X,Y两元素的相对原子质量之比( )
A. 1:1 B. 1:2 C. 3:1 D. 3:4
难度: 中等查看答案及解析
-
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是
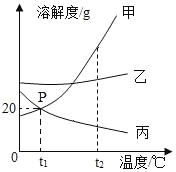
A. 丙物质的溶解度随温度的升高而增大
B. P点表示t1 ℃时,甲、丙两种物质的溶解度均为20 g
C. t2 ℃时,乙的溶解度最大
D. 将t2 ℃的甲的饱和溶液降温至t1 ℃,溶液变为不饱和溶液
难度: 简单查看答案及解析