-
500mL含有MgCl2 、NaC1、Na2SO4三种物质的混合溶液,已知其中含有C1-为1.8mol,Na+ 为2mol,Mg2+ 为0.5mol,则SO42- 的物质的量浓度为
A. 0.6mo1/L B. 0.7mo1/L C. 1.0mo1/L D. 1.2mo1/L
难度: 简单查看答案及解析
-
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A. 分液、萃取、蒸馏 B. 萃取、蒸馏、分液
C. 分液、蒸馏、萃取 D. 蒸馏、萃取、分液
难度: 简单查看答案及解析
-
下列实验操作要求中,主要是从实验安全方面考虑的是( )
A. 实验剩余的药品不能放回原试剂瓶 B. 点燃可燃性气体前必须验纯
C. 气体实验装置在实验前要进行气密性检查 D. 滴管不能交叉使用
难度: 中等查看答案及解析
-
以下是一些常用的危险品标志,装运乙醇(酒精)的包装箱应贴的图标是( )
A.
 B.
B.  C.
C.  D.
D. 
难度: 简单查看答案及解析
-
下列现象或新技术的应用中,不涉及胶体性质的是( )
A. 肾功能衰竭等疾病,可利用血液透析进行治疗
B. 在饱和氯化铁溶液中滴加NaOH溶液,产生红褐色沉淀
C. 清晨,在茂密的树林中,可看到枝叶间透过的一道光线
D. 使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血
难度: 中等查看答案及解析
-
下图所示是分离混合物时常用的主要仪器,从左至右,可以进行的混合物分离操作分
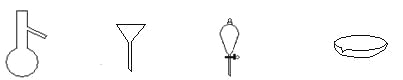
A. 蒸馏、蒸发、萃取、过滤 B. 蒸馏、过滤、萃取、蒸发
C. 萃取、过滤、蒸馏、蒸发 D. 过滤、蒸发、萃取、蒸馏
难度: 简单查看答案及解析
-
下列关于电解质说法正确是( )
A. 能导电的物质叫电解质 B. NaCl晶体不导电,所以NaCl不是电解质
C. 熔融的KOH导电,所以KOH是电解质 D. 电解质在通电时发生电离
难度: 中等查看答案及解析
-
下列电离方程式错误的是( )
①NaHCO3= Na++H++ CO32- ② NaHSO4 = Na++H++ SO42-
③H2SO4 = 2H++ SO42- ④KC1O3 = K++ C1++3O2-
A. ①② B. ① C. ①④ D. ③④
难度: 简单查看答案及解析
-
将金属钠分别投入下列物质的稀溶液中,有气体放出,且有沉淀生成的是( )
A. 稀盐酸 B. K2SO4 C. CuCl2 D. NaOH
难度: 中等查看答案及解析
-
使溶液中的Al3+完全转化成Al(OH)3,应选择的最好试剂是( )
A. NH3·H2O B. HCl C. NaOH D. CO2
难度: 中等查看答案及解析
-
下列叙述中,正确的是
A. 阳离子中一定含有金属元素
B. 在氧化还原反应中,非金属单质一定是氧化剂
C. 某元素从化合态变为游离态时,该元素一定被还原
D. 金属阳离子被还原不一定得到金属单质
难度: 简单查看答案及解析
-
NA表示阿伏加德罗常数,下列叙述中正确的是( )
A. 常温常压下,48g O3所含的原子数为3NA
B. 1mol NH3所含有的原子数为NA
C. 标准状况下,22.4L水中所含原子数为3 NA
D. 0.1mol/L NaC1溶液中所含Na+数目为0.1 NA
难度: 中等查看答案及解析
-
下列各组离子中,能在无色透明溶液中大量共存的是
A. Na+、H+、Cl-、OH- B. K+、Na+、CO32-、OH-
C. K+、SO42-、NO3-、MnO4- D. Na+、HCO3-、H+、Ca2+
难度: 中等查看答案及解析
-
鉴别NaOH、Na2CO3、Ba(OH)2三种溶液,最好选用下列试剂中的( )
A. 石蕊溶液 B. 稀硫酸 C. 澄清石灰水 D. CaCl2溶液
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是
A. 铜片插入硝酸银溶液Cu+Ag+=Ag+Cu2+
B. 向稀硫酸溶液中投入铁粉2Fe+6H+=2Fe3++3H2↑
C. 向碳酸钠溶液中加入足量盐酸CO32-+2H+=H2O+CO2↑
D. 氧化铜溶于盐酸O2-+2H+=H2O
难度: 中等查看答案及解析
-
0.1 mol某元素的单质直接与足量氯气反应,质量增加7.1 g,这种元素可能是( )
A. 钠 B. 铝 C. 铁 D. 铜
难度: 简单查看答案及解析
-
下列说不正确的是
A. 金属钠有强还原性,能和硫酸铜溶液反应,析出金属铜
B. 用Al(OH)3治疗胃酸过多
C. 过氧化钠可用于呼吸面具中作为氧气的来源
D. 绚丽缤纷的烟花中添加了含钾、钙、钠、铜等金属元素化合物
难度: 中等查看答案及解析
-
下列物质中,既能和酸反应又能和碱反应的化合物是
①Al ②Al2O3 ③Al(OH)3 ④NaHCO3
A. ②③④ B. ①②④ C. ①②③④ D. ①③④
难度: 中等查看答案及解析
-
在Cu2S+2Cu2O=6Cu+SO2↑反应中,说法正确的是( )
A. 生成1 mol Cu,反应中转移2mol电子 B. Cu元素被氧化
C. 氧化剂只有Cu2O D. Cu2S在反应中既是氧化剂,又是还原剂
难度: 中等查看答案及解析
-
将定量的Na2CO3和NaHCO3的混合物加热到不再放出气体时,收集到CO2aL,冷却后向残余物中加入足量盐酸又收集到CO2 2 aL (体积均在标准状况下测定)。则混合物中Na2CO3和NaHCO3的物质的量之比为( )
A. 1:1 B. 1:2 C. 1:3 D. 1:4
难度: 简单查看答案及解析