-
某溶液中存在Mg2+、Ag+、Ba2+三种金属离子,现用NaOH、Na2CO3、NaCl三种溶液使它们分别沉淀并分离出来,要求每次只加一种溶液,滤出一种沉淀,所加溶液顺序正确的是
A. Na2CO3 NaCl NaOH B. NaOH NaCl Na2CO3
C. NaCl NaOH Na2CO3 D. NaCl Na2CO3 NaOH
难度: 困难查看答案及解析
-
在标准状况下,下列四种气体的关系中,从大到小的顺序正确的是
①6.72LCH4 ②3.01×1023个HCl分子 ③13.6gH2S ④0.2molNH3
A. 体积:③>①>②>④ B. 氢原子数:①>②>③>④
C. 质量:②>①>③>④ D. 密度:②>③>④>①
难度: 简单查看答案及解析
-
为了除去粗盐中的CaCl2、MgCl2、Na2SO4及泥沙,可将粗盐溶于水,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤过滤,不正确的操作顺序是
A. ③②①⑤④ B. ②①③⑤④ C. ③①②⑤④ D. ②③①⑤④
难度: 简单查看答案及解析
-
在盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的
A.
 B.
B.  C.
C.  D.
D. 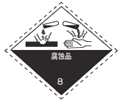
难度: 简单查看答案及解析
-
下列分散系不能发生丁达尔现象的是
A. 豆浆 B. 硫酸铜溶液 C. 淀粉溶液 D. 雾
难度: 简单查看答案及解析
-
下列实验中均需要的仪器是
①配制一定物质的量浓度的溶液 ②浓硫酸的稀释 ③过滤 ④蒸发 ⑤灼烧
A. 玻璃棒 B. 胶头滴管 C. 试管 D. 漏斗
难度: 简单查看答案及解析
-
关于溶液配制,下列说法正确的是
A. 配制480mL0.1mol/LCuSO4溶液,需要称量CuSO4·5H2O晶体12.0g
B. 用浓硫酸配制稀硫酸时,将浓硫酸稀释后立即转入容量瓶中
C. 称量5.3g碳酸钠固体时,若将称量物和砝码放反,将会使称量结果偏小
D. 定容时俯视刻度线,可使配制物质的量浓度偏低
难度: 中等查看答案及解析
-
设NA表示阿伏加德罗常数,下列①至⑥选项叙述中说法正确的是
①标准状况下,22.4L H2O含有的分子数为NA
② NA个CO2的质量与CO2的摩尔质量相同
③ 25℃,101kPa下,64gSO2中含有的原子数为3NA
④ 0.1mol/LCu(NO3)2溶液中含有的NO3-数目为0.2NA
⑤ 常温常压下,11.2L NH3所含的电子数为5NA
⑥相同物质的量的O2分子和O3分子所含的分子数目均为NA
A. 4个正确 B. 3个正确 C. 2个正确 D. 1个正确
难度: 中等查看答案及解析
-
下列物质的分类正确的是
酸
碱
盐
氧化物
A
H2SO4
Na2CO3
NaCl
SO2
B
CO2
NaOH
NaCl
Na2CO3
C
HCl
NaOH
CaO
CH3COOH
D
HNO3
KOH
CaCO3
CaO
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
与100mL 0.1mol/LNa2CO3溶液中Na+离子浓度相同的是
A. 50mL 0.2mol/LNaCl溶液 B. 10mL1mol/LNa2SO4溶液
C. 200mL0.1mol/LNaNO3溶液 D. 10mL0.2mol/LNa2SO4溶液
难度: 简单查看答案及解析
-
下列说法正确的是
①江河入海口三角洲的形成通常与胶体的性质有关
②分离煤油和水可采用分液的方法
③溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀可以证明含硫酸根
④雾是气溶胶,在阳光下可观察到丁达尔现象
⑤某无色溶液加入稀盐酸,产生气体可使澄清石灰水变浑浊,则原溶液中一定含CO32-
⑥可用渗析法分离Fe(OH)3胶体和KCl溶液
A. ①③④⑤ B. ①②④⑥ C. ①③④⑤⑥ D. ①②③④⑤⑥
难度: 简单查看答案及解析
-
下列除杂所选用的试剂及操作方法均正确的一组是(括号内为杂质)
选项
待提纯的物质
选用的试剂
操作方法
A
NaCl(Na2CO3)
硝酸
蒸发
B
酒精(水)
生石灰
萃取分液
C
Zn (Cu)
稀硫酸
过滤
D
CO2(HCl)
饱和碳酸氢钠溶液
洗气
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
某溶液中只含有K+、Al3+、NO3-、SO42- 四种离子,已知前三种离子的个数比为2∶1∶1,则溶液中Al3+和 SO42-的离子个数比为
A. 1∶2 B. 1∶4 C. 3∶4 D. 3∶2
难度: 简单查看答案及解析
-
在体积相同的两个密闭容器中分别充满NO2、N2O4气体,当这两个容器内温度和气体密度相等时,下列说法正确的是
A. 两种气体N原子为1:2 B. 两种气体的质量相等
C. 两种气体的分子数目相等 D. 两种气体的压强相等
难度: 中等查看答案及解析
-
标准状况下,VLHCl气体溶解在1L水中,所得溶液的密度为ρg/mL,溶质的质量分数为ω,溶质的物质的量浓度为cmol/L,则下列关系中不正确的是
A.
B.
C.
D.
难度: 困难查看答案及解析
-
下列实验操作或装置错误的是
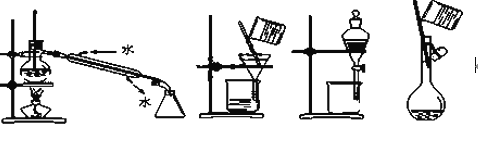
A. 蒸馏 B. 过滤 C. 萃取 D. 转移溶液
难度: 简单查看答案及解析
-
进行化学实验必须注意安全和操作规范,下列说法不正确的是
A. 进行分液操作时,下层液体从分液漏斗的下口放出,上层液体从上口倒出
B. 实验室进行蒸馏实验结束时,应先撤酒精灯,继续通冷凝水一段时间
C. 实验室中进行可燃性气体燃烧性质实验时,必须先验纯、再点燃
D. 配制稀硫酸时,可先在量筒中加一定体积的水,再在搅拌下慢慢加入浓硫酸
难度: 简单查看答案及解析
