-
分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可以采取多种分类方法。下列关于“NaHCO3”的分类正确的是
A. 酸 B. 有机物 C. 盐 D. 氧化物
难度: 简单查看答案及解析
-
下列变化属于物理变化的是
A. 工业制漂白粉 B. 焰色反应 C. 铜的锈蚀 D. 煤的燃烧
难度: 简单查看答案及解析
-
为纪念俄国化学家门捷列夫,人们把第101号元素(人工合成元素)命名为钔。该元素最稳定的一种原子为258101Md ,关于该原子下列说法正确的是
A. 质子数是258 B. 质量数是101
C. 中子数是157 D. 电子数是359
难度: 简单查看答案及解析
-
下列化学反应中,属于氧化还原反应的是
A. Na2CO3 + CaCl2=CaCO3 ↓ + 2NaCl B. Cl2 + 2KI=2KCl + I2
C. 2NaHCO3
Na2CO3 + CO2 ↑ + H2O D. CaO + H2O=Ca(OH)2
难度: 简单查看答案及解析
-
下列化学用语表示正确的是
A. 硫酸亚铁的电离方程式:Fe2(SO4)3 =2Fe3++3SO42-
B. H2SO4的电离方程式:H2SO4=H2+ + SO42-
C. 质子数为6,中子数为7的微粒:76C
D. 钠离子的结构示意图:
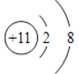
难度: 简单查看答案及解析
-
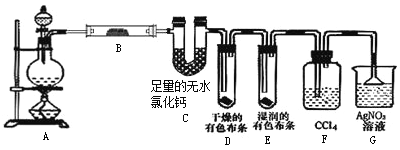
下列实验装置(部分仪器已省略)或操作,能达到相应实验目的的是
A. 闻气体气味
 B. 干燥氯气
B. 干燥氯气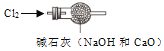
C. 分离乙醇和水
 D. 配制100 mL 0.10 mol•L﹣1盐酸
D. 配制100 mL 0.10 mol•L﹣1盐酸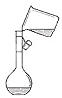
难度: 简单查看答案及解析
-
下列关于胶体的叙述不正确的是
A. 胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9 ~ 10-7m之间
B. 胶体属于混合物
C. Fe(OH)3胶体能吸附水中的悬浮颗粒并沉降,达到净水的目的
D. 用平行光线照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同
难度: 简单查看答案及解析
-
A. 用纸擦干净
B. 放在火焰上灼烧,直到铂丝发红为止
C. 用水洗涤几次
D. 用稀盐酸洗涤,再灼烧到跟酒精灯火焰颜色相同为止
难度: 简单查看答案及解析
-
下列物质,既能导电又属于电解质的是
A. 熔融的氢氧化钾 B. 氯化钠溶液 C. 铜固体 D. 氯化镁晶体
难度: 简单查看答案及解析
-
下列有关物质用途的说法不正确的是
A. 氯气可用于自来水的消毒 B. 去除铁锈可用适量的稀盐酸
C. 石墨可用作绝缘体材料 D. AgI可用于人工降雨
难度: 简单查看答案及解析
-
下列除杂所选用的试剂及操作方法均正确的一组是(括号内为杂质)
选项
待提纯的物质
选用的试剂
操作方法
A.
NaBr溶液(NaI)
Cl2
洗气
B.
Cl2(HCl)
饱和食盐水
洗气
C.
HNO3溶液(H2SO4)
BaCl 2溶液
过滤
D.
NaCl(I2)
水
萃取分液
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列说法正确的是
A. 常温常压下,11.2 L Cl 2 所含有的原子数目为NA
B. 常温常压下,18 g H2O 中含有的电子数目为2 NA
C. 足量的铁在0.1 mol Cl2 燃烧时转移的电子数目为0.3 NA
D. 2.0 L 0.5 mol·L-1 MgSO4溶液中含有的SO42-数目为NA
难度: 简单查看答案及解析
-
下列有关离子的检验及结论正确的是
A. 向某溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水中,出现浑浊,则该溶液中可能有CO32-
B. 向某溶液中加入NaOH溶液后,再滴入酚酞试液显红色,则该溶液中一定有NH4+
C. 某溶液焰色反应呈黄色,则该溶液中一定有K+
D. 向无色溶液中加入氯化钡溶液有白色沉淀生成,再加入盐酸,沉淀不消失,则溶液中一定有SO42-
难度: 简单查看答案及解析