-
24 mL浓度为0.05 mol·L-1的Na2SO3溶液恰好与20 mL浓度为0.02 mol·L-1的K2Cr2O7溶液完全反应。已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
A. +2 B. +3 C. +4 D. +5
难度: 简单查看答案及解析
-
在相同的温度和压强下,下列气体密度最小的是
A. CO2 B. Cl2 C. O2 D. H2
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数,下列说法正确的是
①标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA
②同温同压下,体积相同的氢气和氩气所含的分子数相等
③1L 2mol/L的氯化镁溶液中含氯离子数为4NA
④标准状况下,22.4LH2O中分子数为NA
⑤32g O2和O3混合气体中含有原子数为2NA
A. ①②③④ B. ③④ C. ①②③⑤ D. ①③④
难度: 困难查看答案及解析
-
在无色透明的强酸性溶液中,能大量共存的是
A. Na+、CO32-、Ca2+、NO3- B. Na+、NO3-、Al3+、Cl-
C. K+、SO42-、Cl-、Cu2+ D. Ba2+、Cl-、K+、SO42-
难度: 中等查看答案及解析
-
下列诗句或谚语都与化学现象有关,下列说法不正确的是
A. “忽闻海上有仙山,山在虚无缥缈间”的海市蜃楼是一种自然现象,与胶体知识有关
B. “春蚕到死丝方尽,蜡炬成灰泪始干” 诗句中涉及氧化还原反应
C. “滴水石穿”包含化学变化,而“绳锯木断”则不包含化学变化
D. “卤水点豆腐,一物降一物”发生了化学反应
难度: 中等查看答案及解析
-
有两种金属混合物3.4g,与足量的盐酸反应放出H22.24L(标况下),这两种金属可能是
A. 铜和铁 B. 镁和铝 C. 锌和铝 D. 锌和铁
难度: 中等查看答案及解析
-
下列反应的离子方程式中不正确的是
A. H2SO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-===BaSO4↓+2H2O
B. 氧化铝溶于稀盐酸溶液中:Al2O3+6H+═ 2Al3+ +3H2O
C. NaOH溶液中通入少量CO2:2OH-+CO2 ===CO32-+H2O
D. CH3COOH溶液与NH3·H2O溶液反应:CH3COOH+OH-===CH3COO- + H2O
难度: 中等查看答案及解析
-
下列变化必须加入氧化剂才能实现的是
A. CO2→CO B. KMnO4→O2 C. Fe → Fe3O4 D. CuO →CuSO4
难度: 中等查看答案及解析
-
下列物质中既能与稀H2SO4反应, 又能与NaOH溶液反应的是
①NaHCO3 ②Al2O3 ③Al(OH)3④Al ⑤Na2CO3
A. ③④ B. ①②③④ C. ①③④ D. 全部
难度: 简单查看答案及解析
-
下述对焰色反应实验操作注意事项的说明,正确的是
①钾的火焰颜色要透过蓝色钴玻璃观察
②先将铂丝灼烧到与原来火焰的颜色相同,再蘸取被检验的物质
③每次实验后,要将铂丝用盐酸洗净
④实验时最好选择本身颜色较浅的火焰
⑤没有铂丝时,也可以用光洁无锈的铁丝代替
A. 仅有③不正确 B. 仅有④不正确 C. 仅有⑤不正确 D. 全正确
难度: 简单查看答案及解析
-
反应2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O,下列叙述不正确的是
A. 氧化剂为KMnO4,其中Cl元素被还原
B. 若有0.5molCl2生成,则反应中有NA个电子转移
C. 浓HCl在反应中起酸性和还原性的作用
D. 若消耗0.4mol氧化剂,则被氧化的还原剂的物质的量为2mol
难度: 简单查看答案及解析
-
下列变化不可能通过一步实验直接完成的是
A. Al(OH)3→Al2O3 B. Al2O3→Al(OH)3 C. Al→Al2O3 D. AlCl3→Al(OH)3
难度: 中等查看答案及解析
-
常温下,在溶液中可发生以下反应:
①H++Z-+XO42-→X2++Z2+H2O(未配平) ②2M2++R2=2M3++2R- ③2R-+Z2 =R2+2Z-
由此判断下列说法正确的是
A. 氧化性强弱顺序为XO42->Z2>R2>M3+
B. Z2在③中发生氧化反应
C. R元素在反应②中被氧化,在③中被还原
D. 常温下反应不可进行2M2++Z2 =2M3++2Z-
难度: 中等查看答案及解析
-
有某植物的营养液,其配方如下:对于两种营养液的成分,下列说法中,正确的是
KCl
K2SO4
ZnSO4
ZnCl2
1
0.3mol/L
0.2mol/L
0.1mol/L
—
2
0.1mol/L
0.3mol/L
—
0.1mol/L
A. 只有K+的物质的量浓度相等 B. 只有Cl-的物质的量浓度相等
C. 各离子的物质的量浓度均不同 D. 各离子的物质的量浓度完全相同
难度: 中等查看答案及解析
-
下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是
选项
陈述Ⅰ
陈述Ⅱ
判断
A
碳酸钠可用于治疗胃溃疡
碳酸钠可与盐酸反应
Ⅰ对,Ⅱ对,有
B
向Na2O2的水溶液中滴入酚酞变红色
Na2O2与水反应生成氢氧化钠
Ⅰ对,Ⅱ错,无
C
金属钠具有强还原性
高压钠灯发出透雾性强的黄光
Ⅰ对,Ⅱ对,有
D
Al(OH)3胶体有吸附性
明矾可用作净水剂
Ⅰ对,Ⅱ对,有
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
将0..4gNaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是
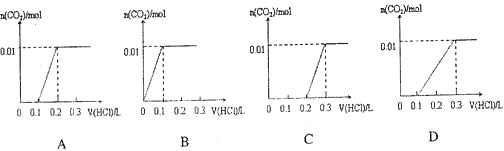
难度: 中等查看答案及解析