-
收藏家收藏的清末铝制品至今保存十分完好,该艺术品不易锈蚀的原因( )
A. 铝的氧化物容易发生还原反应
B. 铝不易氧化
C. 铝易氧化,但铝表面的氧化铝具有保护内部铝的作用
D. 铝不易发生化学反应
难度: 简单查看答案及解析
-
节能减排,保护环境,伊娃美丽广安,是我们共同的责任.下列做法中,与此倡导不相符的是( )
A.提倡使用一次性发泡塑料餐具和塑料袋
B.合理使用化肥、农药
C.发展快速公交、减少私家车出行
D.提倡使用无磷洗衣粉
难度: 简单查看答案及解析
-
下列区别物质的方法不正确的是( )
A. 用肥皂水区别软水和硬水
B. 用酚酞溶液区分盐酸和氢氧化钠溶液
C. 用燃烧的方法区别羊毛和涤纶
D. 用观察颜色的方法区别O2和CO2
难度: 简单查看答案及解析
-
下列纺织材料中属于合成纤维的是
A.棉花 B.腈纶 C.羊毛 D.蚕丝
难度: 中等查看答案及解析
-
下列物质中,不能提供动物生命活动所需能量的是( )
A. 葡萄糖
B. 油脂
C. 蛋白质
D. 水
难度: 简单查看答案及解析
-
酸与碱作用生成盐和水的反应,叫做中和反应。下列应用与中和反应原理无关的是[提示:Ca(OH)2+CuSO4===Cu(OH)2↓+CaSO4↓]( )
A. 用熟石灰和硫酸铜配制波尔多液
B. 服用含Mg(OH)2的药物治疗胃酸过多
C. 施用熟石灰改良酸性土壤
D. 用NaOH溶液中和石油产品中残余的硫酸
难度: 中等查看答案及解析
-
金属R与CuCl2溶液反应的化学方程式为R+CuCl2===RCl2+Cu,则下列说法错误的是( )
A. 该反应是置换反应
B. 金属R可能是铝
C. 金属R活动性比Cu强
D. 该反应前后R的化合价发生了改变
难度: 困难查看答案及解析
-
生活中最常见的含钠元素的化合物是
A.NaOH B.NaCl C.Na2CO3 D.NaHCO3
难度: 中等查看答案及解析
-
下列各组物质全部是混合物的是( )
A. 空气、石油、冰水
B. 液化石油气、水煤气、甲烷
C. 赤铁矿石、石灰石、氧化铁
D. 酒精溶液、汽水、葡萄糖溶液
难度: 中等查看答案及解析
-
下列有关金属的说法错误的是( )
A. 金属具有金属光泽,常温下金属都是固体
B. 生铁和钢是含碳量不同的铁合金,其中生铁的含碳量大于钢的含碳量
C. 炒完菜后,应及时除掉锅底的水,这样可以防止铁锅生锈
D. 金属的回收利用是保护金属资源的有效途径之一
难度: 中等查看答案及解析
-
印刷铜制电路板的“腐蚀液”是FeCl3溶液。已知铜铁均能与FeCl3溶液反应,反应的化学方程式分别为Cu+2FeCl3===2FeCl2+CuCl2,Fe+2FeCl3===3FeCl2。现将一包铜铁的混合粉末加入到盛有FeCl3溶液的烧杯中,充分反应后,烧杯中仍有少量固体,关于烧杯中物质组成的说法中正确的是( )
A. 溶液中一定含有FeCl3,固体一定是铁和铜
B. 溶液中一定含FeCl2,固体一定含铜
C. 溶液中一定含FeCl2、CuCl2,固体一定含铜
D. 溶液中一定含有FeCl2,固体一定是铁和铜
难度: 中等查看答案及解析
-
甲、乙两种固体物质的溶解度曲线如图所示,下列结论正确的是( )

A. 乙的溶解度小于甲的溶解度
B. 甲的溶解度受温度影响比乙大
C. t2℃时,100 g乙的饱和溶液中含乙50 g
D. 相同质量的甲、乙的饱和溶液由t2℃降至t1℃,析出晶体较多的是乙
难度: 中等查看答案及解析
-
锡、铅的熔点分别是232℃和327℃。焊锡是锡铅合金,焊锡的熔点小于200℃,把铅加入锡中制成合金的主要目的是( )
A. 增加强度
B. 降低熔点
C. 增加延展性
D. 增加耐磨性
难度: 中等查看答案及解析
-
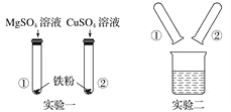
某同学探究X、Y、Z三种金属的活动性顺序,做了以下实验:
(1)取样,分别加入到CuSO4溶液中,发现X、Z表面出现红色物质而Y却没有;
(2)取X、Z大小相等的颗粒,分别加入到溶质质量分数相等的稀H2SO4中,发现X表面产生气泡的速度明显比Z快。
则X、Y、Z的金属活动性由强到弱依次是( )
A. X>Z>Y
B. Z>Y>X
C. X>Y>Z
D. Z>X>Y
难度: 简单查看答案及解析
-
生活处处有化学,下列做法正确的是( )
A.碘是人体需要的微量元素,需大量补充
B.霉变大米、花生等含有黄曲霉素,蒸煮后食用
C.腌制的泡菜虽然含亚硝酸盐,但多吃无妨
D.有的指甲油中国含少量的甲醛,青少年尽量少用
难度: 简单查看答案及解析
-
我市一家企业生产的“土豆农膜”是一种新型环保农膜,在塑料中添加土豆淀粉,可被细菌和微生物释放的酶分解,使塑料呈多孔状+强度下降。下列有关说法错误的是
A.塑料属于天然高分子材料 B.淀粉属于高分子化合物
C.该新型农膜有助于解决农村“白色污染”问题 D.土豆农膜容易降解
难度: 中等查看答案及解析
-
工业上把铁划为黑色金属,纯铁片呈( )
A. 黑色
B. 银白色
C. 金黄色
D. 紫红色
难度: 简单查看答案及解析
-
食盐是重要的调味品,精盐是由粗盐提纯而来,在提纯过程中通常不需要的操作是
A. 蒸发 B. 吸附 C. 过滤 D. 溶解
难度: 中等查看答案及解析
-
目前世界上有近20亿人患有缺铁性贫血。我国政府即将启动“酱油补铁工程”。这里的铁是指( )
A. 铁元素
B. 铁单质
C. 铁分子
D. 铁离子
难度: 简单查看答案及解析
-
下列有关“一定”的说法中,正确的是( )
A. 单质和化合物发生的反应一定是置换反应
B. 混合物一定是由不同种元素组成的
C. 由同种元素组成的物质一定是单质
D. 能分解出氧气的化合物一定是含氧化合物
难度: 中等查看答案及解析
-
同学们在学习酸碱的化学性质时构建了如图知识网络,A、B、C、D是不同类别的无机化合物,“-”表示物质在一定条件下可以发生化学反应。请回答下列问题:
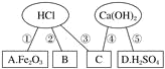
(1)反应①的化学方程式为____________________________________________________;反应的实验现象有___________________________________________。
(2)物质C应是酸、碱、盐中的哪类物质?________。
(3)写出图中一个中和反应的化学方程式________________________________________。
难度: 中等查看答案及解析