-
下列说法中不正确的是
A. K2FeO4可代替Cl2处理饮用水,有杀菌消毒作用
B. CaO2 属于碱性氧化物,也属于离子化合物,其阴阳离子个数比为1:2
C. 《本草纲目》中“以火烧之,紫青烟起,乃真硝石”利用焰色反应区分硝石(KNO3)和朴硝(Na2SO4)
D. 高温下可用金属钠还原四氯化钛来制取金属钛
难度: 中等查看答案及解析
-
下列说法中不正确的有
A. “青蒿一握,以水二升渍,绞取汁”,该过程属于物理变化
B. 食品添加剂对于改善食品外观、防止食品腐败具有重要作用
C. 将适量SO2和CO2分别通入BaC12、CaCl2、Ba(NO3)2溶液中,均无白色沉淀生成
D. “浮梁巧烧瓷,颜色比琼玖”,描述的是陶瓷,陶瓷是一种硅酸盐产品
难度: 中等查看答案及解析
-
设阿伏加德罗常数的值为NA,下列说法正确的是
A. 标准状况下,2.24LCH3OH分子中共价键的数目为0.5NA
B. 1molNa2O2与足量CO2充分反应,转移的电子数为2 NA
C. 用浓盐酸分别和KMnO4、KClO3反应制备l mol氯气,转移的电子数均为2NA
D. 5.6gFe粉与足量S粉加热充分反应转移的电子数为0.2NA
难度: 困难查看答案及解析
-
某溶液X中可能含有下列离子中的若干种:Cl−、SO42−、SO32−、HCO3−、Na+、Mg2+、Fe3+,为了确定该溶液的组成,某同学取100mL上述溶液X,进行了如下实验,下列说法不正确的是
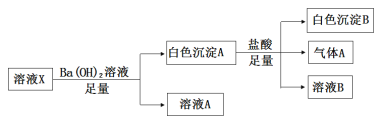
A. 气体A可能是CO2或SO2
B. 溶液X中一定存在SO42−
C. 溶液X中一定不存在Fe3+和Mg2+,可能存在Na+
D. 向溶液A加入硝酸酸化的硝酸银溶液可能生成白色沉淀
难度: 困难查看答案及解析
-
下列实验操作对应的现象和根据现象得出的结论均正确的是
实验操作
现象
结论
A
向FeCl3溶液中加入浓NaOH溶液
溶液由黄色变为红棕色
生成了氢氧化铁胶体
B
向Co2O3中滴入浓盐酸
产生黄绿色气体
氧化性:Cl2>Co2O3
C
向某溶液中滴加K3[Fe(CN)6]溶液
产生蓝色沉淀
溶液中存在亚铁离子
D
向NaHCO3溶液中滴加NaAlO2溶液
有白色沉淀和气体产生
AlO2-与HCO3-发生了双水解反应
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列各组微粒能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式书写正确的是
选项
微粒组
所加试剂
离子方程式
A
NH4+、Mg2+、SO42-
少量Ba(OH)2溶液
NH4++SO42-+Ba2++OH-=BaSO4↓+NH3·H2O
B
Mg2+、HCO3-、Cl-
过量NaOH溶液
Mg2++2HCO3-+40H-=MgCO3↓+2H2O
C
Fe2+、NO3-、Cl-
NaHSO4溶液
3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
D
K+、NH3·H2O、CO32-
通入过量CO2
NH3·H2O+CO2==NH4++HCO3-
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列的图示与对应的叙述相符的是
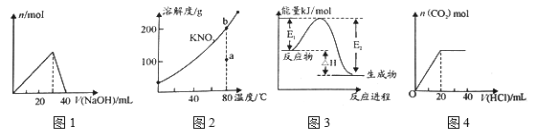
A. 图1表示向l00mL0.l mol·L-l的A1Cl3溶液中滴加1 mol·L-1的NaOH溶液时n [Al(OH)3]的变化情况
B. 图2表示KNO3的溶解度曲线,图中a点表示的溶液通过升温可以得到b点
C. 图3表示某一放热反应,若使用催化剂,E1、E2、△H都会发生改变
D. 图4表示向Na2CO3溶液中滴加稀盐酸时,产生n(CO2)的情况
难度: 困难查看答案及解析

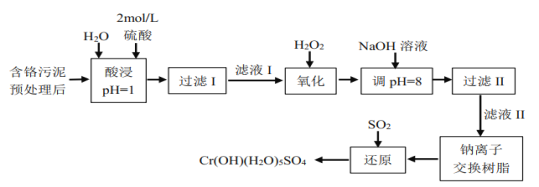

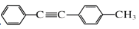 的合成路线(不考虑溶剂的合成): _______________________。
的合成路线(不考虑溶剂的合成): _______________________。