-
能够用来鉴别BaCl2、 NaCl 、 Na2CO3三种物质的试剂是
A. AgNO3溶液 B. 稀硫酸 C. 稀盐酸 D. 稀硝酸
难度: 简单查看答案及解析
-
下列事故或药品的处理正确的是( )
A. 少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
B. 当出现CO中毒时,应立即将中毒者抬到室外新鲜空气处
C. 制取并收集氧气结束后,应立即停止加热
D. 将含硫酸的废液倒入水槽,用水冲入下水道
难度: 中等查看答案及解析
-
下列电离方程式书写正确的是( )
A. NaOH ===Na++ O2-+ H+ B. FeCl3===Fe3++ Cl3-
C. Ca(NO3)2===Ca2++ 2(NO3) 2- D. H2SO4===2H++ SO42-
难度: 简单查看答案及解析
-
下列各组物质相互混合后,不会发生离子反应的是( )
A. Na2SO4溶液和MgCl2溶液 B. Na2CO3溶液和稀硫酸
C. NaOH溶液和Fe2(SO4)3溶液 D. Ca(OH)2溶液和盐酸
难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是( )
A. 钠和冷水反应:Na +2H2O=Na++2OH-+H2↑
B. 金属铝溶于氢氧化钠溶液:Al +2OH-=AlO2-+ H2↑
C. 金属铝溶于盐酸:2Al+6H+=2Al3++3H2↑
D. 铁和稀硫酸反应:Fe+2H+=Fe3++H2↑
难度: 简单查看答案及解析
-
丙酮是一种常用的有机溶剂,可与水以任意体积比互溶,其密度小于1g/ml,沸点约55℃,分离水和丙酮最合理的方法是( )
A. 蒸发 B. 分液 C. 蒸馏 D. 过滤
难度: 中等查看答案及解析
-
图标
 所警示的是( )
所警示的是( )A. 当心火灾——氧化物 B. 当心火灾——易燃物质
C. 当心爆炸——自燃物质 D. 当心爆炸——爆炸性物质
难度: 简单查看答案及解析
-
下列关于Na2O和Na2O2的叙述正确的是( )
A. Na2O比Na2O2稳定 B. 均可与CO2、H2O反应产生氧气
C. 所含氧元素的化合价均为-2 D. 阴阳离子的个数比均为1:2
难度: 中等查看答案及解析
-
某溶液中滴入BaCl2溶液,产生白色沉淀,再滴入稀盐酸,沉淀不溶解,则该溶液中( )
A. 一定有SO42- B. 可能有SO42-或Ag+ C. 一定无Ag+ D. 还可能有CO32-
难度: 简单查看答案及解析
-
若a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是(设NA为阿伏加德罗常数的值)( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 分子总数为NA的NO2和CO2的混合气体中含有的氧原子数为2NA
B. 1mol NaCl中所含电子总数为20NA
C. 46g NO2和N2O4的混合气体中含有的原子总数为4.5NA
D. 常温常压下,22.4L CO2中含有的CO2分子数为NA
难度: 中等查看答案及解析
-
下列配制的溶液浓度偏高的是( )
A. 配制H2SO4溶液,用量筒量取浓硫酸时俯视刻度线
B. 配制溶液定容时,仰视容量瓶刻度线
C. 配制100mL 1.0mol·L-1NaOH溶液,称取药品时砝码错放左盘
D. NaOH溶解后直接注入容量瓶
难度: 简单查看答案及解析
-
下列说法错误的是( )
A. “血液透析”利用了胶体的性质
B. 向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体
C. 葡萄糖注射液不能产生丁达尔现象,不属于胶体
D. 依据丁达尔现象可将分散系分为溶液、胶体与浊液
难度: 简单查看答案及解析
-
如图所示,下列说法不正确的是( )
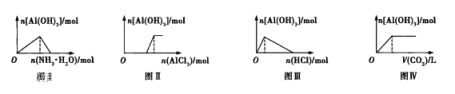
A. 图I表示向以AlCl3溶液中滴加氨水至过量
B. 图Ⅱ表示向NaOH溶液中滴加AlCl3溶液至过量且边滴边振荡
C. 图Ⅲ表示向NaAlO2溶液中滴加稀盐酸至过量且边滴边振荡
D. 图IV表示向NaAlO2溶液中缓慢通入二氧化碳至过量
难度: 中等查看答案及解析
-
中国传统文化对人类文明贡献巨大,古代文献中充分记载了古代化学研究成果,我国晋代《抱朴子》中描述了大量的化学反应,其中有①“丹砂烧之成水银,积变又成丹砂”;②“以曾青涂铁,铁赤色如铜”,下列有关叙述正确的是( )(已知丹砂化学式为HgS)
A. ①中水银“积变又成丹砂”说明水银发生了还原反应
B. ②中反应的离子方程式为2Fe+3Cu2+=2Fe3++3Cu
C. 根据①可知温度计打破后可以用硫粉覆盖水银,防止中毒
D. 水银能跟曾青发生置换反应生成单质铜
难度: 中等查看答案及解析