-
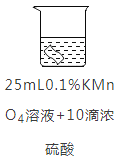
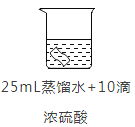
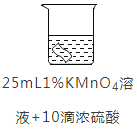
甲、乙、丙三个集气瓶分别盛有空气、氧气、氮气中的一种,用一根燃着的木条分别插人瓶中,观察到的现象依次为:甲中火焰熄灭,乙中木条继续燃烧如初,丙中木条燃烧更旺。则可判断出甲、乙、丙三瓶气体中依次是( )
A. 氧气、氮气、空气 B. 氮气、空气、氧气
C. 空气、氧气、氮气 D. 氮气、氧气、空气
难度: 简单查看答案及解析
-
空气成分中,体积分数最大的是( )
A. 氮气 B. 二氧化碳 C. 氧气 D. 稀有气体
难度: 简单查看答案及解析
-
2019 年北京世园会主题为“绿色生活,美丽家园”。下列做法值得提倡的是
A.任意排放工业废水
B.露天焚烧树叶、秸秆
C.选用一次性筷子、塑料袋
D.将生活垃圾进行分类处理
难度: 简单查看答案及解析
-
下列属于非金属元素的是( )
A. Mg B. Zn C. Cl D. Ag
难度: 中等查看答案及解析
-
下列物质属于纯净物的是
A.冰水混合物 B.澄清石灰水 C.除去氧气后剩余的空气 D.雪碧饮料
难度: 简单查看答案及解析
-
下列物质在氧气中燃烧,火星四射、生成黑色固体的是
A.木炭 B.红磷 C.氢气 D.铁丝
难度: 简单查看答案及解析
-
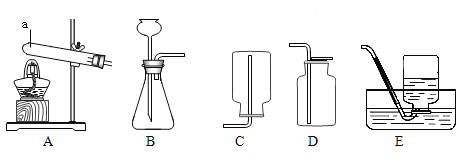
下列实验操作中,正确的是( )
A.倾倒液体
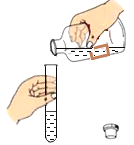 B.过滤
B.过滤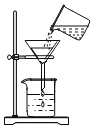
C.加热液体
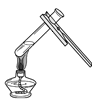 D.称量固体
D.称量固体
难度: 简单查看答案及解析
-
下列物质含有氢分子的是( )
A. H2 B. H2O2 C. H2CO3 D. H2O
难度: 中等查看答案及解析
-
下列物质的用途中,利用其物理性质的是
A.铜用于制作导线
B.氮气用于食品防腐
C.天然气用作燃料
D.氧气用于气焊
难度: 简单查看答案及解析
-
正确量取8ml液体,应选用的最合适仪器是
①5ml量筒 ②10ml量筒 ③50ml量筒 ④胶头滴管
A. ①④ B. ② C. ③④ D. ②④
难度: 中等查看答案及解析
-
25 m3的氧气可以装入0.024 m3的钢瓶中,这说明
A.分子间有间隔 B.分子体积很小 C.分子在不停地运动 D.分子质量很小
难度: 简单查看答案及解析
-
一种碳原子的原子核内有6个质子和8个中子,该碳原子的核电荷数为
A.8 B.6 C.2 D.14
难度: 简单查看答案及解析
-
铼在元素周期表中的相关信息如图所示。下列有说法不正确的是
A.铼的元素符号是Re B.铼原子的核内质子数为75
C.铼是非金属元素 D.铼的相对原子质量为186.2
难度: 简单查看答案及解析
-
下列物质中,由原子直接构成的是
A.氮气 B.水 C.铜 D.氯化钠
难度: 简单查看答案及解析
-
防治佝偻病和骨质疏松症需适量补钙,这里的“钙”指的是
A.钙单质 B.钙的化合物
C.碳酸钙 D.钙元素
难度: 简单查看答案及解析
-
下列物质的化学式不正确的是
A.二氧化碳— CO2
B.氢氧化钙—Ca(OH)2
C.碳酸钠—NaCO3
D.氧化铁—Fe2O3
难度: 简单查看答案及解析
-
地壳中含量最多的金属元素与地壳中含量最多的非金属元素形成的化合物化学式是
A.Fe2O3 B.Fe3O4 C.Al2O3 D.SiO2
难度: 简单查看答案及解析
-
下列关于葡萄糖(C6H12O6)的说法中,正确的是
A. 葡萄糖中碳、氢元素质量比为1∶2 B. 葡萄糖由24个原子构成
C. 1个葡萄糖分子中含有6个水分子 D. 葡萄糖由三种元素组成
难度: 简单查看答案及解析
-
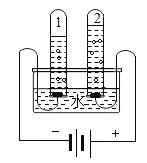
用下图装置进行实验。下列现象能证明空气中O2的含量的是( )
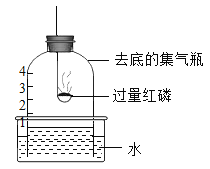
A. 红磷燃烧,产生白烟 B. 瓶中液面先下降,后上升
C. 瓶中液面最终上升至1处 D. 水槽中液面下降
难度: 中等查看答案及解析
-
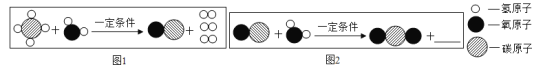
已知某两种物质在一定条件下能发生化学反应,其反应的微观示意图如下,则下列说法中,正确的是
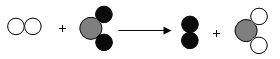
(说明: 一种小球代表一种元素的原子)
A.图中的反应物都是化合物
B.反应前后,原子的种类和个数均不变
C.反应前后,分子种类不变
D.该反应不符合质量守恒定律
难度: 简单查看答案及解析
-
下列反应类型中,属于化合反应的是
A.CH4+2O2
CO2+ 2H2O B.CaO+ H2O=Ca(OH)2
C.Zn+ H2SO4(稀)=ZnSO4 +H2↑ D.CaCO3
CaO+CO2↑
难度: 简单查看答案及解析
-
下列化学方程式书写正确的是
A.C+O2=CO2
B.H2O2
H2↑+O2↑
C.P+O2
P2O5
D.Fe +CuSO4=FeSO4+ Cu
难度: 简单查看答案及解析
-
实验室利用过氧化氢、高锰酸钾、水等物质发生分解反应来制取氧气,原因之一是它们
A.都属于氧化物
B.都含有氧气
C.都含有氧元素
D.都含有氧气分子
难度: 简单查看答案及解析
-
下列关于2CO+O2
2CO2的说法中,正确的是( )
A.反应后原子种类减少
B.表示一氧化碳加氧气等于二氧化碳
C.参加反应的一氧化碳与氧气的质量比为2:1
D.参加反应的氧气与生成的二氧化碳的分子个数比为1:2
难度: 中等查看答案及解析
-
下列中草药煎制步骤中,属于过滤操作的是
A.冷水浸泡
B.加热煎制
C.箅渣取液
D.灌装保存

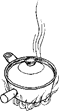
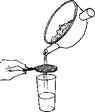
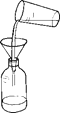
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
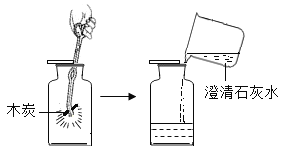
钠着火不能用二氧化碳灭火。钠在二氧化碳中燃烧生成炭黑和一种白色固体,它可能是( )
A. 碳酸钠 B. 硫酸钠 C. 碳酸氢钠 D. 氢氧化钠
难度: 简单查看答案及解析
-
下图为尿素(CO(NH2)2)中各个元素质量分数的示意图,其中表示氧元素质量分数的
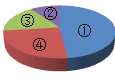
A. ① B. ② C. ③ D. ④
难度: 简单查看答案及解析
-
某可燃物在空气中燃烧时,只产生二氧化碳和水,关于该可燃物的组成的推论正确的是
A.只含有C、O元素 B.只含有C、H元素
C.一定含有C、H、O元素 D.一定含有C、H元素,可能含有O元素
难度: 中等查看答案及解析
-
丙烷(C3H8)是液化石油气的主要成分之一,燃烧前后分子种类变化微观示意图如下。下列说法正确的是
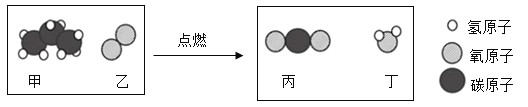
A.甲中碳、氢元素质量比为3:8 B.乙和丙元素组成相同
C.44g甲含碳元素的质量为36g D.生成丙与丁的分子个数比为1:1
难度: 中等查看答案及解析
-
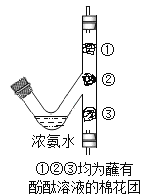
可用推拉注射器活塞的方法检查图中装置的气密性,当缓慢向左推活塞时,如果装置气密性良好,可观察到
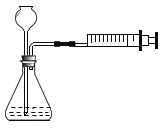
A.长颈漏斗下端管口有气泡冒出
B.锥形瓶中液面明显上升
C.长颈漏斗下端导管内有液柱上升
D.注射器内有液体进入
难度: 简单查看答案及解析