-
下列化合物中氯元素的化合价最低的是( )
A. Cl2 B. KCl C. KClO3 D. KClO
难度: 简单查看答案及解析
-
下列清洁用品中碱性最强的是
A. 厕所清洁剂pH=1 B. 牙膏pH=8 C. 肥皂pH=10 D. 炉具清洁剂pH=13
难度: 简单查看答案及解析
-
高锰酸钾和浓盐酸发生如下反应:2KMnO4+16HCl=2KC1+2X+5Cl2↑+8H2O,则X的化学式是( )
A. MnCl2 B. MnO2 C. ClO2 D. HClO
难度: 简单查看答案及解析
-
下列属于化学变化的是( )
A. 食物腐败 B. 矿石粉碎 C. 木已成舟 D. 干冰气化
难度: 简单查看答案及解析
-
下列物质名称与俗名不对应的是( )
A. 氢氧化钙(熟石灰) B. 氢氧化钠(烧碱)
C. 乙醇(酒精) D. 碳酸钠(小苏打)
难度: 中等查看答案及解析
-
下列溧阳土特产中富含蛋白质的是( )
A. 白茶 B. 板栗 C. 鸟米饭 D. 鸡蛋
难度: 简单查看答案及解析
-
下列属于物理性质的是( )
A. 毒性 B. 还原性 C. 挥发性 D. 可燃性
难度: 简单查看答案及解析
-
动物的肝脏和坚果类食物中含有丰富的铁和锌,这里的“铁”和“锌”是指( )
A. 维生素 B. 原子 C. 元素 D. 单质
难度: 简单查看答案及解析
-
芯片是内含集成电路的硅片,如图是硅元素在元素周期表中的相关信息,下列说法正确的是( )

A. 硅元素属于金属元素
B. 硅原子核内有14个质子
C. 硅的相对原子质量为28.1g
D. 硅元素是地壳中含量最高的元素
难度: 中等查看答案及解析
-
下列涉及化学学科观点的有关说法中,错误的是( )
A. 微粒观:水是由水分子构成的
B. 转化观:CO2和CaCO3在一定条件下可以相互转化
C. 守恒观:水通电分解后,看不到其他物质生成,因此不存在质量守恒
D. 元素观:酸和碱在组成上都含有氢元素
难度: 中等查看答案及解析
-
下列有关溶液的叙述中,正确的是( )
A. 饱和溶液一定比不饱和溶液浓
B. 某液体静置后不分层,该液体一定是溶液
C. 增加溶剂的量可使溶解度增大
D. 某溶液析出晶体后,其溶质质量分数可能不变
难度: 中等查看答案及解析
-
下列有关实验现象的描述中,不正确的是( )
A. 鸡蛋清中加浓硝酸微热后变黄
B. 硫在氧气中燃烧发出蓝紫色火焰
C. 灼烧棉线有烧焦羽毛气味
D. 镁条在空气中燃烧生成白色固体
难度: 中等查看答案及解析
-
下列实验不能达到实验目的是( )
A.
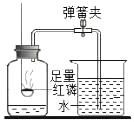 测定空气中氧气含量
测定空气中氧气含量B.
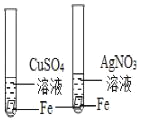 验证Fe、Cu、Ag的活动性
验证Fe、Cu、Ag的活动性C.
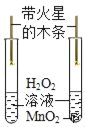 探究MnO2能否加快H2O2分解
探究MnO2能否加快H2O2分解D.
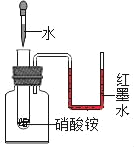 验证硝酸铵溶于水吸热
验证硝酸铵溶于水吸热难度: 中等查看答案及解析
-
某化学反应的微观示意图如图所示,下列叙述不正确的是( )
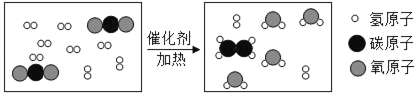
A. 该反应属于置换反应
B. 该反应中原子没有发生改变
C. 该反应生成了两种物质
D. 参加反应的CO2和H2分子个数比为1:3
难度: 中等查看答案及解析
-
下列转化不能一步实现的是( )
A. H2O→O2 B. CuO→Cu(OH)2
C. Fe→Fe3O4 D. .Ca(OH)2→NH3
难度: 中等查看答案及解析
-
碳酸乙烯酯(C3H4O3)可用作锂电池电解液,下列有关说法正确的是( )
A. 碳酸乙烯酯属于有机化合物
B. 碳酸乙烯酯中碳元素和氢元素的质量比为6:1
C. 碳酸乙烯酯的相对分子质量为88g
D. 碳酸乙烯酯分子由碳、氢、氧三种元素组成
难度: 中等查看答案及解析
-
除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
物质
杂质
除杂所用的试剂和方法
A
CaO
CaCO3
加入适量的水、过滤、蒸发
B
SO2
水蒸气
把气体通过盛有生石灰的干燥管
C
NaCl
Na2CO3
加入稍过量的稀盐酸、蒸发
D
K2SO4溶液
CuSO4
加入过量的氢氧化钾溶液、过滤
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
甲、乙、丙是初中化学中常见的三种物质,它们有如图所示的转化关系。下列说法不正确的是( )
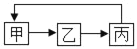
A. 若甲是氧化物则丙可能是盐
B. 若甲是非金属单质则丙可能是酸
C. 若甲是非金属单质则丙可能是氧化物
D. 若甲是金属单质则丙可能是碱
难度: 困难查看答案及解析
-
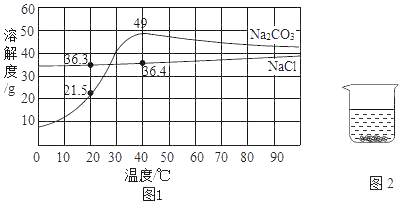
为探究CO2与NaOH溶液发生的反应,某兴趣小组将CO2持续通入一定浓度一定量的NaOH溶液中,用数字化实验技术测定反应过程中溶液的pH和温度变化,结果如图1、图2所示(实验条件下,Na2CO3溶液和 NaHCO3溶液的pH分别约为11.0和8.5)。下列说法不正确的是( )
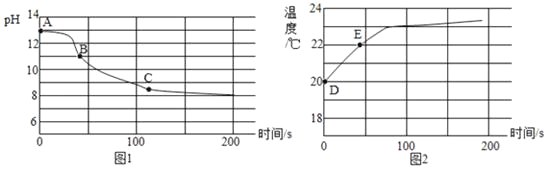
A. 二氧化碳与氢氧化钠反应放热
B. 图1中,BC段发生的反应是CO2+Na2CO3+H2O=2 NaHCO3
C. 图1中,pH=12时对应溶液中的溶质只含Na2CO3和NaHCO3
D. 对于现象不明显的反应,可通过现代技术手段实现反应过程的“可视化”
难度: 中等查看答案及解析
-
将4.84g某纯净的铁的氧化物,与足量的一氧化碳在加热的条件下完全反应,反应生成的气体被足量的澄清石灰水完全吸收,得到11.0g白色沉淀,则该铁的氧化物的化学式为( )
A. FeO B. FeO2 C. Fe2O3 D. Fe3O4
难度: 中等查看答案及解析