-
请按照要求完成下列金属性质的探究:
探究一:铝片与盐酸反应过程中的能量及反应速率的变化。
(1)实验时需将铝片进行打磨,其目的是_____。
(2)反应中试管外壁发烫,说明铝与盐酸反应是_____(填“吸热”或“放热”)反应,化学方程式为_____。
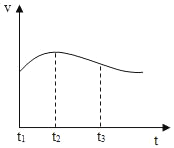
(3)实验测得铝片产生气体的速率(v)与时间(t)的关系如图所示,t1~t2时间内反应逐渐加快的主要原因是_____。
(查阅资料)铁、铜均能与氯化铁溶液反应,化学方程式分别为:2FeC13+Fe═3FeCl2、2FeCl3+Cu=2FeCl2+CuCl2
(4)向氯化铁和氯化铜的混合溶液中,加入一定量的铁粉,充分反应后过滤。取少量滤渣加入稀盐酸,有气泡产生。则滤液中的溶质是_____,滤渣中一定含有_____。
-
请按要求完成下列金属性质的实验。
探究一:金属与酸反应过程中的能量变化。
(1)打磨后的镁条与稀盐酸反应,试管外壁发烫,说明该反应________(填“吸热”或“放热”),反应的化学方程式为____________________________________________________。
(2)实验测得反应中产生气体的速率(v)与时间(t)的关系如图,请根据t1~t2时间段反应速率的变化,说明化学反应速率受________等因素影响。

探究二:金属与金属化合物溶液反应过程中的相关变化。
(3)某同学用硫酸铜溶液把“铁勺”变“铜勺”,其反应的化学方程式为______________________。
-
(4分)请按要求完成下列金属性质的实验:
研究一:金属与酸反应过程中的能量变化.
(1)打磨后的镁条与稀盐酸反应,试管外壁发烫,说明该反应 (填“吸热”或“放热”),反应的化学方程式为 .
(2)实验测得反应中产生的气体的速率(v)与时间(t)的关系如图,请根据t1﹣t2时间段反应速率变化,说明化学反应速率受 等因素影响.

研究二:金属与盐溶液反应过程中的相关变化.
(1)某同学用硫酸铜溶液把“铁勺”变“铜勺”,其反应的化学方程式为 .
(2)在一定量AgNO3和Cu(NO3)2的混合溶液中加入铁粉,充分反应后,下图描述相关变化曲线,一定不正确的是 .

-
请按要求完成下列金属性质的实验:
研究一:金属与酸反应过程中的能量变化.
(1)打磨后的镁条与稀盐酸反应,试管外壁发烫,说明该反应_____(填“吸热”或“放热”),反应的化学方程式为______________.
(2)实验测得反应中产生的气体的速率(v)与时间(t)的关系如图,请根据t1﹣t2时间段反应速率变化,说明化学反应速率受___________________等因素影响.

研究二:金属与盐溶液反应过程中的相关变化.
(1)某同学用硫酸铜溶液把“铁勺”变“铜勺”,其反应的化学方程式为_____________.
(2)在一定量AgNO3和Cu(NO3)2的混合溶液中加入铁粉,充分反应后,下图描述相关变化曲线,一定不正确的是____________.

-
请按要求完成下列物质性质的实验:
研究一:金属与酸反应过程中的能量变化。
(1)打磨后的镁条与稀盐酸反应,试管外壁发烫,说明该反应_____(填“放热”或“吸热”),反应的化学方程式为:_________;
(2)实验测得反应中产生气体的速率(v)与时间(t)的关系如下图,请根据t1~t2时间段反应速率变化,说明化学反应速率受__________等因素影响。

研究二:金属与氧气的反应:
(3)将一镁条取出发现其表面有一层灰白色物质,猜想这一物质可能是:______。(填化学式)
(4)再将镁条用砂纸打磨,表面变为光亮的银白色,用坩埚钳夹住镁条在酒精灯上点燃观察到的现象为:_____________。
(5)写出镁在空气中燃烧的化学方程式式:_________。由此说明,化学反应常常伴随能量的变化。
-
实验小组同学探究金属的化学性质。他们将打磨好表面积相同的铝片分别放入不同浓度的稀盐酸中,结果发现产生气泡的速率明显不同。
(1)写出该反应的化学方程式:_____。
(2)实验小组的同学根据所学的知识得出:_______影响了该反应速率。
(3)打磨铝片的目的:_______。
实验小组的同学偶然发现把硫酸铜溶液加入到上述试管中,发现反应的速率明显加快。
[提出问题] 硫酸铜溶液中的什么粒子导致反应速率明显加快的?
[作出猜想] 猜想一:硫酸铜溶液中的水分子;
猜想二:硫酸铜溶液中的硫酸根离子;
猜想三:______;
上述猜想____肯定是错误的,原因:____。
[进行实验]
取三只干净的试管,分别向试管中加入打磨干净的表面积相同的铝片,再分别加入相同体积相同浓度的稀盐酸:
(1)向第一支试管中加入氯化钠晶体,观察到产生气泡的速率不变,得出_离子对实验没有影响;
(2)向第二支试管中加入__晶体,观察到产生气泡的速率不变,得出硫酸根离子对实验没有影响;
(3)向第三支试管中继续加入___晶体,观察到产生气泡的速率明显加快,得出猜想三成立;
[反思] 上述实验的第3步,还可以加入___晶体,也可以验证猜想三成立。
-
2013年合肥市化学实验考试试题之一就是探究金属的某些物理性质和化学性质,该实验内容之一是:用镊子将打磨后的铝片放入试管中,然后倒入约3mL的稀盐酸.同学们在实验过程中发现,铝片一开始和稀盐酸反应只是冒出小气泡,过一段时间后才变得越来越快.请你和同学们一道探究铝与稀盐酸的反应速率究竟受到什么因素的影响?
(1)写出铝与盐酸反应的化学方程式________;
(2)【猜想一】温度越高,反应速率越快?
【猜想依据】活泼金属和盐酸反应是________(填写“放热”或“吸热”)反应;
【进行实验】在实验开始和实验很剧烈的时候分别轻触试管外壁,会发现试管温度________;
【实验拓展】同学们也发现,时间在延长一点,铝片和酸反应的速率又会降低下来,你认为可能的原因是________;
【设计实验】
(6)(注意:若答对本小题奖励4分,化学试卷总分不超过60分.)
你认为影响铝和盐酸反应速率的因素还有________.
-
小明同学在练习“金属的化学性质”实验操作时,将没有打磨的铝片放入试管中,加入稀盐酸,结果发现产生的气泡很慢,于是他想:铝与稀盐酸反应的速率受哪些因素影响呢?经过认真思考,小明认为铝与稀盐酸反应的速率与酸的浓度、反应的温度有关,如表是他设计的实验和记录的数据(每次实验用相同质量的铝片和足量的稀盐酸反应).请你根据表中的信息填空:
| 实验 编号 | 温度 | 盐酸 浓度 | 铝片消失的时间/s |
| ① | 20℃ | 5% | 60 |
| ② | 20℃ | 10% | 42 |
| ③ | 40℃ | 10% | 30 |
(1)没有打磨的铝片和稀盐酸反应慢的原因是, .写出铝与稀盐酸反应的化学方程式 .
(2)小明设计实验组合①②的目的是探究 ;实验组合②③的目的是探究 ;本实验的结论是 .
(3)除了用铝片消失的时间来衡量反应的快慢,还可以用 方法来衡量反应的快慢.
(4)小明将稀盐酸换成稀硫酸继续实验,发现铝丝和稀硫酸反应现象不明显.
【发现问题】为什么铝丝易与稀盐酸反应而难与稀硫酸反应呢?
【提出假设】Cl﹣的存在使酸和铝的反应容易进行.
【设计实验】如果你能帮助小明设计一个合理的实验来验证假设 .
-
以下是甲、乙两同学对有关镁与盐酸反应的系列研究研究一:镁与盐酸反应过程中的能量变化以及反应速率的变化:

(1)实验时需将镁条进行打磨,其目的是。
(2) 反应中试管外壁发烫,说明镁与稀盐酸反应是反应(填“吸热”或“放热”),化学方程式为
(3)实验测得镁片产生气体的速率(v)与时间(t)的关系如图所示,则t1~t2时间内反应速率逐渐加快的主要原因是。

研究二.反应后所得溶液的酸碱性探究
【发现问题】
(1)反应后甲同学用pH试纸测定试管中溶液的酸碱性,发现pH小于7,说明甲同学所得溶液呈________性,(选填“酸”“碱”或“中”)。
(2)反应后乙同学的试管中镁条有剩余,向试液中滴入两滴酚酞溶液,振荡显红色,说明乙同学所得溶液呈________性。对此现象,乙同学重复如上实验,得到同样结果。
【提出猜想】
甲同学:猜想Ⅰ:稀盐酸过量,使溶液pH小于7;猜想Ⅱ:氯化镁溶液pH小于7。
乙同学:猜想Ⅰ:氯化镁溶液使酚酞变红色; 猜想Ⅱ:镁与热水反应使酚酞变红色。
【实验与思考】
为验证猜想,甲、乙两同学均需测定________溶液的酸碱性,实验表明该溶液显弱酸性。
乙同学为完成猜想Ⅱ,在滴有两滴酚酞的热水中放入一段打磨过的镁条,观察到溶液很快变为红色,同时还观察到镁条表面有气体生成,收集并点燃该气体,发现能燃烧,请根据实验现象写出镁与水反应的化学反应方程式________。
【结论】
镁与稀盐酸反应,镁反应完全后所得溶液显酸性;
镁与稀盐酸反应,镁过量时所得溶液显碱性。
【拓展与延伸】
(1)金属氯化物的水溶液可能显中性或弱酸性;与金属的活动性顺序有关,如氯化钠溶液显中性,氯化镁溶液显弱酸性,氯化钾溶液显________性。
(2)活泼金属能与水在一定条件下反应。实验发现钠与冷水剧烈反应,产生大量的气体。由此可见金属与水反应与金属的活动性顺序_______(填“有关”或“无关”)。
研究三. 金属活动性强弱与原子结构的关系
下图为镁原子、钙原子和钡离子结构示意图,据此推测,这三种金属的活动性最强的是
__________________。

【解析】研究一、
(1)依据镁的化学性质较活泼易形成氧化镁保护膜进行分析;
(2)依据反应时温度的变化分析反应时能量的问题,依据镁与盐酸反应会生成氢气及氯化镁书写方程式;
研究二、
发现问题:依据酸碱性溶液pH的大小进行分析判断;
实验思考:根据甲乙同学的不同猜想分析两人必做的实验操作,以据反应的现象结合质量守恒定律的有关应用对化学方程式进行书写即可;
拓展延伸:(1)依据题目中有关的信息对相关物质的溶液酸碱性进行判断即可;
(2)根据活泼金属与水反应的条件分析即可;
研究三、根据钠镁活动性强弱的关系分析三种金属中活动性最强的物质即可.
-
某校课外兴趣小组同学对有关镁与盐酸反应的系列研究:
研究一:镁与盐酸反应过程中的能量变化以及反应速率的变化:
(1)实验时需将镁条进行打磨,其目的是_____。
(2)反应中试管外壁发烫,说明镁与稀盐酸反应是_____反应,化学方程式为_____。
(3)实验 测得镁片产生气体的速率(v)与时间(t)的关系如图所示,则 t1~t2 时间 内反应速率逐渐加快的主要原因是_____。

研究二:探究反应后所得溶液的酸碱性
(发现问题]
(1)反应后甲同学用 pH 试纸测定试管中溶液的酸碱性,发现 pH 小于 7。
(2)反应后乙同学的试管中镁条有剩余,向试液中滴入两滴酚酞溶液,振荡显红色, 对此现象,乙同学重复如上实验,得到同样结果。
(提出猜想)甲同学:猜想Ⅰ:稀盐酸过量,使溶液 pH 小于 7;
猜想Ⅱ:氯化镁溶液 pH 小于 7. 乙同学:猜想Ⅰ:氯化镁溶液使酚酞变红色;
猜想Ⅱ:镁与热水反应使酚酞溶液变红色。
(实践与思考)为验证猜想,甲、乙两同学均需进行一个探究实验是_____. 乙同学为完成猜想Ⅱ,在滴有两滴酚酞的热水中放入一段打磨过的镁条,观察到溶液很 快变为红色,同时还观察到镁条表面有气体生成.该气体能燃烧。请你根据实验现象写 出镁与水反应的化学反应方程式_____。
(结论)(1)镁与稀盐酸反应,镁反应完全后所得溶液显酸性;
(2)镁与稀盐酸反应,镁过量时所得溶液显碱性。
(交流与反思)氯化钠溶液呈中性,而上述甲同学实验中镁完全反应后所得溶液显酸 性,你认为与溶液中_____(填离子符号)。
一段时间后,乙同学观察到溶液红色逐渐变淡,最后消失,你认为原因可能是_____ 请设计实验验证你的猜想_____。





