-
爱国科学家侯德榜先生发明了侯氏制碱法,为我国民族工业的发展做出了杰出的贡献,该方法是将CO2和NH3通入饱和的NaCl溶液中充分反应,其中的一步反应是NH4HCO3+NaCl==NaHCO3↓+NH4Cl,下列叙述错误的是( )
A. 该反应不符合复分解反应发生的条件 B. 该反应中四种物质都是盐
C. 反应后可用过滤的方法分离出NaHCO3 D. 反应后的溶液中还能继续溶解NaCl
难度: 简单查看答案及解析
-
将适量的铜粉和镁粉的混合物放入一定量的硝酸银溶液中,充分反应后过滤,得到固体物质和无色滤液,则关于滤出的固体和无色滤液的下列判断正确的是( )
A. 滤出的固体中一定含有银和铜,一定不含镁
B. 滤出的固体中一定含有银,可能含有铜和镁
C. 滤液中一定含有硝酸银和硝酸镁,一定没有硝酸铜
D. 滤液中一定含有硝酸镁,一定没有硝酸银和硝酸铜
难度: 中等查看答案及解析
-
人体中发生的以下变化属于物理变化的是( )
A. 汗水的挥发 B. 蛋白质的水解 C. 葡萄糖的氧化 D. 油脂的消化吸收
难度: 简单查看答案及解析
-
对比分析不同物质的共性与差异是学习化学的有效方法。下列关于CO2和CO的各项对比,有错误的是( )
选项
共性
差异性
A
均由分子构成
分子的种类不同
B
均由碳元素和氧元素组成
元素的质量比不同
C
均能与水化合
化合时现象不同
D
常温下均是无色气体
相同条件下气体的密度不同
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列关于稀有气体的叙述中,错误的是( )
A. 空气中稀有气体含量虽少,但却包含了氦;氖;氩、氪、氙等多种气体
B. 因为稀有气体化学性质很不活泼,所以不能与其它任何物质发生化学反应
C. 稀有气体不仅可作保护气,而且作为制冷剂制造低温环境
D. 稀有气体充入灯泡内,不仅能使灯泡经久耐用,而且还能发出不同颜色的光
难度: 简单查看答案及解析
-
如图为某原子的结构示意图,下列说法不正确的是( )

A.该原子的质子数为6
B.该原子的核电荷数为16
C.该原子的最外层电子数为6
D.该原子的核外共有3个电子层
难度: 简单查看答案及解析
-
测定人体内体液的pH,可以帮助人们了解身体的健康状况,一些体液的近似pH如下:下列液体中,碱性最强的是( )
液体
胃液
胰液
胆汁
血浆
PH
0.9﹣1.5
7.5﹣8.0
7.1﹣7.3
7.35﹣7.45
A. 胃液 B. 胰液 C. 胆汁 D. 血浆
难度: 简单查看答案及解析
-
下列物质:①洁净的空气、②干冰、③水银、④不锈钢、⑤冰水混合物、⑥高锰酸钾、⑦液氧,分类不正确的是( )
A. 混合物:①③④ B. 氧化物:②⑤ C. 单质:③⑦ D. 化合物:②⑤⑥
难度: 中等查看答案及解析
-
在一密闭容器中,有四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如下表:已知X的相对分子质量为n、Q的相对分子质量为2n.下列推理中正确的是 ( )
物质
X
Y
Z
Q
反应前质量/g
4
10
1
21
反应后质量/g
0
12
15
待测
A. 该反应后待测Q质量为12g
B. 反应后生成15gZ
C. 该化学方程式中X与Q的化学计量数之比为2:3
D. 该反应中Y与Q质量之比为1:1
难度: 中等查看答案及解析
-
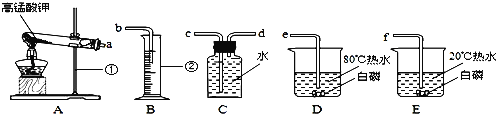
下列实验基本操作错误的是( )
A.
B.
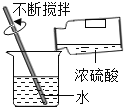 C.
C. 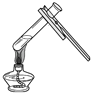 D.
D. 难度: 简单查看答案及解析
-
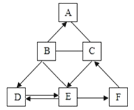
如图是小凡用手势OK表示初中常见化学反应中生成水的不同方法,要求手指上的物质分别通过某种反应的基本类型直接生成水(如图中的H2O2、O2)则物质X一定不是下列物质中的 ( )
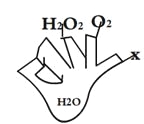
A. H2 B. H2CO3 C. CH4 D. KOH
难度: 困难查看答案及解析
-
往硫酸和硫酸铜的混合溶液中,逐滴加入氢氧化钠溶液直至过量,根据实验实施绘制如图所示曲线,下列说法正确的是( )
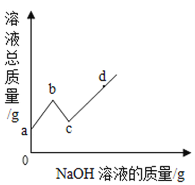
A.a至b段有蓝色沉淀生成
B.d点溶质种类为三种
C.c至d段,溶液pH不断减少
D.c点所含的溶质种类最少
难度: 困难查看答案及解析