-
用四氯化碳萃取碘的饱和水溶液中的碘,下列说法中不正确的是 ( )
A. 实验时使用的主要仪器是分液漏斗
B. 碘在四氯化碳中的溶解度比在水中的溶解度大
C. 碘的四氯化碳溶液呈紫红色
D. 分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从分液漏斗上口倒出
难度: 中等查看答案及解析
-
下列离子检验的方法正确的是( )
A. 某溶液中加硝酸银溶液生成白色沉淀,说明原溶液中有Cl–
B. 某溶液中加BaCl2溶液生成白色沉淀,说明原溶液中有SO42–
C. 某溶液中加NaOH溶液生成蓝色沉淀,说明原溶液中有Cu2+
D. 某溶液加稀硫酸生成白色沉淀,说明原溶液中有Ba2+
难度: 中等查看答案及解析
-
下列叙述错误的是( )
①摩尔是国际单位制中七个基本物理量之一;
②1mol任何物质都含有约6.02×1023个原子;
③6.02×1023就是阿伏加德罗常数;
④氢原子的摩尔质量是1g;
⑤HCl的摩尔质量等于1molHCl分子的质量;
⑥1molCO2中含有1mol碳和2mol氧。
A. ①②③ B. ②③④ C. ②④④⑥ D. 全部
难度: 中等查看答案及解析
-
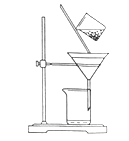
用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是( )

A. 称量 B. 溶解 C. 转移 D. 定容
难度: 简单查看答案及解析
-
下列有关气体体积叙述正确的是
A. 一定温度、压强下,气体体积由其分子的大小决定
B. 一定温度、压强下,气体体积由其物质的量的多少决定
C. 气体摩尔体积是指1mol任何气体所占的体积约为22.4L
D. 不同的气体,若体积不等,则它们所含的分子数一定不等
难度: 中等查看答案及解析
-
与50 mL 0.1 mol·L-1 K2CO3 溶液中 K+ 的物质的量浓度相同的溶液是
A. 50mL 0.2mol·L-1 的 KCl 溶液 B. 100mL 0.1mol·L-1 的 KCl 溶液
C. 25mL 0.2mol·L-1 的 K2SO4 溶液 D. 10mL 0.5mol·L-1 的 K2CO3 溶液
难度: 中等查看答案及解析
-
已知1.505×1023个X气体分子的质量为8 g,则X气体的摩尔质量是
A. 16 g B. 32 g C. 64 g/mol D. 32 g /mol
难度: 中等查看答案及解析
-
Na2O、NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为同一类物质,下列分类标准正确的是
①化合物 ②能与硝酸反应 ③钠盐 ④氧化物
A. ②④ B. ①②④ C. ①③ D. ①
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A. 标准状况下,11.2 L H2O含有的分子数为0.5NA
B. 25 ℃,1.01×105 Pa,64 g SO2中含有的原子数大于3NA
C. 40 g NaOH溶解在1 L水中,则其100 mL溶液中含Na+数为0.1NA
D. 在25 ℃、1.01×105Pa的条件下,2.24 L H2中含有的分子数小于0.1NA
难度: 困难查看答案及解析
-
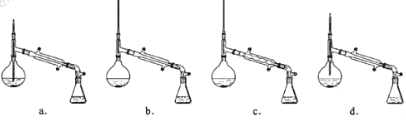
从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是



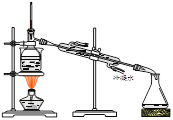
A.海带灼烧成灰 B.过滤得含I-溶液 C.放出碘的苯溶液 D.分离碘并回收苯
难度: 简单查看答案及解析
-
某同学用Na2CO3配制0.10 mol/L Na2CO3溶液的过程如图所示。你认为该同学的错误有
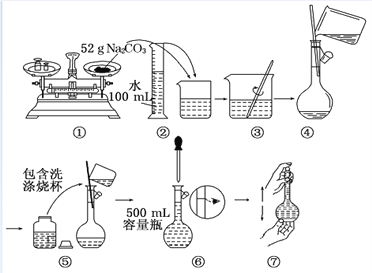
A. ①⑤⑥ B. ②④⑦ C. ①⑥⑦ D. ⑤⑥⑦
难度: 中等查看答案及解析
-
标准状况下某种O2和N2的混合气体mg含有b个分子,则ng该混合气体在相同状况下所占的体积应是
A.
B.
C.
D.
难度: 困难查看答案及解析
-
VL Fe2(SO4)3溶液中含有ag SO42﹣,取此溶液0.5VL,用水稀释至2VL,则稀释后溶液中Fe3+的物质的量的浓度为
A.
mol/L B.
mol/L C.
mol/L D.
mol/L
难度: 困难查看答案及解析
-
在两个容积相同的容器中,一个盛有NH3,另一个盛有H2和O2的混合气体。在同温同压下,两容器内的气体不可能具有相同的
A. 原子数 B. 分子数 C. 质量 D. 电子数
难度: 困难查看答案及解析
-
已知25%氨水的密度为0.91g.cm-3,5%氨水的密度为0.98g.cm-3,若将上述两溶液等体积混合,所得氨水溶液的质量分数是
A. 等于15% B. 大于15% C. 小于15% D. 无法估算
难度: 中等查看答案及解析
-
用98%的浓硫酸(密度为1.84 g·cm-3)配制80 mL 1 mol·L-1的稀硫酸。现给出下列仪器(配制过程中可能用到):①100 mL量筒 ②10 mL量筒 ③50 mL烧杯 ④托盘天平 ⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻璃棒 ⑧80 mL容量瓶 按使用仪器的先后顺序排列正确的是
A. ④③⑦⑧⑥ B. ②⑤⑦⑥
C. ①③⑧⑥⑦ D. ②⑥③⑦⑤⑥
难度: 中等查看答案及解析
-
把500 mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀。其它三份留待其它实验使用。则该混合溶液中钾离子浓度为( )
A. 0.1(b-2a) mol·L-1
B. 10(2a-b) mol·L-1
C. 10(b-a) mol·L-1
D. 10(b-2a) mol·L-1
难度: 困难查看答案及解析
-
在标准状况下,将a L HCl完全溶于水得到V mL盐酸,溶液的密度为ρ g·cm-3,溶质的质量分数为w,溶质的物质的量浓度为c mol·L-1。下列叙述中正确的是
①c=
×100% ②c=
③若上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w ④将50 g上述溶液加入一定量的水稀释成0.5c mol·L-1,则加入水的体积应大于50 mL
A. ①④ B. ②③
C. ①③ D. ②④
难度: 困难查看答案及解析




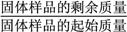 ×100%)随温度的变化如下图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。
×100%)随温度的变化如下图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。