-
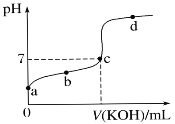
25℃时,在10mL浓度均为0.1mol/LNaOH和NH3·H2O混合溶液中,滴加0.1mol/L的盐酸,下列有关溶液中粒子浓度关系正确的是
A. 未加盐酸时:c(OH-)>c(Na+)= c(NH3·H2O)
B. 加入10mL盐酸时:c(NH4+) +c(H+) = c(OH-)
C. 加入盐酸至溶液pH=7时:c(Cl-) = c(Na+)
D. 加入20mL盐酸时:c(Cl-) =c(NH4+) +c(Na+)
难度: 中等查看答案及解析
-
下列离子方程式,书写正确的是
A. H2S
2H++S2
B. KHCO3
K++H++CO32-
C. Cu(OH)2
Cu2++2OH
D. HClO===H++ClO
难度: 简单查看答案及解析
-
下列化学用语表达正确的是
A. 丙烯的结构简式:CH3CHCH2 B. 乙炔的电子式:H∶C∶∶C∶H
C. 乙酸的实验式:C2H4O2 D. 乙烯的结构式:
难度: 简单查看答案及解析
-
只用水不能鉴别的一组物质是
A. 乙酸乙酯和乙醇 B. 乙醇和乙酸
C. 汽油和氯化钠溶液 D. 苯和硝基苯
难度: 简单查看答案及解析
-
下列说法不正确的一组是
A. H和D互为同位素 B. 丁烯和环丁烷互为同分异构体
C. 碳链
与
的烃为同系物 D. 金刚石、石墨和C60为同素异形体
难度: 简单查看答案及解析
-
下列叙述正确的是
A. 铜、铁和FeCl3溶液形成的原电池,铜电极放出氢气
B. 电解滴加了酚酞的氯化钠溶液,阳极附近溶液变红
C. 铅蓄电池负极反应为:Pb-2e-=Pb2+
D. 铁锅生锈的正极反应为:O2+2H2O+4e-===4OH-
难度: 中等查看答案及解析
-
下列关于乙烷、乙烯、乙炔的说法正确的是
①它们既不是同系物,也不是同分异构体
②乙烷是饱和烃,乙烯、乙炔是不饱和烃
③乙烯、乙炔能使溴水褪色,乙烷不能使溴水褪色
④它们都能燃烧,乙炔燃烧火焰最明亮,有浓烟
⑤它们都能使酸性KMnO4溶液褪色
A. ①③④ B. ①②③⑤ C. ②③④⑤ D. ①②③④
难度: 中等查看答案及解析
-
下列各组中的两种物质各1mol,分别燃烧时,需要氧气的量相等的是
A. 乙烯、乙醇 B. 乙烯、乙烷 C. 丙烷、丙烯 D. 甲烷、甲醇
难度: 简单查看答案及解析
-
下列图示中关于铜电极的连接错误的是
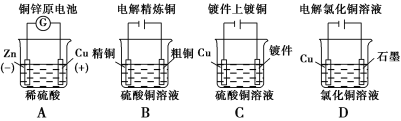
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
分子式为C4H8Cl2的有机物共有(不含立体异构)
A. 7种 B. 8种 C. 9种 D. 10种
难度: 简单查看答案及解析
-
下列说法和应用与盐的水解有关的是
①配制硫酸亚铁溶液时加入少量硫酸 ②铝盐和铁盐可作净水剂
③MgCl2溶液蒸干后灼烧得到MgO ④实验室盛放Na2CO3溶液的试剂瓶不能用磨口玻璃塞
A. ①②③ B. ②③④ C. ①④ D. ①②③④
难度: 中等查看答案及解析
-
常温时,pH=14和pH=10的两种NaOH溶液等体积混合,所得溶液中c(H+)约为
A. pH>7 B. pH=7
C. pH<7 D. 无法确定
难度: 简单查看答案及解析
-
某烯烃与H2加成后的产物的结构简式如下,则该烯烃可能有

A. 1种 B. 2种 C. 3种 D. 4种
难度: 简单查看答案及解析
-
下列有机物的命名正确的是
A. 2-甲基-4-乙基戊烷 B. 4-甲基-2-戊烯
C. 二氯丙烷 D. 2,2-二甲基-3-戊炔
难度: 简单查看答案及解析
-
下列关于有机化合物的叙述不正确的是
A. 丙烷跟甲烷一样能与氯气发生取代反应
B. 1mol乙酸与1mol乙醇在一定条件下发生酯化反应,可生成1 mol乙酸乙酯
C. CH2Cl2只有一种空间结构,说明甲烷是正四面体结构而不是平面正方形结构
D. 溴水既可鉴别乙烷与乙烯,又可除去乙烷中的乙烯
难度: 中等查看答案及解析
-
两种气态烃组成的混合气体0.1mol,完全燃烧得0.15 molCO2和3.6 g H2O,下列关于该混合气体的说法正确的是
A. 一定有乙烯 B. 一定没有乙烯 C. 一定有乙烷 D. 一定有甲烷
难度: 困难查看答案及解析
-
下列实验现象或结论不正确的是
实验操作
现象
结论
A
食醋浸泡水垢
产生无色气体
乙酸的酸性比碳酸强
B
乙醇与橙色酸性重铬酸钾溶液混合
橙色溶液变为绿色
乙醇具有氧化性
C
向试管中加入苯,再加入酸性高锰酸钾溶液,振荡
分层,下层紫红色
苯与高锰酸钾溶液不反应
D
甲烷通入氢氧化钠溶液中
无明显变化
甲烷的化学性质稳定
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列叙述正确的是
A. 46g乙醇存在的共价键总数为7NA
B. 常温常压下,28 g C2H4和CO的混合气体中含碳原子的数目为1.5NA
C. 4g丙炔中共用电子对数为0.8NA
D. 标准状况下,11.2 L苯中含有的碳氢键数为3NA
难度: 中等查看答案及解析
-
一种由甲醇(CH3OH)和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。下列说法不正确的是
A. 放电时CH3OH参与负极反应为:CH3OH-6e-+6OH-=CO2+5H2O
B. 放电时每消耗1molCH3OH转移6 mol电子
C. 充电时阳极的电极反应为:4OH--4e- = O2+2H2O
D. 充电时电解质溶液的pH逐渐增大
难度: 中等查看答案及解析
-
pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积的关系如图,下列说法正确的是
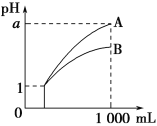
①若a<4,则A、B都是弱酸
②稀释后,A酸溶液的酸性比B酸溶液强
③若a=4,则A是强酸,B是弱酸
④A、B两种酸溶液的物质的量浓度一定相等
A. ①④ B. ②③ C. ①③ D. ②④
难度: 中等查看答案及解析
-
向CH3COONa稀溶液中分别加入少量下列物质(忽略温度与体积变化),可以使
的比值减小的是
A. KOH固体 B. 冰醋酸 C. CH3COONa固体 D. NaHSO4固体
难度: 中等查看答案及解析
-
的物质的量浓度相等的下列溶液:①(NH4)2SO4 ② (NH4)2Fe(SO4)2 ③(NH4)2CO3,溶质的物质的量浓度由大到小的顺序为
A. ① > ② > ③ B. ③ > ① > ②
C. ③ > ② > ① D. ② > ① > ③
难度: 中等查看答案及解析
-
六苯乙烷为白色固体,其结构如图,下列有关说法正确的是
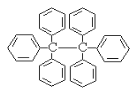
A. 它是一种饱和烃,易溶于有机溶剂中
B. 它的分子式为C38H30,只含有非极性键
C. 它的一氯代物只有三种
D. 在同一平面上的原子最多有14个
难度: 中等查看答案及解析
-
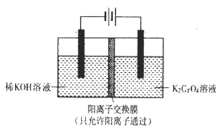
如图所示装置除去含有CN-、Cl-废水中的CN-时,控制溶液的pH值为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是
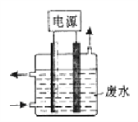
A. 用石墨作阳极,铁作阴极
B. 阳极的电极反应式为:Cl-+2OH--2e-= ClO-+H2O
C. 阴极附近碱性增强,阳极附近碱性减弱
D. 除去CN-的反应:5ClO-+2CN-+2H+ = N2↑+2CO2↑+5Cl-+H2O
难度: 困难查看答案及解析
-
不同温度T1、T2时,硫酸钡在水中的溶解平衡曲线如图所示,已知硫酸钡的溶度积随温度升高而增大,下列说法正确的是
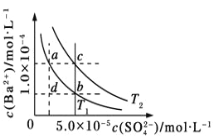
A. 升高温度,可以使溶液由b点变为d点
B. 加入BaCl2固体,可以使溶液由a点变为c点
C. c点表示在T1、T2温度下溶液中均有固体析出
D. T1温度下,恒温蒸发溶剂,可以使溶液由d点变为T1曲线上a、b之间某一点
难度: 中等查看答案及解析