-
物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当溶液的体积比为3∶2∶1时,三种溶液中Cl-的物质的量之比为
A. 1∶1∶1 B. 1∶2∶3
C. 3∶2∶1 D. 3∶4∶3
难度: 中等查看答案及解析
-
下列溶液中的Cl-浓度与150mL 1mol·L-1 MgCl2溶液中的Cl-浓度相等的是( )
A. 150mL 1mol·L-1 NaCl溶液 B. 75mL 2mol·L-1 CaCl2溶液
C. 150mL 2mol·L-1KCl溶液 D. 75mL 1mol·L-1 AlCl3溶液
难度: 中等查看答案及解析
-
“纳米材料”是粒子直径为1~ 100nm的材料,纳米碳就是其中的一种,若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后,会析出黑色沉淀
A. ①④⑥ B. ②③④ C. ②③⑤ D. ①③④⑥
难度: 中等查看答案及解析
-
下列说法中,正确的是( )
A. 化学的特征就是认识分子和制造分子
B. 在任何条件下,1mol任何气体的体积都约是22.4L
C. 在化学反应中,参加反应的各物质的质量比等于其物质的量之比
D. 俄国化学家门捷列夫提出原子学说,为近代化学的发展奠定了坚实的基础
难度: 简单查看答案及解析
-
物质的性质决定物质反应现象,下列关于钠与水反应的现象和钠的性质无关的是
A. 钠的熔点较低 B. 钠的密度小于水
C. 钠的硬度较小 D. 钠很活泼
难度: 中等查看答案及解析
-
下列关于氯气的叙述,正确的是 ( )
A. 氯气是一种无色,没有刺激性气味的气体
B. 氯气、氯水、液氯的成分相同
C. 氯气不能与碱发生反应
D. 氯气有毒,但可用来自来水的杀菌消毒
难度: 简单查看答案及解析
-
为了实现下列各变化,需加入还原剂的是( )
A. KClO3→O2 B. NH4+→NH3 C. Fe→FeCl3 D. CO2→CO
难度: 简单查看答案及解析
-
常温常压下,用等质量的CH4、CO2、O2、SO2四种气体分别吹出四个气球,其中气体为CH4的是( )。
A.
B.
C.
D.
难度: 简单查看答案及解析
-
相等物质的量的CO和CO2的下列比较中正确的是( )
①所含的分子数目之比为1:1 ②所含的O原子数目之比为1:2
③所含的原子总数目之比为2:3 ④所含的C原子数目之比为1:1
A. ①② B. ②③ C. ④ D. ①②③④
难度: 简单查看答案及解析
-
用如图表示的一些物质或概念间的从属关系中不正确的是
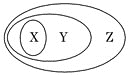
X
Y
Z
A
氧化物
化合物
纯净物
B
电解质
盐
化合物
C
胶体
分散系
混合物
D
碱性氧化物
金属氧化物
氧化物
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列关于氧化物的叙述正确的是( )
A. 金属氧化物不一定是碱性氧化物
B. 与水反应生成碱的氧化物为碱性氧化物
C. 非金属氧化物都是酸性氧化物
D. 不能跟酸反应的氧化物一定能跟碱反应
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是( )
A. 实验室用大理石和稀盐酸制取CO2:2H+ + CO32- = CO2↑+ H2O
B. 稀盐酸与氢氧化钡溶液反应: H++OH-=H2O
C. 硫酸镁溶液与氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓
D. 铁与稀硫酸溶液反应:2Fe + 6H+ =2Fe3++3H2↑
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数,下列说法错误的是( )
A. 2mol·L-1的氯化镁溶液中含氯离子数为4NA
B. 标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA
C. 32gO2和O3混合气体中含有的氧原子数为2NA
D. 化学反应中1mol金属镁变成镁离子时失去电子数目为2NA
难度: 中等查看答案及解析
-
在某无色透明的强酸性溶液中,能大量共存的离子组是( )
A. K+、Na+、Cu2+、SO42- B. Na+、Al3+、Cl-、NO3-
C. Na+、K+、HCO3-、Cl- D. K+、 SO42-、 Cl-、Ba2+
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A. 尽管BaSO4难溶于水,但它仍然是强电解质
B. 溶于水后能电离出氢离子的化合物都是酸
C. NaCl溶液在电流的作用下电离为钠离子和氯离子
D. 二氧化碳溶于水后能部分电离,所以二氧化碳是弱电解质
难度: 简单查看答案及解析
-
下表中评价合理的是( )
选项
化学反应及其离子方程式
评 价
A.
NaHSO4溶液与Ba(OH)2溶液反应至中性:
2H++SO42—+Ba2++2OH-===BaSO4↓+2H2O
正 确
B.
向碳酸镁中加入足量稀盐酸:
MgCO3+2H+===Mg2++CO2↑+H2O
错误,碳酸镁应拆成离子形式
C.
向沸水中滴加饱和的氯化铁溶液至液体变为红褐色:
Fe3++3H2O===Fe(OH)3↓+3H+
正 确
D.
NaOH溶液中通入少量CO2反应:OH-+CO2===HCO3—
正 确
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
关于反应CaH2+2H2O==Ca(OH)2+2H2↑,下列说法正确的是
A. H2O既不是氧化剂又不是还原剂 B. CaH2中H元素被还原
C. 此反应中氧化产物与还原产物的原子个数比为1:1 D. Ca(OH)2是氧化产物
难度: 中等查看答案及解析
-
下列各组物质中,X是主体物质,Y是少量杂质,Z是为除去杂质所要加入的试剂,其中所加试剂正确的是( )
A
B
C
D
X
FeCl3溶液
FeCl3溶液
Cu
Na2SO4溶液
Y
FeCl2
CuCl2
Fe
Na2CO3
Z
Fe
Fe
稀硫酸
BaCl2溶液
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列说法错误的是
A. 利用丁达尔效应可区分蛋白质溶液与葡萄糖溶液
B. 某物质经科学测定只含有一种元素,则可以断定该物质是一种纯净物
C. 用过滤法无法除去Fe(OH)3胶体中的FeCl3
D. 向豆浆中加入硫酸钙制豆腐,是利用了胶体的聚沉性质
难度: 中等查看答案及解析
-
向一定量的Fe、Fe2O3、FeO的混合物中加入200 mL 1 mol·L-1的盐酸,恰好使混合物完全反应溶解,放出4.48 mL(标准状况)气体。所得溶液中,加入KSCN溶液无红色出现,那么用足量的CO在高温下还原相同质量的此混合物,得到铁的质量为
A. 11.2 g B. 5.6 g C. 2.8 g D. 无法计算
难度: 中等查看答案及解析