-
2012年10月29日,超强飓风“桑迪”登陆美国东海岸,给人们的生命财产造成巨大损失。灾区人们的饮水必须用漂白粉等药品消毒后才能饮用,以防止传染病发生。
(1)试用化学方程式表示工业制取漂白粉的过程______________________________;
(2)已知浓盐酸和漂白粉中的成分之一次氯酸钙能发生如下反应:
Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能含有的杂质气体是(______)
① CO2 ② HCl ③ H2O ④ O2
A.①②③ B.②③④ C.②③ D.①④
(3)若用KMnO4氧化盐酸。其反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
该反应中,氧化剂是____,1 mol氧化剂在反应中_______(填“得到”或“失去”)______mol电子。当有1mol KMnO4恰好和盐酸全部完全反应,反应后溶液的体积为2L,则所得溶液中Cl—的物质的量浓度为_______,此时产生的Cl 2在标准状况下的体积为_______,被氧化的HCl的物质的量为________。
高一化学综合题中等难度题查看答案及解析
-
2012年10月29日,超强飓风“桑迪”登陆美国东海岸,给人们的生命财产造成巨大损失。灾区人们的饮水必须用漂白粉等药品消毒后才能饮用,以防止传染病发生。
(1)试用化学方程式表示工业制取漂白粉的过程______________________________;
(2)若用KMnO4氧化盐酸。其反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,该反应中,氧化剂是____,1 mol氧化剂在反应中_______(填“得到”或“失去”)______mol电子。当有1mol KMnO4恰好和盐酸全部完全反应,反应后溶液的体积为2L,则所得溶液中Cl—的物质的量浓度为_______,此时产生的Cl 2在标准状况下的体积为_______,被氧化的HCl的物质的量为________。
高一化学填空题简单题查看答案及解析
-
北京时间3月11日13点46分,日本海域发生了里氏9.0级强震,不仅造成了巨大的人员财产损失更直接导致了福岛核电站的核泄漏事故,在全球引起了核恐慌,许多国家都已检测出来自福岛核泄漏的放射性131I,下列说法正确的是( )
A.碘是第四周期元素
B.131I2与127I2互为同素异形体
C.131I的中子数是78
D.碘元素的近似相对原子质量为131高一化学选择题中等难度题查看答案及解析
-
北京时间3月11日13点46分,日本海域发生了里氏9.0级强震,不仅造成了巨大的人员财产损失更直接导致了福岛核电站的核泄漏事故,在全球引起了核恐慌,许多国家都已检测出来自福岛核泄漏的放射性131I,下列说法正确的是
A.碘是第四周期元素 B. 131I2 与127I2互为同素异形体
C.131I的中子数是78 D.碘元素的近似相对原子质量为131
高一化学选择题中等难度题查看答案及解析
-
天津港“8·12”危化仓库爆炸,造成生命、财产重大损失,其爆炸品中有金属钠。运输金属钠的集装箱应贴有的警示标识是

高一化学选择题简单题查看答案及解析
-
2010年,我国接连发生多起煤矿爆炸事故,造成重大人员伤亡和财产损失。煤矿发生爆炸事故的元凶是煤矿坑道气中含有的甲烷。下列关于甲烷的叙述中错误的是
A.甲烷分子是一种呈正四面体型的、含极性共价键的分子
B.甲烷分子中两个氢原子被氯取代后,可形成两种不同结构的分子
C.甲烷是重要的化工原料,其分解产物可用于合成氨和橡胶工业
D.“抽”出坑道中的甲烷,既可用作清洁燃料,又可防止爆炸
高一化学选择题中等难度题查看答案及解析
-
2015年8月12日晚,天津塘沽滨海新区危险品仓库发生大爆炸,造成了巨大损失.此次涉事公司网站显示,该公司仓储业务的商品类别如下表所示:
物质类别
具体物质
物质类别
具体物质
压缩气体和液化气体
氩气、压缩天然气易燃固体、自然物品和遇湿易燃物品
硫磺、硝化纤维素、电石、硅钙合金、钠、钾
氧化剂和有机过氧化物
硝酸钾、硝酸钠、过氧乙酸
易燃液体
甲乙酮、乙酸乙酯
腐蚀品、杂类
甲酸、磷酸、甲基磺酸、烧碱、硫化碱
毒害品
氰化钠、甲苯二异氰酸酯
请用化学用语回答下列问题:
(1)压缩气体和液化气体中属于单质的是 ,天然气的主要成分是 ,按物质树状分类法,天然气属于 ;
(2)氧化剂和有机过氧化物中,硝酸钾、硝酸钠均属于 ;
A.硝酸盐 B.氧化物 C.钾盐 D.钠盐
(3)在毒害品中含有剧毒化学品氰化钠(NaCN).下列有关氰化钠的说法中错误的是 ;
A.NaCN易溶于水
B.NaCN中碳元素的化合价为+4
C.可用H2O2将NaCN还原为无毒物质
D.为防止中毒,须加强对地表水、排海口等位置水体中氰化物的排查监测
(4)写出易燃固体中金属钾与水反应的离子方程式: ;
(5)腐蚀品中烧碱的主要成份是 ,如在实验室中配制500mL浓度为0.2mol•L﹣1的烧碱溶液,需称量烧碱 g.需要的玻璃仪器.除了烧杯、玻璃棒外,还必须有 、 .
高一化学填空题中等难度题查看答案及解析
-
据统计,全球每90秒钟就有1吨钢铁被锈蚀,每年有1.3亿吨钢铁被腐蚀掉,造成巨大的经济损失。钢铁在潮湿的空气中发生腐蚀生成铁锈
,其反应的化学方程式为:
①2Fe+O2+2H2O = 2Fe(OH)2;
②4Fe(OH)2+O2+2H2O = 4Fe(OH)3;
③2Fe(OH)3 = Fe2O3+3H2O
上面三个反应中,属于非氧化还原反应的是( )
A.①② B.①③ C.①②③ D.③
高一化学选择题简单题查看答案及解析
-
天津港“8.12”特大火灾爆炸事故,造成了极其恶劣的社会影响。原因是化学危险 品随意堆放,管理人员安全意识淡漠,对人民的生命财产极不负责任。
下面是其中一部分危险品。请回答下列问题:
⑴ 写出过氧化氢的电子式
⑵ 上述危险品中,和水反应且符合下列条件的离子方程式
① 属于氧化还原反应
② 水既不做氧化剂也不做还原剂
⑶ 4000C时,硝酸铵会发生爆炸,生成氮气、二氧化氮和水蒸气,20g硝酸铵爆炸放出QkJ的热量,试写出该反应的热化学方程式
⑷ 写出酸性高锰酸钾溶液与过氧化氢化应的离子方程式
⑸ 氰化钠有剧毒,为防止扩散,消防队员和工作人员离场前都用双氧水消毒。氰化钠和双氧水反应生成一种酸式盐和一种有刺激性气味的气体,反应的离子方程式是 ;调查查明现
场有700吨的氰化钠,如果用密度为1.2g/mL质量分数为17%的双氧水进行消毒,最少需要这种双氧水_______L。
高一化学填空题困难题查看答案及解析
-
天津港“8.12”特大火灾爆炸事故,造成了极其恶劣的社会影响。原因是化学危险 品随意堆放,管理人员安全意识淡漠,对人民的生命财产极不负责任。
下面是其中一部分危险品。请回答下列问题:
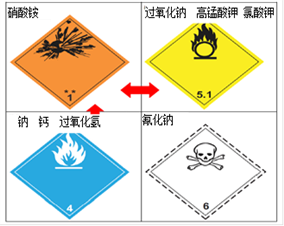
⑴ 写出过氧化氢的电子式 ______________;
⑵ 上述危险品中,和水反应且符合下列条件的离子方程式______________;
① 属于氧化还原反应 ② 水既不做氧化剂也不做还原剂;
⑶ 400℃时,硝酸铵会发生爆炸,生成氮气、二氧化氮和水蒸气,20g硝酸铵爆炸放出QkJ的热量,试写出该反应的热化学方程式______________;
⑷ 写出酸性高锰酸钾溶液与过氧化氢化应的离子方程式______________;
⑸ 氰化钠有剧毒,为防止扩散,消防队员和工作人员离场前都用双氧水消毒。氰化钠和双氧水反应生成一种酸式盐和一种有刺激性气味的气体,反应的离子方程式是______________;调查查明现场有700吨的氰化钠,如果用密度为1.2g/mL质量分数为17%的双氧水进行消毒,最少需要这种双氧水_______L。
高一化学填空题中等难度题查看答案及解析