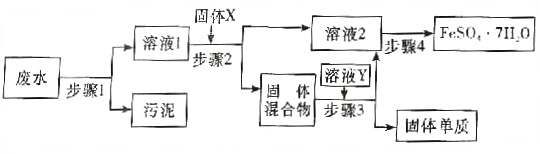
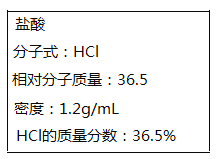
-
化学与生活、社会发展息息相关,下列有关说法不正确的是
A. “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
B. “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化
C. 古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金
D. “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
难度: 中等查看答案及解析
-
明代《本草纲目》收载药物1892种,其中“烧酒”条目下写道:“自元时始创其法,用浓酒和精人甑,蒸令气上……其清如水,球极浓烈,盖酒露也。”这里所用的“法”是指
A. 萃取 B. 过滤 C. 蒸馏 D. 升华
难度: 简单查看答案及解析
-
下列各物质含少量杂质,除去这些杂质应选用的试剂或操作方法正确的是
序号
物质
杂质
除杂应选用的试剂或操作方法
①
KNO3溶液
KOH
加入FeCl3溶液,并过滤
②
FeSO4溶液
CuSO4
加入过量铁粉,并过滤
③
H2
CO2
通过盛NaOH溶液的洗气瓶
④
NaNO3固体
CaCO3
溶解,过滤、蒸发
A. ②④ B. ②③④ C. ①③④ D. ①②③④
难度: 简单查看答案及解析
-
下列各种混合物中,能用分液漏斗进行分离的是
A. 酒精和水 B. 水和四氯化碳 C. 碘和四氯化碳 D. 汽油和植物油
难度: 简单查看答案及解析
-
进行化学实验必须注意安全,下列说法中正确的是
A. 不慎碰倒酒精灯,洒出的酒精在桌上燃烧时,应立即用湿抹布扑盖
B. 氢气还原氧化铜时,先加热再通氢气
C. 不慎将浓硫酸溅到皮肤上,立即用大量水冲洗,再涂3%--5%的氢氧化钠溶液
D. 稀释浓硫酸的操作为将水加入浓硫酸中,并用玻璃棒不断搅拌
难度: 中等查看答案及解析
-
下列两种气体分子数一定相同的是
A. 等温等体积的O2与N2 B. 质量相等密度不等的N2O与CO2
C. 等压等体积的CO2与N2 D. 体积相等密度相等的CO2与CO
难度: 简单查看答案及解析
-
如图所示,相同状况下,分别用氯化氢和四种混合气体吹出体积相等的五个气球。A、B、C、D四个气球中所含原子数与氯化氢气球中所含原子数一定相等的是
A.
B.
C.
D.
难度: 中等查看答案及解析
-
分类法在化学学科的发展中起到了非常重要的作用,下列分类标准合理的是
A. 根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
B. 依据分子组成中含有氢原子的数目,将酸分为一元酸、二元酸等
C. 根据水溶液是否能够导电,将物质分为电解质和非电解质
D. 依据组成元素的种类,将纯净物分为单质和化合物
难度: 简单查看答案及解析
-
下列说法正确的是
A. 阿伏伽德罗常数个硫酸分子里含有4mol O
B. 摩尔是国际单位制中的七个基本物理量之一
C. CH4的摩尔质量为16g
D. 1mol任何物质都含有6.02×1023个原子
难度: 简单查看答案及解析
-
下列溶液中的Cl- 浓度与50mL 1mol/L AlCl3溶液中的Cl- 浓度相等的是
A. 150mL 1mol/L NaCl溶液 B. 75mL 2mol/L CaCl2溶液
C. 150mL 2mol/L MgCl2溶液 D. 75mL 3mol/L KCl溶液
难度: 简单查看答案及解析
-
下列叙述与胶体知识无关的是
A. 向氯化铁溶液中加入过量氢氧化钠溶液会看到红褐色沉淀
B. 江河入海口常有三角洲形成
C. 在电影院看电影,会看到从放映室到银幕的光柱
D. “卤水点豆腐”
难度: 简单查看答案及解析
-
下列物质属于电解质的是
A. SO3 B. Al2O3固体 C. 氨水 D. NaCl溶液
难度: 简单查看答案及解析
-
在无色透明的酸性溶液中,能大量共存的离子组是
A. K+、Fe2+、SO42-、NO3- B. OH-、Cl-、Na+、Cu2+
C. NH4+、NO3-、Al3+、K+ D. S2-、SO42-、Na+、Ag+
难度: 简单查看答案及解析
-
下列关于物质分类的正确组合是
物质分类
碱
酸
盐
碱性氧化物
酸性氧化物
A
Na2SO3
H2SO4
NaHCO3
SO2
CO2
B
NaOH
HCl
NaCl
Na2O
CO
C
KOH
HNO3
CaCO3
CaO
SO3
D
NaOH
CH3COOH
CaF2
CO2
SO2
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是
A. 氧化铁与盐酸反应:FeO+2H+=Fe2++H2O
B. 碳酸钙与盐酸反应:CO32-+2H+=CO2↑+H2O
C. 钠与水反应:2Na+2H2O=2Na++2OH-+H2↑
D. 氢氧化钡溶液与稀硫酸反应:Ba2++SO42—=BaSO4↓
难度: 简单查看答案及解析
-
常温下在溶液中可发生如下两个离子反应:Sn2++2Fe3+===2Fe2++Sn4+, Ce4++Fe2+=Fe3++Ce3+。由此可以确定Fe3+、Ce4+、Sn4+三种离子的氧化性由强到弱的顺序是
A. Ce4+、Fe3+、Sn4+ B. Sn2+、Fe2+、Ce3+
C. Sn4+、Ce3+、Fe2+ D. Fe2+、Sn2+、Ce3+
难度: 中等查看答案及解析
-
将0.195g锌粉加入到20.0mL的0.100mol/L的MO2+溶液中,恰好完全反应,则还原产物可能是
A. M2+ B. M C. MO2+ D. M3+
难度: 中等查看答案及解析
-
化学实验中若使某步中的有害产物作为另一步的反应物,形成一个循环,则可不再向环境排放该种有害物质。在如图所示有编号的反应中,属于氧化还原反应的有
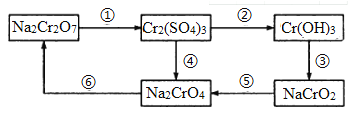
A. 6个 B. 5个 C. 4个 D. 3个
难度: 中等查看答案及解析
-
中科大发现了人工合成金刚石的新方法,化学原理为:Na+CO2 →C(金刚石)+C(石墨)+Na2CO3 (未配平,一定条件下),这种合成具有深远的意义。下列说法不正确的是
A. 该反应中,钠作还原剂,二氧化碳作氧化剂
B. 还原性Na大于C
C. 该反应中Na2CO3是氧化产物
D. 每生成1mol Na2CO3时,共转移4mol电子
难度: 中等查看答案及解析
-
用NA代表阿伏加德罗常数的值,下列说法正确的是
A. 0.5 mol镁粒与足量盐酸反应产生11.2 L H2
B. 1L0.5mol/LFeCl3溶液完全转化可制得0.5NA个Fe(OH)3胶粒
C. 0.5 mol/L的FeCl2溶液中含有Cl﹣个数为NA
D. 25℃、101Pa时,16g O2和O3混合气体中含有的原子数为NA
难度: 中等查看答案及解析
-
取50mL0.3mol/L的硫酸注入250mL容量瓶中,加水稀释至刻度线,则该溶液中的H+的物质的量浓度为
A. 0.06mol/L B. 0.12 mol/L C. 0.24mol/L D. 0.03mol/L
难度: 简单查看答案及解析
-
氧化还原反应与四个基本反应类型的关系如下图所示,则下列化学反应属于阴影部分的是( )
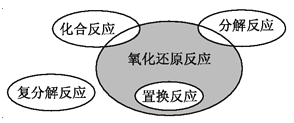
A. Cl2+2KBr=Br2+2KCl
B. 2NaHCO3
Na2CO3+H2O+CO2↑
C. 4Fe(OH)2+O2+2H2O=4Fe(OH)3
D. 2Na2O2+2CO2=2Na2CO3+O2(提示:Na2O2中的氧为-1价)
难度: 中等查看答案及解析
-
将250mL含有BaCl2和KCl的混合溶液分成2等份,一份加入含amol硫酸钠的溶液,恰好使钡离子完全沉淀;另一份加入含bmol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子的浓度为
A. (b-2a) mol/L B. 8(2a-b) mol/L
C. 8(b-2a) mol/L D. 4(b-2a) mol/L
难度: 中等查看答案及解析
-
一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分。当左边充入1molN2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置(左、右两侧温度相同)。右侧CO2与CO分子数之比为
A. 1:3 B. 3:1 C. 1:2 D. 2:1
难度: 困难查看答案及解析