-
下列物质中,含有氧分子的是
A. O2 B. MnO2 C. CO2 D. H2O2
难度: 简单查看答案及解析
-
中华民族的发明创造为人类文明进步作出了巨大贡献。下列古代发明及应用中,不涉及化学变化的是
A.
 陶瓷烧制 B.
陶瓷烧制 B.  玉石雕印
玉石雕印C.
 粮食酿醋 D.
粮食酿醋 D.  火药爆炸
火药爆炸难度: 简单查看答案及解析
-
空气中体积分数约为78%的气体是
A. 二氧化碳 B. 氧气 C. 氮气 D. 水蒸气
难度: 简单查看答案及解析
-
青团是清明时节的传统食品,下列制作青团的部分原料中,富含维生素的是
A. 糯米粉 B. 植物油 C. 蔗糖 D. 绿色蔬菜汁
难度: 简单查看答案及解析
-
下列人体所必需的元素中,缺乏会引起骨质疏松的是
A. 铁 B. 钙 C. 锌 D. 碘
难度: 简单查看答案及解析
-
下列关于物质用途的描述中,不正确的是
A. 氧气用于气焊 B. 二氧化碳作燃料
C. 浓硫酸作干燥剂 D. 碳酸氢钠用于治疗胃酸过多
难度: 简单查看答案及解析
-
下列实验操作中,正确的是
A.
倾倒液体 B.
称量氢氧化钠
C.
测定溶液的pH D.
稀释浓硫酸
难度: 简单查看答案及解析
-
下列反应中,属于复分解反应的是
A. CH4 + 2O2
CO2 + 2H2O B. Na2CO3 + Ca(OH)2 === CaCO3↓ + 2NaOH
C. 2H2O
2H2↑+ O2↑ D. CO2 + 2 NaOH === Na2CO3 + H2O
难度: 中等查看答案及解析
-
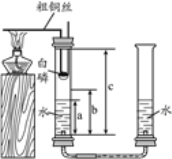
下列关于电解水实验的说法中,正确的是

A. 管a中的气体为H2
B. 与管a相连的是电源的正极
C. 管a与管b中气体质量比为2:1
D. 该实验可说明水由H2和O2组成
难度: 中等查看答案及解析
-
下列对于灭火原理的分析中,正确的是
A. 砍掉大火蔓延路线前的树木 —— 隔离可燃物
B. 用水扑灭燃着的木材 —— 降低木材的着火点
C. 用锅盖盖灭油锅内的火 —— 降低油温
D. 用扇子扇灭烛火 —— 隔绝空气
难度: 简单查看答案及解析
-
M、N两种固体的溶解度曲线如图甲。40℃时,将等质量的M、N两种固体,分别加入到盛有100g水的烧杯中,充分搅拌后,现象如图乙,降温到20℃时,现象如图丙。将图丙烧杯a中的固体移除后,所得溶液的质量为

A. 100 g B. 110 g C. 120 g D. 130 g
难度: 中等查看答案及解析
-
下列说法正确的是

A. 烧杯a中加入的固体为N
B. 40℃时烧杯a中溶液一定是饱和溶液
C. 40℃时烧杯b和20℃时烧杯b中溶质质量不相等
D. 40℃时烧杯a和20℃烧杯b中溶液的溶质质量分数相等
难度: 中等查看答案及解析