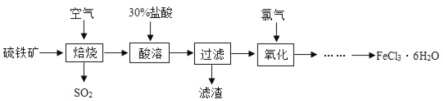
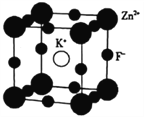
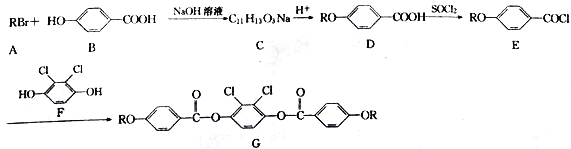
-
下列实验过程可以达到实验目的的是
编号
实验目的
实验过程
A
配制0.2mol·L-1的硫酸
量取5mL10.0mol/L硫酸,转移至250mL的容量瓶中定容
B
探究亚硫酸钠的还原性
向盛有2mL亚硫酸钠溶液的试管中滴加浓盐酸,观察颜色变化
C
制取并纯化氯气
向二氧化锰中加入浓盐酸并加热,将产生的气体依次通过饱和碳酸氢钠溶液和浓硫酸
D
探究催化剂对反应速率的影响
向试管中同时加入2mL5%H2O2溶液,向其中一个试管中滴入1滴氯化铁溶液,观察实验现象
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
化学与科学技术的发展密切相关,下列有关说法正确的是
A. 柴油汽车中尿素溶液进入尾气系统,是为了处理尾气
B. “可燃冰”中的甲烷对温室效应的影响几乎为零
C. 古代用明矾除去铜器表面的铜绿,利用了明矾溶液显碱性的特性
D. 铌酸锂( LiNbO3)材料将用于量子通信,41Nb位于第VA族
难度: 简单查看答案及解析
-
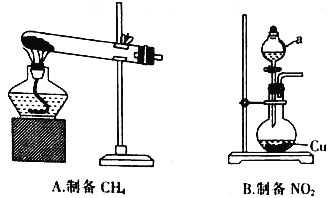
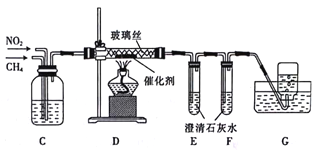
1,2-二溴乙烷(沸点为131℃),可溶于CCl4,某同学在实验室将乙烯通入溴的四氯化碳溶液中,在生成和纯化1,2-二溴乙烷的实验过程中,下列操作未涉及的是
A.
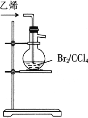 B.
B. 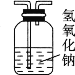 C.
C. 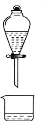 D.
D. 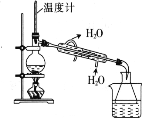
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的数值。下列叙述正确的是
A. 64gCaC2固体中所含的阴、阳离子总数为3NA
B. 7.8gNa2O2与足量水反应时,转移的电子数为0.2NA
C. 0.5 mol Mg在空气中完全燃烧生成MgO和Mg3N2时,转移的电子数为NA
D. 密闭容器中充入1molH2与1mol I2反应制备HI时,生成H-I键的数目为2NA
难度: 中等查看答案及解析
-
短周期主族元素X、Y、Z、M、W的原子序数依次增大,X元素的某种原子不含中子,X与M同主族,W的单质为黄色,W和Z同主族,5种元素最外层电子总数为19。下列说法正确的是
A. 元素周期表中,短周期主族元素共有18种
B. X、Y、Z、W均可以和M形成离子化合物
C. 以上5种元素形成的化合物中,从阳离子的分类角度来看,只能形成一类盐
D. 原子半径和离子半径均满足:Z<M
难度: 中等查看答案及解析
-
燃烧产生的尾气中含有一定量的NO。科学家们设计了一种间接电处理法除去其中NO的装置,如下图所示,它可以将NO转化为NH4+。下列说法正确的是
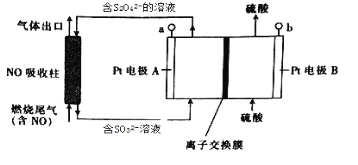
A. a连接电源的正极
B. Pt电极B上发生的电极反应为2H2O-4eˉ=O2↑+4H+
C. 当NO吸收柱中产生1mol SO32ˉ时,理论上处理的NO气体的体积为8.96L(标准状况)
D. 图中的离子交换膜应为阴离子交换膜
难度: 中等查看答案及解析
-
25℃时,改变醋酸溶液的pH[溶液中c(CH3COOˉ)与c(CH3COOH)之和始终为0.1mol·Lˉ1],溶液中H+、OHˉ、CH3COOˉ及CH3COOH浓度的对数值(lgc)与pH关系如图所示。
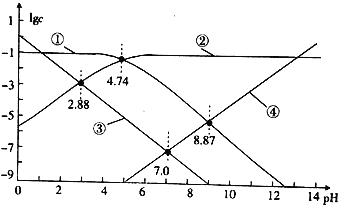
下列说法错误的是
A. lgK(CH3COOH)=-9.26
B. 图中①表示 CH3COOH浓度的对数值与pH的关系曲线
C. 0.1mol·Lˉ1CH3COOH溶液的pH约为2.88
D. 0.1mol·Lˉ1CH3 COONa溶液的pH约为8.87
难度: 困难查看答案及解析