-
下列情况会对人体健康造成较大危害的是
A.自来水中通入少量Cl2进行消毒杀菌
B.用SO2漂白食品
C.用食醋清洗热水瓶胆内壁附着的水垢
D.用小苏打(NaHCO3)发酵面团制作馒头
难度: 简单查看答案及解析
-
现有两瓶溶液,新制饱和氯水和亚硫酸,下列方法或试剂(必要时可加热)能用于鉴别它们的是:①观察颜色;②石蕊试剂;③品红溶液
A.①②③ B.只有①③ C.只有②③ D.只有①
难度: 中等查看答案及解析
-
下列各组离子一定能大量共存的是
A.在含有大量AlO2-的溶液中:NH4+、 Na+、Cl-、H+
B.在强碱溶液中:Na+、K+、CO32-、NO3-
C.常温下,在pH=12的溶液中:Mg2+、Na+、SO42-、Cl-
D.在水电离出的c(H+)=1×10-13mol·L-1的溶液中:K+、I-、Cl-、NO3-
难度: 中等查看答案及解析
-
NA代表阿伏加德罗常数的值,下列叙述正确的是
A.60g丙醇中存在的共价键总数为10NA
B.1L 0.1 mol·L-1的NaHCO3溶液中HCO3-和CO32-的离子数之和为0.1NA
C.钠在空气中燃烧可生成多种氧化物,23g钠充分燃烧时转移电子数为1 NA
D.235g核素
发生裂变反应:
+
+
+10
,净产生的中子(
)数为10 NA
难度: 中等查看答案及解析
-
下列离子方程式正确的是
A.向NaHSO4溶液中滴加过量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
B.用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32-
C.向FeCl3溶液中加入铜片:Fe3++Cu=Fe2++Cu2+
D.向碳酸氢钠溶液中加入氢氧化钠:HCO3-+ OH-==CO2↑+H2O
难度: 中等查看答案及解析
-
下列有关说法正确的是
A.丙烯的结构简式为CH2CHCH3
B.2,2-二甲基丙烷的一氯代物有2种
C.分子式为CH4O和C2H6O的物质一定互为同系物
D.键线式为
的有机物的分子式为C8H8
难度: 中等查看答案及解析
-
下列有关实验的叙述正确的是
A.实验室用浓溴水与苯在Fe粉催化下制溴苯
B.欲检验CH2=CHCHO中的碳碳双键,应向其中先加入足量的新制银氨溶液,水浴加热,待出现银镜后,再加入适量的溴水,若溴水褪色,即可验证
C.实验室制备乙酸乙酯时,向试管中加入试剂的顺序为:乙醇、浓硫酸、冰醋酸
D.将CH3CH2Br与NaOH溶液共热后,向其中加入AgNO3溶液,若产生沉淀,即可证明CH3CH2Br中含有溴元素
难度: 中等查看答案及解析
-
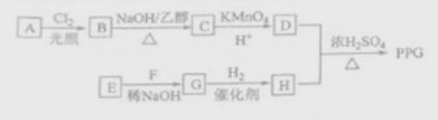
由2-氯丙烷制取1,2-丙二醇时,需要经过下列哪几步反应
A.加成 → 消去 → 取代 B.消去 → 加成 → 取代
C.取代 → 消去 → 加成 D.消去 → 加成 → 消去
难度: 中等查看答案及解析
-
等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出氢气最多的是
A.2 mol·L-1 H2SO4溶液 B.18 mol·L-1 H2SO4溶液
C.6 mol·L-1 KOH溶液 D.3 mol·L-1 HNO3溶液
难度: 中等查看答案及解析
-
下列有机物中,既能发生消去反应,又能发生酯化反应,还能发生催化氧化,且催化氧化产物能发生银镜反应的是
A.CH3OH B.CH3CH(OH)COOH
C.(CH3)2C(OH)CH2CH3 D.HOCH2CH2COOH
难度: 中等查看答案及解析
-
下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是

A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制 MnCl2·4H2O
难度: 中等查看答案及解析
-
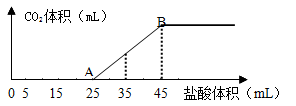
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是
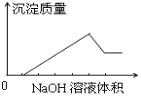
A.Mg2+、Al3+、Fe2+ B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+ D.只有Mg2+、Al3+
难度: 困难查看答案及解析
-
下述实验能达到预期目的的是
编号
实验内容
实验目的
A
将SO2通入溴水中
验证SO2具有漂白性
B
在滴有酚酞的Na2CO3溶液中,加入BaC12溶液后红色褪去
验证Na2CO3溶液中存在水解平衡
C
淀粉溶液和稀H2SO4混合加热,后加新制的Cu(OH)2悬浊液加热至沸腾
检验淀粉水解产物有还原性
D
将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中
检验气体中含有乙烯
难度: 中等查看答案及解析
-
分枝酸可用于生化研究,其结构简式如图。下列关于分枝酸的叙述正确的是

A.分子中含有2种官能团
B.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
C.1mol分枝酸最多可与3molNaOH发生中和反应
D.可与乙醇、乙酸反应,且反应类型相同
难度: 中等查看答案及解析
-
取m g的某物质在氧气中完全燃烧,所得产物跟足量的Na2O2固体完全反应。若Na2O2固体的质量增加m g,则下列物质中不能满足上述结果的是
A.CH3COOH B.H2 C.HCOOH D.CO
难度: 中等查看答案及解析
-
取x g铜和镁的合金完全溶于浓硝酸,若反应中硝酸被还原只产生8960 mL NO2气体和672 mL N2O4气体(都已折算成标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为17.02 g,则x等于
A.8.64 g B.9.00 g C.9.20 g D.9.44 g
难度: 困难查看答案及解析