-
自然界中存在的碘的稳定性核素是碘﹣127(
I).日本福岛第一核电站事故释放出的放射性物质中,含有人工放射性核素碘﹣131(
I).碘﹣131 (
I) 一旦被人体吸入,就可能会引发甲状腺疾病.对于这两种核素的下列说法正确的是( )
A.
I是一种新元素 B.
I的摩尔质量为131g
C.
I和
I互为同位素 D.
I中子数与质子数之差为74
难度: 简单查看答案及解析
-
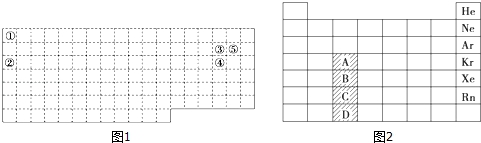
下列物质中,含有Cl-的是( )
①盐酸 ②氯化钠溶液 ③氯化钠固体 ④次氯酸 ⑤氯化氢气体 ⑥氯仿
A、①②⑥ B、①②③ C、③④⑥ D、②④⑤
难度: 中等查看答案及解析
-
下列各组中的两种物质发生变化时,所克服的作用力属于同种类型的是( )
A
、二氧化硅和氯化镁熔化 B、碘和氯化铵受热变成气体
C、水和干冰的气化 D、氯化钠和氯化氢溶于水
难度: 中等查看答案及解析
-
下列物质中属于共价化合物的是( )
A.Cl2 B.NH4Cl C.HCl D.NaOH
难度: 中等查看答案及解析
-
a、b、c、d均为短周期元素,它们在周期表中的位置如图所示.下列说法正确的是( )
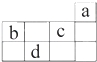
A.a原子的最外电子层上有8个电子 B.c的最高价氧化物对应水化物为强酸
C.d的原子半径比c的原子半径大 D.b的气态氢化物比c的气态氢化物稳定
难度: 中等查看答案及解析
-
下列结论错误的是( )
①微粒半径:K+>Al3+>S2﹣>Cl﹣
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2﹣>Cl﹣>Br﹣>I﹣
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO4
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K
⑧沸点:H2Se>H2S>H2O.
A.①⑤ B.①③⑤⑧ C.②④⑥⑦ D.②④⑥
难度: 中等查看答案及解析
-
下列关于指定粒子构成的几种描述中不正确的是( )
A.37Cl与39K具有相同的中子数
B.第114号元素的一种核素
X与82Pb具有相同的最外层电子数
C.O22﹣和S2﹣具有相同的质子数和电子数
D.H3O+与OH﹣具有相同的质子数和电子数
难度: 中等查看答案及解析
-
下列说法中正确的是( )
A.离子化合物中可以含有共价键,但共价化合物中一定不含离子键
B.含有共价键的物质一定是共价化合物
C.HCl溶于水只需克服分子间作用力
D.干冰升华时,分子内共价键会发生断裂
难度: 中等查看答案及解析
-
用NA代表阿伏加德罗常数的值,下列有关说法正确的是 ( )
A.3molNO2与足量H2O反应,转移的电子数为NA
B.常温常压下,22.4L氦气含有NA个氦原子
C.锂在氧气中燃烧,1molO2作氧化剂时得到的电子数为2NA
D.常温常压下,17克NH3中含有共价键的数目为3NA
难度: 中等查看答案及解析
-
下列有关粒子的表示方法正确的是( )
A.氨气分子的电子式:
B.硫原子结构示意图:
C.氯气分子的结构式:Cl﹣Cl D.H2O的电子式:
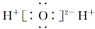
难度: 中等查看答案及解析
-
丁烷广泛应用于家用液化石油气中,也用于打火机中作燃料。下列叙述不正确的是( )
A.在常温下,丁烷是气体
B.丁烷与甲烷互为同系物
C.丁烷有正丁烷和异丁烷两种同分异构体
D.戊烷进行一氯取代后生成两种沸点不同的产物
难度: 中等查看答案及解析
-
在一定条件下,
和I-发生反应的离子方程式为:
+6I-+6H+=R-+3I2+3H2O(R为主族元素)则:R元素最外层电子数为( )
A.7 B. 5 C.3 D.4
难度: 中等查看答案及解析
-
某元素的一种同位素原子
,它与3H原子组成HmX分子,在agHmX中所含中子的物质的量是( )
A.
(A-Z+2m)mol B.
(A+2m)mol
C.
(A-Z+3m)mol D.
(A-Z+2m)mol
难度: 中等查看答案及解析
-
等质量的下列物质燃烧,消耗氧气量最多的是( )
A.CH4 B.C2H6 C.C3H6 D.C3H8
难度: 中等查看答案及解析
-
下列有关化学键的叙述,正确的是( )
A.硫酸氢钠溶于水既有离子键被破坏又有共价键被破坏
B.单质分子中均含共价键
C.HF与HBr相比,分子内共价键更强,所以HF沸点更高
D.由不同元素组成的多原子分子里,只存在极性键
难度: 中等查看答案及解析
-
下列分子中所有原子都满足最外层为8电子稳定结构的是( )
A.H2O2 B.CO2 C.SF6 D.BeCl2
难度: 中等查看答案及解析
-
如下图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
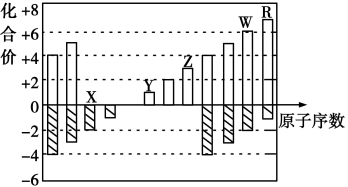
A.离子半径:Y > Z >X
B.气态氢化物的稳定性:R<W
C.WX3和水反应形成的化合物是离子化合物
D.Y和Z两者最高价氧化物对应的水化物能相互反应
难度: 中等查看答案及解析
-
A、B是元素周期表中同周期的两种主族元素,它们可以形成离子化合物AmBn,且离子均达到稀有气体原子的电子层结构。若A的原子序数为a,则B的原子序数可能是( )
A.a+8+m-n B.a+18-m+n C.a+32-m-n D.a+24-m-n
难度: 中等查看答案及解析
-
下列物质中互为同分异构体的是( )
A.13C 与 14C B.CH3CH2OH与CH3COOH
C.甲烷与丙烷 D.CH3CH2CH2CH3 与 CH3CH(CH3)2
难度: 中等查看答案及解析
-
aAn+,bB(n+1)+,cCn- ,dD(n+1)-离子具有相同的电子层结构的短周期元素形成的简单离子,下列叙述正确的是( )
A.原子半径C>D>A>B B.原子序数:b>a>c>d
C.离子半径Cn-> D(n+1)->An+>B(n+1)+ D.单质还原性A>B>C>D
难度: 中等查看答案及解析
-
两种气态烷烃的混合物,在标准状况下其密度为1.16g/L,则关于此混合物的组成的说法正确 的是( )
A.一定有甲烷 B.一定有乙烷
C.可能是甲烷和正戊烷的混合物 D.可能是乙烷和丙烷的混合物
难度: 中等查看答案及解析
-
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表; J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的元素。
J
R
下列说法错误的是( )
A .J的单质一定能导电
B.J、R形成的化合物JR2中J与R原子间是极性共价键
C.R、T两元素的气态氢化物中,T的气态氢化物更稳定
D.四种元素中T的最高价氧化物的水化物酸性最强
难度: 中等查看答案及解析
-
A、B、C、D、E五种短周期元素中,A、B、C位于同一周期相邻位置,A、C的原子序数之 比为3:4,A、B、C分别与D形成化合物分子中都含有10个电子,E的原子结构中从内到外各电子层的电数之比为1:4:1.下列叙述中,正确的是( )
A.A、B、C分别与D形成的化合物的热稳定性依次减弱
B.B、D原子构成的一中分子B2D4只含有极性共价单键
C.B、C、D三种元素可以形成酸、碱或者盐三种物质
D.C的离子半径小于E的离子半径
难度: 中等查看答案及解析
-
氢的同位素1H、2H、3H与氧的同位素16O、18O相互结合为水,可得到水分子的种数为
A.6 B.9 C.12 D.18
难度: 中等查看答案及解析