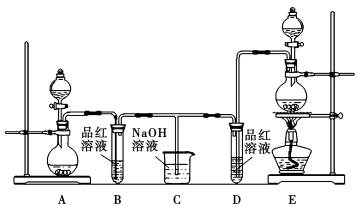
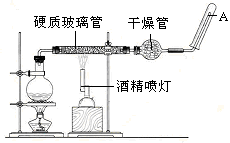
-
可用来干燥氨气的有( )
A.浓硫酸 B.碱石灰
C.氯化钙 D.五氧化二磷
难度: 简单查看答案及解析
-
检验氨气可选用( )
A.湿润的蓝色石蕊试纸 B.干燥的红色石蕊试纸
C.干燥的蓝色石蕊试纸 D.湿润的红色石蕊试纸
难度: 简单查看答案及解析
-
下列试剂保存或盛放方法正确的是( )
A.浓硝酸盛放在铜质器皿中
B.稀硝酸盛放在铁质器皿中
C.NaOH溶液保存在带橡胶塞的试剂瓶中
D.NaOH溶液保存在带玻璃塞的试剂瓶中
难度: 简单查看答案及解析
-
下列有关金属的说法正确的是( )
A.生铁与钢的区别在于生铁含碳杂质,而钢不含
B.铜在自然界中的含量高,所以铜是人类最早使用的金属
C.黑色金属材料包括铁、铬、锰及其化合物
D.金属一般都具有导电性、导热性、延展性
难度: 简单查看答案及解析
-
将下列各种单质投入或通入CuSO4溶液中,能产生铜单质的是( )
A.Fe B.Na C.H2 D.Ag
难度: 简单查看答案及解析
-
化学在生产和日常生活中有着重要的应用,下列说法不正确的是( )
A.氧化镁用作耐火材料
B.Na2O常用于潜水艇或呼吸面具的供氧剂
C.明矾溶于水形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
D.FeCl3溶液可用于刻制印刷铜电路板
难度: 简单查看答案及解析
-
下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),化学反应的产物并不改变的是( )
A.Na和O2 B.NaOH和CO2
C.Na2O2和CO2 D.木炭(C)和O2
难度: 简单查看答案及解析
-
有关合金的叙述正确的是( )
A.合金的导电性比成分金属强
B.合金的抗腐蚀性能都很好
C.合金的机械强度比各成分金属小
D.多数合金比成分金属熔点低,硬度大
难度: 简单查看答案及解析
-
从反应类型的角度来看,下列化学反应中,与其他三个类型不同的是( )
A.锌粒与稀硫酸反应制取氢气
B.铁粉投入硫酸铜溶液中析出铜
C.金属钠投入水中产生氢气和氢氧化钠
D.一氧化碳与三氧化二铁加热生成金属铁
难度: 简单查看答案及解析
-
在Na2O2与CO2的反应中,氧化剂与还原剂的质量比是( )
A.1∶1 B.2∶1 C.1∶2 D.8∶53
难度: 简单查看答案及解析
-
下列反应,其产物颜色按红色、红褐色、淡黄色、蓝色顺序排列的是( )
①金属钠在纯氧中燃烧 ②FeSO4溶液中滴入NaOH溶液并在空气中放置一段时间 ③FeCl3溶液中滴入KSCN溶液 ④无水硫酸铜放入医用酒精中
A.②③①④ B.③②①④ C.③①②④ D.①②③④
难度: 简单查看答案及解析
-
铁片放入下列溶液中,反应时无气体放出,取出后铁片质量减轻,则该溶液是( )
A.稀硫酸 B.浓盐酸 C.AgNO3 D.Fe2(SO4)3
难度: 简单查看答案及解析
-
在氯化铁、氯化铜和盐酸的混合溶液中加入铁粉,待反应结束,所剩余的固体滤出后能被磁铁吸引,则反应后溶液中存在较多的阳离子是( )
A.Cu2+ B.Fe2+ C.Fe3+ D.H+
难度: 简单查看答案及解析
-
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
选项
叙述Ⅰ
叙述Ⅱ
A
NH4Cl为强酸弱碱盐
用加热法除去NaCl中的NH4Cl
B
Fe3+具有氧化性
用KSCN溶液可以鉴别Fe3+
C
溶解度:CaCO3<Ca(HCO3)2
溶解度:Na2CO3<NaHCO3
D
SiO2可与HF反应
氢氟酸不能保存在玻璃瓶中
难度: 简单查看答案及解析
-
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
A.常温常压下,8 g O2含有4nA个电子
B.1 L 0.1 mol·L-1的氨水中有nA个NH
C.标准状况下,22.4 L盐酸含有nA个HCl分子
D.1 mol Na被完全氧化生成Na2O2,失去了2nA电子
难度: 中等查看答案及解析
-
下列有关物质的用途叙述错误的是( )
A.硅酸钠是制备木材防火剂的原料
B.二氧化硅是酸性氧化物,它不溶于任何酸
C.硅胶常作实验室和袋装食品等的干燥剂
D.石英、水晶、硅石的主要成分都是二氧化硅
难度: 简单查看答案及解析
-
用如右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是( )
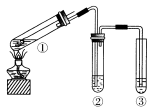
A.上下移动①中铜丝可控制SO2的量
B.②中选用品红溶液验证SO2的生成
C.③中选用NaOH溶液吸收多余的SO2
D.为确认CuSO4生成,向①中加水,观察颜色
难度: 简单查看答案及解析
-
在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验。下列收集Cl2的正确装置是( )
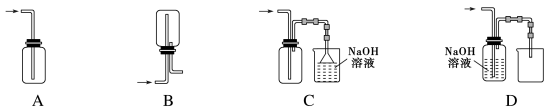
难度: 简单查看答案及解析
-
下列实验过程中,始终无明显现象的是( )
A.NO2通入FeSO4溶液中
B.CO2通入CaCl2溶液中
C.NH3通入AlCl3溶液中
D.SO2通入已酸化的Ba(NO3)2溶液中
难度: 简单查看答案及解析
-
下列措施不合理的是( )
A.用SO2漂白纸浆和草帽辫
B.用硫酸清洗锅炉中的水垢
C.高温下用焦炭还原SiO2制取粗硅
D.用Na2S做沉淀剂,除去废水中的Cu2+和Hg2+
难度: 简单查看答案及解析
-
已知:KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O。如下图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是( )
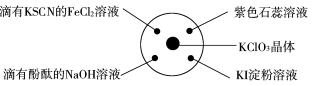
选项
实验现象
结论
A
滴有KSCN的FeCl2溶液变红
Cl2具有还原性
B
滴有酚酞的NaOH溶液褪色
Cl2具有酸性
C
紫色石蕊溶液先变红后褪色
Cl2具有漂白性
D
KI淀粉溶液变蓝色
Cl2具有氧化性
难度: 中等查看答案及解析
-
已知氨气极易溶于水,而难溶于有机溶剂CCl4,下列装置中不适宜做NH3的尾气吸收装置的是( )

难度: 简单查看答案及解析
-
水溶液中能大量共存的一组离子是( )
A.Na+、Mg2+、Cl-、CO
B.H+、Na+、Fe2+、MnO
C.K+、Ca2+、Cl-、NO
D.K+、NH
、OH-、SO
难度: 简单查看答案及解析
-
下列说法不正确的是( )
A.硫粉在过量的纯氧中燃烧可以生成大量的SO2
B.可以用品红溶液鉴别SO2和CO2
C.SO2能使品红溶液、酸性KMnO4溶液褪色,但褪色原理不同
D.少量SO2通过CaCl2的溶液能生成白色沉淀
难度: 简单查看答案及解析