-
设NA为阿佛加德罗常数,下列叙述错误的是( )
A.46g二氧化氮与四氧化二氮的混合气体中的原子数大于3NA
B.28g乙烯、丙烯、丙烷的混合气体中的碳原子数小于2NA
C.1mol/L 500mL氯化镁溶液中的镁离子数小于0.5NA
D.标准状况下,11.2L三氧化硫中所含的氧原子数大于1.5NA
难度: 简单查看答案及解析
-
下列叙述不正确的是( )
A.船底镶嵌锌块,锌作负极,以防船体被腐蚀
B.锌表面镀铜,锌作阳极
C.工业上电解饱和食盐水的阳极反应:
D.氢氧燃料电池(碱性)的正极反应是:
难度: 简单查看答案及解析
-
在下列各溶液中,离子一定能大量共存的是( )
A.强酸性溶液中:Na+、、Mg3+、Cl-、AlO2-
B.含有0.5 mol·L-1 Al3+的溶液中:K+、Cl-、CO32-、NO-3
C.含有0.5 mol·L-1 Ca2+的溶液中:Na+、K+、HCO3-、Cl-
D.室温下,pH=13的溶液中:Na+、K3+、NO-3、HCO3-
难度: 简单查看答案及解析
-
下列文字表述与反应方程式对应且正确的是 ( )
A.溴乙烷中滴入硝酸银溶液检验其中的溴元素:Br-+ Ag+ =AgBr↓
B.在碘化亚铁溶液中通人少量的氯气:2Fe2++Cl2 = 2Fe3+ + 2Cl-
C.实验室用液溴和苯在催化剂作用下制溴苯:

D.用醋酸除去水垢:CaCO3 + 2H+= Ca2+ + H2O + CO2↑
难度: 简单查看答案及解析
-
通常情况下,氯化钠、氯化铯、二氧化碳和二氧化硅的晶体结构分别如下图所示:

下列关于这些晶体结构和性质的叙述不正确的是
A.在氯化钠晶体中每个Cl周围同时吸引6个Na,在氯化铯晶体中每个Cl周围同时吸引8个Cs
B.氯化钠、氯化铯和二氧化碳的晶体都有立方的晶胞结构,它们具有相似的物理性质
C.二氧化碳晶体是分子晶体,其中不仅存在分子间作用力,而且也存在共价键
D.在二氧化硅晶体中,平均每个Si原子形成4个Si一O共价单键
难度: 简单查看答案及解析
-
可逆反应:3A(g)
3B(?)+C(?)其△H>0,随着温度升高,混合气体的平均相对分子质量有变小的趋势,则下列判断正确的是( )
A.若C为固体,则B一定是气体 B. B、C可能都是固体
C.B和C一定都是气体 D.B和C不可能都是气体
难度: 简单查看答案及解析
-
下表各组物质中,物质之间通过一步反应就能实现如图所示转化的是 ( )
物质
选项
a
b
c
d
A
Al
Al(OH)3
NaAlO2
NaOH
B
CH3CH2OH
CH3CHO
CH3COOH
O2
C
Na2CO3
NaHCO3
NaOH
CO2
D
Cl2
FeCl3
FeCl2
Fe
难度: 简单查看答案及解析
-
被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品。截至2005年底,已被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义。其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如右图所示。有关化合物的叙述正确的是( )
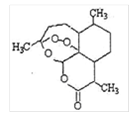 A.分子式为:C16H22O5
A.分子式为:C16H22O5B.该化合物在一定条件下不能与NaOH溶液反应
C.该化合物中含有过氧键,一定条件下有氧化性
D.菁蒿素与维生素一样是水溶性的
难度: 简单查看答案及解析
 (1)装药品前,按图装置连接后,如何检验气密性?
(1)装药品前,按图装置连接后,如何检验气密性?


