-
天然气的主要成分CH4也是一种会产生温室效应的气体,对于相同分子数的CH4和CO2,CH4产生的温室效应更明显.下面是有关天然气的几种叙述;①天然气与煤、柴油相比是较清洁的能源;②等质量的CH4和CO2产生的温室效应也是前者明显;③燃烧天然气也是酸雨的成因之一.其中正确的是( )
A.①和②
B.只有①
C.只有③
D.①②③难度: 中等查看答案及解析
-
为减少大气中CO2的浓度,有人根据液态CO2密度大于海水密度的事实,设想将CO2液化后,送入深海海底,为使CO2液化,可采取的措施是( )
A.减压、升温
B.增压、升温
C.减压、降温
D.增压、降温难度: 中等查看答案及解析
-
食用下列方法处理过的食品,不会危及人体健康的是( )
A.牛奶中添加氧化钙以补充钙质
B.用干冰冷藏的食品
C.用工业用盐腌制的肉类食品
D.用甲醛浸泡的海鲜难度: 中等查看答案及解析
-
钒(V)是一种重要的金属.以下对三个涉及钒化合物反应的分析错误的是
①KClO3+6VOSO4+3H20→KCl+3(V02)2SO4+3H2SO4;
②2NH4Cl+(VO2)2SO4+2H2O→2NH4VO3↓+2HCl+H2SO4
③2NH4VO32NH3↑+H2O+V2O5( )
A.反应①中VOSO4被氧化
B.反应①中钒元素的化合价升高
C.反应②中钒元素的化合价降低
D.反应③是分解反应难度: 中等查看答案及解析
-
以下操作所用试剂错误的是( )
A.清洗做完焰色反应的铂丝-稀盐酸
B.洗去附着在试管内壁的氯化银-稀硝酸
C.干燥氨气-碱石灰
D.干燥CO气体-浓硫酸难度: 中等查看答案及解析
-
下列制取物质的设计中,不可能实现的是( )
①CaOCa(OH)2
CaCl2
CaCO3
②KClO3O2
CuO
Cu(NO3)
③FeH2
Cu
Ag
④SO3Na2SO4
BaSO4
BaCl2.
A.①②
B.②③
C.①④
D.③④难度: 中等查看答案及解析
-
吗啡是严格查禁的毒品.吗啡分子含C71.58%,H6.67%,N4.91%,其余为O.已知其相对分子质量不超过300,则吗啡的分子式是( )
A.C17H19NO3
B.C17H20N2O
C.C18H19NO3
D.C18H20N2O2难度: 中等查看答案及解析
-
研究发现,空气中少量的NO2能参与SO2转化为硫酸的反应.反应过程如下
①SO2+NO2→SO3+NO
②SO3+H2O→H2SO4
③2NO+O2→2NO2
下列说法正确的是( )
A.常温下,SO2很难与O2反应生成SO3
B.常温下NO能与O2生成NO2
C.NO2是SO2转化为硫酸的中间产物
D.NO2是SO2转化为硫酸的催化剂难度: 中等查看答案及解析
-
实验室用纯净N2和H2合成NH3(N2+3H2
2NH3)时,是先将分别制得的含水蒸气的N2和H2通过如图所示的装置.下面是对该装置作用的几种叙述①干燥气体②混合气体③观察气体的流速.正确的是( )
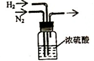
A.只有①
B.只有①和②
C.只有①和③
D.①②③难度: 中等查看答案及解析
-
某混合气体可能含有CO2、CO、水蒸气(H2O)、H2中的一种或几种,依次进行连续处理(假定每步处理均反应完全):①通过碱石灰时,气体体积变小;②通过赤热的氧化铜时,固体变成红色;③通过白色硫酸铜粉末时,粉末变成蓝色;④通过澄清的石灰水时,溶液变得浑浊.由此可以确定原混合气体中( )
A.一定含有CO2、H2O,至少含H2、CO中的一种
B.一定含有H2O、CO,至少含有CO2、H2中的一种
C.一定含有CO、CO2,至少含有H2O、H2中的一种
D.一定含有CO、H2,至少含有H2O、CO2中的一种难度: 中等查看答案及解析
-
已知气体的摩尔质量越小,扩散速度越快.图所示为气体扩散速度的实验.两种气体扩散时形成图示的白色烟环.对甲、乙物质的判断,正确的是( )

A.甲是浓氨水,乙是浓硫酸
B.甲是浓氨水,乙是浓盐酸
C.甲是氢氧化钠溶液,乙是浓盐酸
D.甲是浓硝酸,乙是浓氨水难度: 中等查看答案及解析
-
常温下,下列各组物质只用一种试剂不能鉴别出来的是( )
A.食盐、烧碱、氢氧化镁
B.蔗糖、硫酸铜粉末、碳酸钙粉末
C.焦炭、氧化铜、氧化亚铁
D.碳酸钠溶液、硝酸钠溶液、氯化钠溶液难度: 中等查看答案及解析
-
Cu(NO3)2受热易分解,其分解反应为:2Cu(NO3)2
2CuO+4NO2↑+O2↑.某学生将带火星的木条放入Cu(NO3)2受热分解得到的混合气体中,木条复燃,则下列判断正确的是( )
A.产物中有氧气,所以木条复燃
B.不能确定NO2是否助燃
C.NO2肯定也能助燃
D.NO2肯定不能助燃难度: 中等查看答案及解析
-
金属钨用途广泛,H2还原WO3可得到钨,其总反应为:WO3+3H2
W+3H2O,该总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
;假设WO3完全转化为W,则三个阶段消耗H2质量之比为( )温度(℃) 25℃~550℃~600℃~700℃ 主要成分 WO3 W2O5 WO2 W
A.1:1:4
B.1:1:3
C.1:1:2
D.1:1:1难度: 中等查看答案及解析
-
已知,20℃,NaHCO3的溶解度为9.6g/100g水,饱和食盐水与浓NH4HCO3溶液混合有沉淀产生,反应为NaCl+NH4HCO3=NaHCO3↓+NH4Cl.下列说法错误的是( )
A.该反应是复分解反应
B.反应得到的溶液中NaHCO3已达到饱和
C.NH4Cl可做氨肥
D.反应得到溶液中溶质只有NH4Cl难度: 中等查看答案及解析
-
现有一种营养液,可能由KNO3、Ca(NO3)2、K2CO3、KCl中的一种或几种物质组成,为探究其成分,设计并完成了如图所示的实验.下列推断错误的是( )

A.实验1可确定原营养液中没有K2CO3
B.实验1、2可推测原营养液的组成可能有2种情况
C.只计算实验1沉淀的质量不能确定该营养液的组成
D.计算实验1和实验2的沉淀质量能确定该营养液的组成难度: 中等查看答案及解析
-
如图表示甲、乙两种固体(均不含结晶水)物质饱和溶液的溶质质量分数随温度变化的曲线,现分别向50g甲、80g乙固体中各加入150g水,并加热至完全溶解,同时各蒸发掉50g水,下列分析正确的是( )
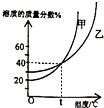
A.冷却至t℃时,甲、乙两种溶液的溶质质量分数相等
B.冷却至t℃时,甲、乙均有晶体析出
C.冷却到0℃时,乙析出的晶体多
D.0℃时,甲的溶解度大于乙难度: 中等查看答案及解析
-
已知2CO2+2Na2O2═2Na2CO3+O2,N2不与Na2O2反应,将等物质的量的N2、O2、CO2通入Na2O2后,剩余气体的物质的量为原来的
,此时N2、O2、CO2物质的量之比是( )
A.3:4:1
B.3:4:2
C.6:7:3
D.6:8:3难度: 中等查看答案及解析
-
已知反应:2FeCl3+Fe→3FeCl2;2FeCl3+Cu→2FeCl2+CuCl2.向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,烧杯中不可能出现的是( )
A.有铜无铁
B.有铁无铜
C.铁、铜都有
D.铁、铜都无难度: 中等查看答案及解析
-
为测定某氢氧化钡溶液的质量分数,取稀硫酸20g,逐滴加入氢氧化钡溶液30g,同时用仪器测定并记录反应过程中混合溶液pH变化情况(如图所示),过滤后得滤液47.67g,则氢氧化钡溶液的质量分数是( )
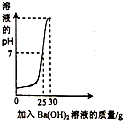
A.0.057
B.0.06
C.0.0684
D.0.00855难度: 中等查看答案及解析
-
电解饱和食盐水及电解产物的反应过程如下:

下列叙述错误的是( )
A.气体A是氢气
B.反应生成的A和Cl2恰好完全反应生成C
C.碱B只能是NaOH
D.酸D只有和碱B反应才能生成NaCl难度: 中等查看答案及解析
-
除去下列物质中混有的杂质,所选用的试剂或操作方法正确的是( )
物质 杂质 除杂质选用的试剂和操作方法 A CO2 H2 通入O2,点燃,通过装浓硫酸的洗气瓶 B CO2 SO2 依次通过装氢氧化钠溶液和浓硫酸的洗气瓶 C KCl溶液 MgCl2溶液 滴加KOH溶液至不再产生沉淀为止 D 氧化钙 碳酸钙 煅烧,至固体质量不在减少为止
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
已知:①K2CO3+C02+H20→2KHCO3;CaCO3+CO2+H2O→Ca(HCO3)2 ②KHCO3、Ca(HCO3)2都易溶于水 ③通入悬浊液中的气体,与溶液反应后才与沉淀反应,将足量CO2通入KOH和Ca(OH)2的混合稀溶液中,则生成沉淀的质量和通入的CO2质量的关系中,正确的是( )
A.
B.
C.
D.难度: 中等查看答案及解析
-
已知有机物C2H4O、C3H62和C4H8组成的混合物中,碳元素的质量分数为a%,则氧元素的质量分数为( )
A.(100-)%
B.%
C.%
D.无法计算难度: 中等查看答案及解析
-
气体A(C2H2) 是无色、难溶于水的气体,实验室常用CaC2(块状固体)和水在常温下反应制备:CaC2+2H2O→Ca(OH)2(微溶)+C2H2↑.下列有关实验室制备A的叙述不正确的是( )
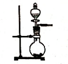
A.用如图所示装置可以制A
B.制A肯定可以用启普发生器
C.用排水法收集到的A较纯
D.用排空气法收集到的A密度偏小难度: 中等查看答案及解析
-
工业上在一定条件下,CO2和H2以物质的量之比为1:3恰好反应,得到了某重要的化工原料和水,该化工原料的化学式不可能为( )
A.C2H6
B.C6H12
C.C2H6O
D.C3H82难度: 中等查看答案及解析
-
如图是甲、乙、丙三种固体(均不含结晶水)的溶解度曲线.20℃时,烧杯中分别盛有相同质量的甲、乙、丙饱和溶液,各加入等质量的对应固体,并升温至40℃,观察到,甲固体逐渐减少至全部溶解,下列判断正确的是( )
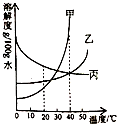
A.乙固体逐渐减少至全部溶解
B.乙溶液是饱和溶液
C.丙固体逐渐增多
D.乙、丙溶液的浓度相同难度: 中等查看答案及解析
-
物质的量为0.10mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为( )
A.3.2g
B.4.0g
C.4.2g
D.4.6g难度: 中等查看答案及解析
-
用NA表示阿伏伽德罗常数,下列叙述正确的是( )
A.S2和S8的混合物质共6.4g,混合物中含硫原子数为0.1NA
B.SO2、SO3一个分子的质量分别为ag和bg,则氧原子的摩尔质量(b-a)g/mol
C.化合物C4H8和C3H6共28g,完全燃烧消耗的氧分子3NA
D.一个氧原子的实际重量约等于16g/NA难度: 中等查看答案及解析
-
把绿矾和足量的KOH溶液加入到含K2Cr2O7的废水中,可得KOH和K2SO4的混合溶液以及磁性材料Cr0.5Fe1.5FeO4(Fe的化合价依次为+3、+2价),处理含K2Cr2O75.00×10-3mol的废水,需要绿矾的质量是( )
A.6.95g
B.13.9g
C.11.12g
D.8.34g难度: 中等查看答案及解析
-
工业上用甲和乙反应制备丙,根据下列微观示意图得出的结论中,正确的是( )
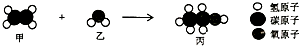
A.甲的摩尔质量是28g/mol
B.反应中甲、乙、丙的分子个数比为2:1:1
C.甲、乙、丙都是有机物
D.丙中C、H、O元素的质量比为12:3:8难度: 中等查看答案及解析
-
如图,将乙针筒内的物质压到甲针筒内,进行下表所列实验,对实验现象的描述错误的是
( )选项 甲针筒内物质 乙针筒内物质 甲针筒的现象 A 10mLCO2 10mL浓氢氧化钠溶液 活塞自动向内压缩 B 20mLH2 10mLO2 生成无色液体,活塞自动向内压缩 C 10mLFe2(SO4)3溶液 10mLBa(OH)2溶液 生成白色沉淀 D 1g铁粉末 10mL49%密度为1.3g/mL稀硫酸 生成无色气体,溶液呈浅绿色,活塞自动外移,无固体剩余 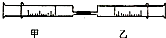
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
下图是物质在不同状态时微粒间距离的示意图.

已知:某气体在常温常压下,1mol的体积是V(L)、密度是ρ(g/L),该气体每个分子的质量为m(g)、体积为△(L),该气体的摩尔质量为M(g/mol),NA为阿伏伽德罗常数,下面关系式正确的是( )
A.m=
B.NA=
C.△=
D.ρ=难度: 中等查看答案及解析
-
在100g浓度为ω%的稀硫酸中加入4g氧化铜粉末,待氧化铜全部溶解后,向所得蓝色溶液中加入10g铁粉,充分反应后,过滤,得滤液和5.2滤渣.下列计算结果正确的是( )
A.5.2g滤渣是由3.2g铜和2g铁组成
B.滤液是25%的硫酸亚铁溶液
C.反应过程中产生的氢气是0.286g
D.ω=14难度: 中等查看答案及解析