-
下列各组物质熔化或气化时,所克服的微粒间的作用力属同种类型的是
A.SiO2和干冰的熔化 B.氧化钠和钠的熔化
C.晶体硅和晶体硫的熔化 D.碘和干冰的气化
难度: 中等查看答案及解析
-
下列叙述错误的是
①离子键没有方向性和饱和性,而共价键有方向性和饱和性
②配位键在形成时,是由成键双方各提供一个电子形成共用电子对
③金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用
④在冰晶体中,既有极性键、非极性键,又有氢键
⑤化合物NH4Cl和CuSO4·5H2O都存在配位键
⑥NaCl、HF、CH3CH2OH、SO2都易溶于水,但原因不完全相同
A.①③ B.②④ C.②⑤ D.④⑥
难度: 中等查看答案及解析
-
下列对σ键的认识不正确的是
A. ss σ键与sp σ键的对称性相同
B.烯烃分子中的碳碳双键的键能是碳碳单键键能的二倍
C.分子中含有共价键,则至少含有一个σ键
D.含有π键的化合物与只含σ键的化合物的化学性质不同
难度: 中等查看答案及解析
-
下列物质中,中心原子的杂化类型为sp3杂化的是
A.C2H6 B.C2H2 C.BF3 D.C2H4
难度: 中等查看答案及解析
-
下列物质的性质与氢键无关的是
A.冰的密度比液态水的密度小
B.NH3易液化
C.在相同条件下,H2O的沸点比H2S的沸点高
D.HF分子比HCl分子稳定
难度: 中等查看答案及解析
-
下列说法中正确的是
A.s区都是金属元素 B.s区都是主族元素
C.稀有气体在ds区 D.所有非金属元素都在p区
难度: 中等查看答案及解析
-
下列各组分子中,都属于含极性键的非极性分子的是
A.C2H4 C6H6 B.CO2 H2O2
C.C60 C2H4 D.NH3 HBr
难度: 中等查看答案及解析
-
下列元素的最高价氧化物对应的水化物酸性最强的是
A.第3周期有7个价电子的元素
B.价电子排布式为3s23p2的元素
C.原子的L电子层p轨道只填了2个电子的元素
D.3p轨道电子半充满的元素
难度: 中等查看答案及解析
-
基态原子的核外电子排布为[Kr]4d105s1的元素属于的区、周期和族为
A.p区、第五周期、ⅠB族 B.ds区、第五周期、ⅠB族
C.d区、第四周期、ⅠB族 D.ds区、第五周期、Ⅷ族
难度: 中等查看答案及解析
-
下列关于晶体的说法中,不正确的是
①晶体中粒子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性;
②含有金属阳离子的晶体一定是离子晶体;
③共价键可决定分子晶体的熔、沸点;
④MgO和NaCl两种晶体中, MgO的晶格能较小,所以其熔点比较低
⑤晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列;
⑥晶体尽可能采取紧密堆积方式,以使其变得比较稳定;
⑦干冰晶体中,一个CO2分子周围有12个CO2分子紧邻;CsCl和NaCl晶体中阴、阳离子的配位数不同
A.①②③ B.②③⑦
C.④⑤⑥ D.②③④
难度: 中等查看答案及解析
-
下列各反应中属于取代反应的是
A.乙醇与浓硫酸在170℃条件下反应
B.乙醇在一定条件下转化为乙醛
C.苯酚与溴水反应
D.乙醛溶液中加入银氨溶液后水浴加热
难度: 中等查看答案及解析
-
下列表述中,属于烷烃特征的是
A.完全燃烧产物只有二氧化碳和水 B.几乎不溶于水
C.分子的通式为CnH2n+2,与氯气发生取代反应 D.它们是非电解质
难度: 中等查看答案及解析
-
以下几种物质:①白磷、②单晶硅、③甲烷、④四氯化碳,具有正四面体构型的分子的是( )
A.①②③ B.①③④ C.②③④ D.①②③④
难度: 中等查看答案及解析
-
下列说法不正确的是
A.乙烯、苯都可与溴水发生加成反应
B.乙醇、乙烯都可被酸性高锰酸钾溶液氧化
C.乙醇、乙酸都可以发生酯化反应
D.淀粉、油脂、蛋白质都可以发生水解反应
难度: 中等查看答案及解析
-
常温常压下,20mL某气态烃与85mL O2混合点燃并完全燃烧后恢复到原来状况,剩余气体为55mL,则此烃的化学式为
A.C2H4 B.C2H2 C.C3H6 D.C6H6
难度: 中等查看答案及解析
-
下列烷烃在光照下与氯气反应,只生成一种一氯代烃的是

难度: 中等查看答案及解析
-
甲醛(CH2O)、乙酸(C2H4O2)和丙醛(C3H6O)组成的混合物中,氧元素的质量分数是37%,则氢元素的质量分数为
A.11% B.28% C.54% D.9%
难度: 中等查看答案及解析
-
下列原子中未成对电子数为3的是
A.O B.N C.F D.Cu
难度: 中等查看答案及解析
-
下列各组互为等电子体的是
A.N2O和NO2 B.O3和SO2 C.CH4和NH3 D.OH-和NH2-
难度: 中等查看答案及解析
-
已知X、Y是主族元素,I为电离能,单位kJ/mol。根据下表所列数据判断错误的是
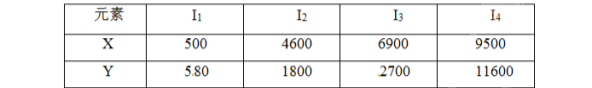
A.元素X的常见化合物价是+1价
B.若元素Y处于第3周期,它可与冷水剧烈反应
C.元素X与氯形成化合物时,化学式可能是XCl
D.元素Y是ⅢA族的元素
难度: 中等查看答案及解析