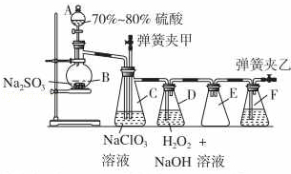
-
(2015秋•湖州期末)下列化合物中,属于盐的是( )
A.NaOH B.HCl C.H2SO4 D.NaCl
难度: 简单查看答案及解析
-
(2015秋•湖州期末)仪器名称为“容量瓶”的是( )
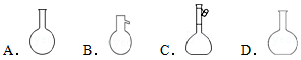
难度: 简单查看答案及解析
-
(2015秋•湖州期末)常温下能与浓硫酸发生剧烈反应的金属单质是( )
A.Cu B.C C.Fe D.Mg
难度: 简单查看答案及解析
-
(2015秋•湖州期末)胶体和溶液的本质区别是( )
A.丁达尔效应 B.分散剂不同
C.能否稳定存在 D.分散质粒子直径的大小
难度: 简单查看答案及解析
-
(2015秋•湖州期末)与KCl的化学键类型相同的物质是( )
A.H2O B.HCl C.MgCl2 D.SO2
难度: 中等查看答案及解析
-
(2015秋•湖州期末)SO2+H2O⇌H2SO3的反应类型属于( )
A.分解反应 B.复分解反应 C.置换反应 D.化合反应
难度: 简单查看答案及解析
-
(2015秋•湖州期末)在反应Cl2+H2O⇌HCl+HClO中,氧化剂是( )
A.Cl2 B.H2O C.HCl D.HClO
难度: 简单查看答案及解析
-
(2015秋•湖州期末)下列化学用语表述正确的是( )
A.甲烷的球棍模型:

B.氯化氢的电子式:
C.Cl2的结构式:Cl=Cl
D.硫离子的结构示意图:
难度: 中等查看答案及解析
-
(2015秋•湖州期末)氧元素在周期表中的位置是( )
A.第二期ⅣA族 B.第三期ⅥA族 C.第二期ⅥA族 D.第三期ⅣA族
难度: 简单查看答案及解析
-
(2015秋•湖州期末)在酸性溶液中,下列离子不能大量存在的是( )
A.Mg2+ B.OHˉ C.SO42﹣ D.Fe3+
难度: 中等查看答案及解析
-
(2015秋•湖州期末)将某气体X通入品红溶液,溶液褪色;加热,溶液不能变红色.X可能是( )
A.O2 B.SO2 C.Cl2 D.CO2
难度: 简单查看答案及解析
-
(2015秋•湖州期末)下列电离方程式中,不正确的是( )
A.NaOH═Na++OHˉ B.H2SO4═H2++SO42﹣
C.Na2CO3═2Na++CO32﹣ D.CH3COOH⇌CH3COOˉ+H+
难度: 简单查看答案及解析
-
(2015秋•湖州期末)实验室用NaOH固体和蒸馏水准确配制一定物质的量浓度的NaOH溶液时,以下仪器中不需要用到的是( )
A.托盘天平 B.锥形瓶 C.烧杯 D.容量瓶
难度: 中等查看答案及解析
-
(2015秋•湖州期末)下列说法不正确的是( )
A.核素
H的中子数是0
B.16O和18O互为同位素
C.纳米碳管和足球烯互为同素异形体
D.C2H6O有两种同分异构体
难度: 简单查看答案及解析
-
(2015秋•湖州期末)下列几种试剂不能把浓度均为0.1mol•L﹣1的Na2CO3、NaHCO3鉴别开的是( )
A.0.1 mol•Lˉ1BaCl2溶液 B.澄清石灰水
C.稀盐酸 D.pH试纸
难度: 中等查看答案及解析
-
(2015秋•湖州期末)100mL0.3mol•L﹣1Na2SO4溶液和50mL0.2mol•L﹣1Al2(SO4)3溶液混合后,溶液中SO42﹣离子的物质的量浓度(设体积为二者之和)为( )
A.0.2mol•L﹣1 B.0.25 mol•L﹣1 C.0.4 mol•L﹣1 D.0.5 mol•L﹣1
难度: 困难查看答案及解析
-
(2015秋•湖州期末)下列物质发生反应时,不因为反应的条件、反应物浓度或反应物的用量不同,而产物不同的是( )
A.钠与氧气 B.碳与氧气 C.硅和氯气 D.铁和硫酸
难度: 中等查看答案及解析
-
(2015秋•湖州期末)下列说法中正确的是( )
A.自然界中不存在游离态的硫
B.二氧化碳的排放会导致酸雨的产生
C.二氧化硫能使滴有酚酞的氢氧化钠溶液褪色,体现了其漂白性
D.浓硫酸可用来干燥SO2、CO、Cl2等气体
难度: 简单查看答案及解析
-
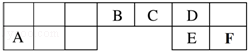
(2015秋•湖州期末)短周期元素X、Y、Z、W、Q在元素周期表中的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法中不正确的是( )
X
Y
Z
W
Q
A.由Y与W形成的氧化物溶于水一定是强酸
B.Z和Y组成的物质是原子晶体
C.Z与Q形成的物质能与H2在一定条件下反应
D.X和Y均存在同素异形体
难度: 中等查看答案及解析
-
(2015秋•湖州期末)下列离子方程式正确的是( )
A.硫酸铜溶液与氢氧化钡溶液反应:SO
+Ba2+═BaSO4↓
B.漂白粉溶液在空气中发生的反应:Ca2++2ClO﹣+CO2+H2O═2HClO+CaCO3↓
C.碳酸钙溶解于盐酸中:CO32﹣+2H+═CO2↑+H2O
D.氯化铁溶液与碘化钾溶液反应:Fe3++2Iˉ═Fe2++I2
难度: 中等查看答案及解析
-
(2015秋•湖州期末)下列说法正确的是( )
A.二氧化硅的化学性质不活泼,能与强碱反应不与任何酸反应
B.生物炼铜就是利用植物对铜离子的吸收达到富集铜的目的
C.过量二氧化硫通入石蕊溶液中能使石蕊溶液先变红色后褪色
D.工业上利用氢气在氯气中燃烧生成氯化氢,再将氯化氢溶于水制得盐酸
难度: 中等查看答案及解析
-
(2015秋•湖州期末)某无色透明的溶液,在强酸性和强碱性的条件下都能大量共存的是( )
A.Fe2+、K+、SO42﹣、HCO3﹣ B.Mg2+、Na+、SO42﹣、Cl﹣
C.Na+、K+、SO42﹣、NO3﹣ D.Ba2+、Na+、MnO4﹣、SO42﹣
难度: 困难查看答案及解析
-
(2015秋•湖州期末)下列说法正确的是( )
A.镁着火后可用二氧化碳灭火器进行灭火
B.焰色反应时,先用稀硫酸洗涤铂丝并在酒精灯火焰上灼烧,然后再进行实验
C.食盐水中混有Mg2+、Ca2+、SO42﹣,可依次加入过量Ba(OH)2溶液、Na2CO3溶液和适量盐酸,过滤后即可得到精制的食盐水
D.现代化学分析测试中,常借助一些仪器来分析化学物质的组成.如用原子吸收光谱确定物质中含有哪些金属元素
难度: 中等查看答案及解析
-
(2015秋•湖州期末)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.含有2NA个氧原子的氧气与臭氧的混合气体的质量为16g
B.标准状况下,22.4 mL水中含有的分子数目约为1.24NA
C.300 mL 2 mol•L﹣1酒精溶液中所含分子数为0.6 NA
D.1 mol Cl2参加的任何反应转移电子数都是2NA
难度: 困难查看答案及解析
-
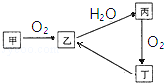
(2015秋•湖州期末)某混合物X由Na2O、Fe2O3、Cu、SiO2中的一种或几种物质组成.某校兴趣小组以两条途径分别对X进行如下实验探究.

下列有关说法不正确的是( )
A.由Ⅱ可知X中一定存在SiO2
B.无法判断混合物中是否含有Na2O
C.1.92 g固体成分为Cu
D.15.6 g混合物X中m(Fe2O3):m(Cu)=1:1
难度: 困难查看答案及解析