-
据ETH天文研究所报告,组成太阳的气体中存在20Ne和22Ne,下列关于20Ne和22Ne的说法正确的是
A. 20Ne和22Ne互为同位素
B. 20Ne和22Ne互为同分异构体
C. 20Ne和22Ne的质量数相同
D. 20Ne和22Ne的中子数相同
难度: 中等查看答案及解析
-
下列有关叙述错误的是
A.人体中没有水解纤维素的酶,纤维素在人体中主要是加强胃肠的蠕动,有通便功能
B.油脂能增加食物的滋味,也是产生能量最高的营养物质,应尽可能多食用
C.动物的毛和皮、蚕丝都是蛋白质,可用来制作服装、药材等
D.葡萄糖是人体内主要供能物质,血液中葡萄糖含量过低,会使人患“低血糖”症
难度: 中等查看答案及解析
-
下列有关化学用语表示正确的是
A.乙烯的结构简式:CH2CH2
B.NH3的电子式:
C.过氧化氢的电子式:
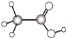
D.乙酸的球棍模型:
难度: 中等查看答案及解析
-
下列物质中含有共价键的离子化合物是
A.CO2 B.NaCl C.KOH D.CH4
难度: 简单查看答案及解析
-
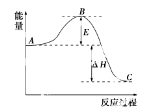
4P(红磷s)
P4(白磷s) △H = +17kJ•mol﹣1根据以上方程式,下列推论正确的是
A.正反应是一个放热反应
B.当lmol白磷完全转变成红磷时放出17kJ热量
C.当4g红磷转变成白磷时吸收17kJ热量
D.白磷比红磷稳定
难度: 中等查看答案及解析
-
下列物质中,不能使酸性KMnO4溶液褪色的物质是
①
②乙烯 ③CH3COOH ④CH3CH2OH ⑤CH2=CH—COOH ⑥
A.①⑥ B.①③④⑥ C.①④ D.①③⑥
难度: 中等查看答案及解析
-
将纯锌片和纯铜片按图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是

A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大
D.甲、乙溶液均变蓝色
难度: 简单查看答案及解析
-
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是
A. X的气态氢化物比Y的稳定
B. W的最高价氧化物对应水化物的酸性比Z的强
C. Z的非金属性比Y的强
D. X与Y形成的化合物都易溶于水
难度: 中等查看答案及解析
-
将等体积的甲烷与氯气混合于一试管中并倒置于水槽里,置于光亮处。下列有关此实验所观察到的现象或结论中,不正确的是
A.瓶中气体的黄绿色逐渐变浅
B.此反应的生成物只有一氯甲烷
C.瓶内壁有油状液滴形成
D.试管中液面上升
难度: 中等查看答案及解析
-
下列反应原理符合工业冶炼金属镁的是
A.2Na+MgCl2=2NaCl+Mg
B.MgCl2(熔化)
Mg+Cl2
C.2MgO
2Mg+O2
D.MgO+C
MgO+C
难度: 中等查看答案及解析
-
为提纯下列物质(括号内为杂质).所选试剂及方法均正确的是
选项
物质(括号内为杂质)
除杂试剂
方法
A
溴苯(溴)
CCl4
分液
B
硝基苯(NO2)
NaOH溶液
分液
C
乙烷(乙烯)
氢气
洗气
D
乙醇(乙酸)
NaOH溶液
分液
难度: 中等查看答案及解析
-
某同学在试管中做铁钉与稀硫酸反应的实验,发现反应速率较慢,下列措施:①给试管加热 ②加入铁粉 ③加入冰块④加入少量醋酸钠晶体 ⑤将稀硫酸换为浓硫酸,能加快反应速率的是
A.①②⑤ B.①② C.③④ D.③④⑤
难度: 中等查看答案及解析
-
“绿色化学”的主要内容之一是从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物.下列化学反应不符合“绿色化学”理念的是
A.制氯乙烷:CH2=CH2+HCl
CH3CH2Cl
B.制甲基丙烯酸甲酯:CH3C≡CH+CO+CH3OH
CH2=C(CH3)COOCH3
C.制CuSO4:2Cu+O2 = 2CuO,CuO+H2SO4(稀)═CuSO4+H2O
D.制Cu(NO3)2:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O
难度: 中等查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列说法中正确的是
A.0.5 mol苯分子中含有C=C双键数目为1.5 NA
B.常温常压下,17 g 羟基含有的电子总数为9NA
C.标准状况下,11.2 L CHCl3 中含有的共价键数目为2NA
D.将1 mol蔗糖与稀H2SO4混合使之完全水解,可生成2NA个葡萄糖分子
难度: 简单查看答案及解析
-
苯环结构中,不存在单双键交替结构,可以作为证据的事实是
①苯不能使酸性KMnO4溶液褪色;
②苯中碳碳键的键长均相等;
③苯能在一定条件下跟H2加成生成环己烷;
④经实验测得邻二甲苯(
)仅一种结构;
⑤苯在FeBr3存在的条件下同液溴可发生取代反应,但不能因化学变化而使溴水褪色。
A. ③④⑤ B. ①③④ . C. ①②④⑤ D. ①②③
难度: 中等查看答案及解析
-
氢氧燃料电池是一种将化学能转化为电能的高效、环境友好的发电装置.该电池的构造如图所示,下列分析判断错误的是
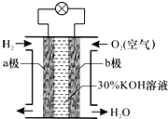
A.a极为负极,b极为正极
B.负极发生氧化反应
C.正极的电极反应为O2+2H2O+2e﹣═4OH﹣
D.负极的电极反应为H2+2OH﹣﹣2e﹣═2H2O
难度: 简单查看答案及解析
-
核糖是合成核酸的重要原料,结构简式为:CH2OHCHOHCHOHCHOHCHO.下列关于核糖的叙述不正确的是
A.与葡萄糖互为同分异构体
B.既可以与氧气反应,也可以与新制氢氧化铜反应
C.1个核糖分子可以与4个乙酸分子发生酯化反应
D.不能使紫色石蕊试液变红
难度: 简单查看答案及解析
-
某烃的结构简式为
,它可能具有的性质是
A. 它能使溴水褪色,但不能使酸性高锰酸钾溶液褪色
B. 它既能使溴水褪色,也能使酸性高锰酸钾溶液褪色
C. 易溶于水,也易溶于有机溶剂
D. 能发生加成反应,一定条件下最多可与三倍物质的量的氢气加成
难度: 中等查看答案及解析
-
下列各实验装置图及其作用正确的是
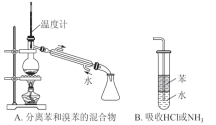

难度: 中等查看答案及解析
-
在相同的温度和压强下,下列两个热化学方程式中△H1与△H2关系为
2H2(g)+O2(g)=2H2O(g) △H1 ; 2H2(g)+O2(g)=2H2O(l) △H2
A.△H1<△H2 B.△H1>△H2 C.△H1=△H2 D.△H1=2△H2
难度: 中等查看答案及解析
-
下列电子式书写正确的是
A.HClO
B.OH—
C.HCl
D.Na2O2
难度: 中等查看答案及解析
-
根据元素周期表和周期律分析下面推断错误的是
A. 铍原子失电子能力比镁弱
B. HI比砹的氢化物稳定
C. 氢氧化铝碱性比氢氧化镁强
D. 高氯酸的酸性比硫酸强
难度: 简单查看答案及解析
-
下面实验操作可以实现实验目的是
A. 鸡蛋白溶液中,加入浓的硫酸铵溶液有沉淀析出,加入水后沉淀不溶解
B. 将SO2通入酸性KMnO4溶液中,溶液褪色,证明SO2具有漂白性
C. 取样灼烧,可以鉴别某白色纺织品是棉织品还是羊毛制品
D. 取少量蔗糖溶液加稀硫酸,水浴加热几分钟后,再加入新制的氢氧化铜悬浊液,并且加热,观察现象,判断蔗糖水解的产物中是否含有葡萄糖
难度: 中等查看答案及解析
-
下列反应中,属于取代反应的是
①CH3CH=CH2 + Br2
CH2BrCH=CH2 + HBr
②CH3CH2Br + NaOH
CH2=CH2 + H2O + NaBr
③CH3COOCH2CH3 + H2O
CH3COOH + CH3CH2OH
④C6H5OH + 3H2
C6H11OH.
A.①② B.③④ C.①③ D.②④
难度: 简单查看答案及解析
-
铜的冶炼大致可分为:
①富集,将硫化物矿进行浮选;
②焙烧,主要反应为2CuFeS2+4O2===Cu2S+3SO2+2FeO(炉渣);
③制粗铜,在1 200 ℃发生的主要反应为2Cu2S+3O2===2Cu2O+2SO2,2Cu2O+Cu2S===6Cu+SO2↑;
④电解精炼铜。
下列说法不正确
A.上述灼烧过程的尾气回收后可用来制硫酸
B.上述过程中,由6 mol CuFeS2制取6 mol Cu时共消耗15 mol O2
C.在反应2Cu2O+Cu2S===6Cu+SO2↑中,氧化产物与还原产物的物质的量比1:6
D.在反应2Cu2O+Cu2S===6Cu+SO2↑中,只有Cu2O作氧化剂
难度: 困难查看答案及解析
 的系统名称是
的系统名称是 的系统名称是
的系统名称是