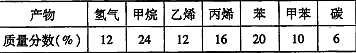
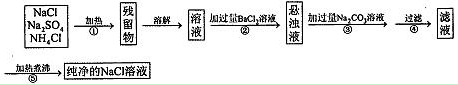
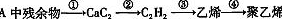-
糖类、油脂、蛋白质为动物性和植物性食物中的基本营养物质。下列有关说法正确的是( )
A.糖类物质中只含有C、H、O三种元素
B.糖类、油脂、蛋白质都是高分子化合物
C.油脂在人体中发生水解生成氨基酸
D.糖类、蛋白质都能发生水解反应
难度: 中等查看答案及解析
-
下列有关物质分类或归纳正确的是 ( )
①混合物:盐酸、漂白粉、水玻璃、水银
②化合物:BaCl2、Ca(OH)2、HNO3、HT
③电解质:明矾、冰醋酸、氯化银、纯碱
④同素异形体:金刚石、石墨、C60、C70
A.①② B.②③ C.③④ D.②④
难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是 ( )
A.氯化铝溶液中加人过量的氨水:Al3+ +4NH3·H2O =AlO—2+4NH+4 +2H2O
B.碳酸氢钠溶液中加入少量澄清石灰水:Ca2+ +OH—+HCO—3===CaCO3↓+H2O
C.将氯气通人氯化亚铁溶液中:Fe2++Cl2==Fe3++2Cl—
D.氯气与水反应:H2O +Cl2===H++Cl—+HClO
难度: 中等查看答案及解析
-
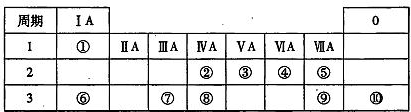
X、Y为短周期元素,X位于IA主族,X、Y可形成化合物X2Y。下列说法不正确的是( )
A.两元素形成的化合物中原子个数比可能为l:1
B.X的原子半径一定大于Y的原子半径
C.X、Y的简单离子可能具有相同的电子层结构
D.X2Y可能是离子化合物,也可能是共价化合物
难度: 中等查看答案及解析
-
向FeCl3和BaCl2的混合溶液中通入SO2气体,溶液颜色由棕黄色变为浅绿色,同时有白色沉淀产生。下列说法正确的是 ( )
A.该实验表明FeCl3有还原性 B.白色沉淀为BaSO3
C.该实验表明SO2有漂白性 D.反应后溶液酸性增强
难度: 中等查看答案及解析
-
设NA表示阿伏加德罗常数的数值。下列说法正确的是 ( )
A.1 L 1 mol/L CH3COONa溶液中存在NA个CH3COO—
B.22.4 L N2和O2的混合气体中所含原子数一定为2NA
C.1 mol CnH2n+2含有(3 n+1)NA个共价键
D.1 mol NO2气体降温后颜色变浅,其所含的分子数仍为NA
难度: 中等查看答案及解析
-
为了除去下列括号中的杂质,所用试剂和操作方法都正确的是 ( )
A.CO2(SO2):饱和Na2CO3溶液,洗气
B.乙酸乙酯(乙酸):乙醇和浓硫酸,加热
C.水(碘):酒精,萃取、分液
D.铜粉(铁粉):稀盐酸,过滤、洗涤、干燥
难度: 中等查看答案及解析
-
下列关于铝合金的说法中错误的是 ( )
A.镁铝合金在冷的浓H2SO4中钝化
B.镁铝合金抗氧化,但能被烧碱腐蚀
C.镁铝合金是一种混合物,它比纯铝的熔点低
D.高温铝液易被氧化,铝合金应在熔剂层覆盖下熔炼
难度: 中等查看答案及解析
-
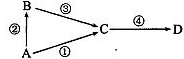
某反应体系的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。
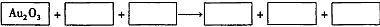
下列选项正确的是 ( )
A.框图中的物质分别为:Na2S4O6、H2O、Na2S2O3、Au2O、NaOH
B.框图中的物质分别为:Na2S2O3、NaOH、Na2S4O6、Au2O、H2O
C.框图中的物质分别为:Na2S2O3、H2O、Na2S4O6、Au2O、NaOH
D.当1 mol Au2O3完全反应时,转移电子的物质的量为6 mol
难度: 中等查看答案及解析
-
红磷(P)和Cl2发生反应生成PCl3和PCl5,反应过程和能量关系如下图所示,图中的△H表示生成1 mol产物的数据。已知PCl5分解为PCl3和Cl2是可逆反应。下列说法正确的是( )
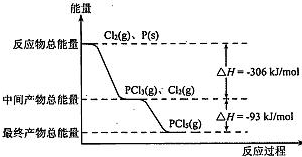
A.其他条件不变,升高温度有利于PCl5生成
B.反应2P(s)+5Cl2(g)===2PCl5(g)对应的反应热△H=-798 kJ/mol
C.P和Cl2反应生成PCl3的热化学方程式为2P(s)+3Cl2(g)=2PCl3(g)△H=-306 kJ/mol
D.其他条件不变,对于PCl5分解生成.PCl3和Cl2的反应,增大压强,PCl5的转化率减小,平衡常数K减小
难度: 中等查看答案及解析
-
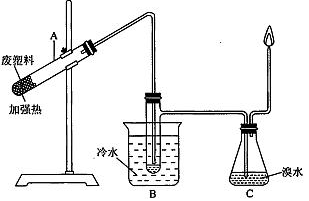
如图所示装置,将Cl2缓慢通人,若打开旋塞b,则小试管中干燥的
品红试纸c不褪色。再将b关闭,则c不久即褪色。由此判断a溶
液是( )
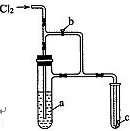
A.浓KI溶液 B.浓H2SO4
C.饱和食盐水 D.NaOH溶液
难度: 中等查看答案及解析
-
目前人类已发现的非金属元素除稀有气体外共有16种。下列对这16种非金属元素的相关判断不正确的是( )
①都是主族元素,最外层电子数都大于4; ②单质在化学反应中都只能作氧化剂;
③氢化物在常温下都是气体,所以又叫气态氢化物;④氧化物常温下都可以与水反应生成酸
A.①② B.①③ C.③④ D.①②③④
难度: 中等查看答案及解析
-
分子式为C7H16的烷烃中,含有3个甲基的同分异构体的数目( )
A.2 B.3 C.4 D.5
难度: 中等查看答案及解析
-
下列关于溶液和胶体的叙述,正确的是 ( )
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律
D.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
难度: 中等查看答案及解析
-
铁和氧化铁的混合物共a mol,加盐酸后固体全部溶解,共收集到氢气6 mol,且向反应后的溶液中加入KSCN溶液不显红色,则原混合物中单质铁的物质的量为( )
A.
mol B.(a-b)mol C.
mol D.(a+b)mol
难度: 中等查看答案及解析