-
如图表示的意义为:①道尔顿实心球式原子模型;②玻尔轨道式原子模型;③汤姆生葡萄干面包式原子模型;④卢瑟福行星运转式原子模型.其中符合历史演变顺序的一组排列是( )
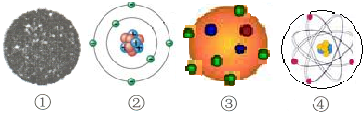
A.①②③④
B.③②①④
C.①③④②
D.①③②④难度: 中等查看答案及解析
-
化学概念在逻辑上存在如图所示关系,对下列概念间的关系说法正确的是( )
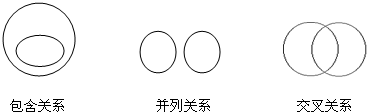
A.纯净物与混合物属于包含关系
B.化合物与电解质属于包含关系
C.单质与化合物属于交叉关系
D.氧化反应与化合反应属于并列关系难度: 中等查看答案及解析
-
下列说法不正确的是( )
A.胶体区别于浊液的本质特征是分散质微粒直径
B.电解质是在水溶液和熔融状态下都能导电的化合物
C.氢氧化铁胶体具有净水能力
D.区别胶体和溶液的简便方法是丁达尔现象难度: 中等查看答案及解析
-
人类探测月球发现,其土壤中存在较丰富的质量数为3的氦元素,它是核聚变的重要原料之一.在地球上,氦元素主要以24He的形式存在.以下关于23He的说法正确的是( )
A.是4He的同分异构体
B.与4He是同一种核素
C.与4He互为同位素
D.比4He少一个质子难度: 中等查看答案及解析
-
痕检是公安机关提取犯罪嫌疑人指纹的一种重要的方法,AgNO3显现法就是其中的一种:人的手上有汗渍,用手动过白纸后,手指纹线就留在纸上.如果将溶液①小心地涂到纸上,溶液①中的溶质就跟汗渍中的物质②作用,生成物质③,物质③在光照下,分解出的银粒呈灰褐色,随着反应的进行,银粒逐渐增多,由棕色变成黑色的指纹线.用下列化学式表示这3种物质都正确的是( )
A.①AgNO3②NaBr③AgBr
B.①AgNO3②NaCl③AgCl
C.①AgCl②AgNO3③NaCl
D.①AgNO3②NaI③AgI难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.磷酸的摩尔质量与NA个磷酸分子的质量在数值上相等
B.NA个氮分子和NA个氢分子的质量比等于14:1
C.32g氧气所含的原子数目为2NA
D.常温常压下,0.5NA一氧化碳分子所占体积是11.2L难度: 中等查看答案及解析
-
下列各组离子能大量共存的是( )
A.H+、Na+、HCO3-、Cl-
B.Fe3+、SCN-、Cl-、NO3-
C.Mg2+、Fe2+、SO42-、Cl-
D.Fe3+、SO42-、OH-、NO3-难度: 中等查看答案及解析
-
下列物质的用途不正确的是( )
A.硅是制造太阳能电池的常用材料
B.硅是制造光导纤维的主要材料
C.水玻璃可用作木材防火剂
D.碳化硅可做砂纸、砂轮的磨料难度: 中等查看答案及解析
-
下列实验装置(部分仪器已省略)或操作,不能达到相应实验目的是( )
A.干燥氯气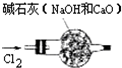
B.闻气体气味
C.分离四氯化碳和水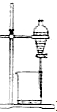
D.进行喷泉实验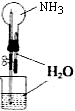
难度: 中等查看答案及解析
-
铝有较强的抗腐蚀性能,主要是因为( )
A.与氧气在常温下不反应
B.铝性质不活泼
C.铝表面形成了一层致密的氧化膜
D.铝耐酸耐碱难度: 中等查看答案及解析
-
为了验证碳酸氢钠固体中是否含有碳酸钠.下列实验及判断中,正确的是( )
A.加热,观察是否有气体放出
B.溶于水后加石灰水,看有无沉淀
C.取少量配成稀溶液滴加氯化钡溶液,看有无沉淀
D.加热后称量,看质量是否变化难度: 中等查看答案及解析
-
下列关于新制氯水和久置氯水的说法中不正确的是( )
A.新制氯水呈黄绿色,久置氯水无色
B.新制氯水漂白能力强,而久置的氯水几乎无漂白作用
C.新制的氯水所含微粒种类多,而久置氯水所含微粒种类少
D.新制的氯水中无氯离子,而久置的氯水中则含有氯离子难度: 中等查看答案及解析
-
现有硫酸钠、硫酸铝、硫酸镁三种无色的溶液,可用一种试剂将它们区别开来,该试剂是( )
A.纯水
B.盐酸
C.氢氧化钠溶液
D.硝酸银溶液难度: 中等查看答案及解析
-
由下列化学方程式改写的离子方程式正确的是( )
A.AlCl3+3NH3•H2O=Al(OH)3↓+3NH4Cl Al3++3OH-=Al(OH)3↓
B.BaCO3+2HCl=BaCl2+CO2↑+H2O CO32-+2H+=CO2↑+H2O
C.2NaOH+H2SO4=Na2SO4+2H2O H++OH-=H2O
D.(NH4)2SO4+Ba(OH)2=BaSO4↓+2NH3•H2O NH4++OH-=NH3•H2O难度: 中等查看答案及解析
-
在电子工业中,制作电路时,常用氯化铁溶液作为铜的腐蚀液,该过程发生的反应为:2FeCl3+Cu=2FeCl2+CuCl2.该反应利用了铜性质中的( )
A.氧化性
B.还原性
C.导电性
D.导热性难度: 中等查看答案及解析
-
下列有关离子的检验方法一定正确的是( )
A.向某溶液中滴加稀氯化钡溶液,以检验硫酸根离子的存在
B.向某溶液中滴加硝酸银溶液和稀硝酸,以检验氯离子的存在
C.向某溶液中滴加KSCN溶液,以检验Fe2+的存在
D.用铂丝蘸取某溶液在无色火焰上灼烧直接观察火焰颜色,以检验K+的存在难度: 中等查看答案及解析
-
具有漂白作用的物质有①氯气②二氧化硫③活性炭④过氧化钠,其漂白原理相同的是( )
A.①③
B.②③
C.①④
D.②④难度: 中等查看答案及解析
-
用98%的浓硫酸(密度为1.84g/cm3)配制100mL 1 mol/L的稀硫酸.现给出下列仪器(配制过程中可能用到):①100mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平 ⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒,按使用仪器的先后顺序排列正确的是( )
A.④③⑦⑤⑥
B.②⑤⑦⑥
C.①③⑤⑥⑦
D.②⑥③⑦⑤⑥难度: 中等查看答案及解析
-
55g铁、铝混合物与足量的盐酸反应,生成标准状况下的氢气44.8L,则混合物中铁和铝的物质的量之比为( )
A.1:1
B.1:2
C.2:1
D.1:3难度: 中等查看答案及解析
-
有关氨气的实验较多,下面对这些实验的实验原理分析中,不正确的是( )
A.氨气极易溶解于水的性质可以解释氨气的喷泉实验
B.氨气的溶解性和相对分子质量可以解释氨气的收集方法
C.铵盐的水溶性大是实验室中用NH4Cl和Ca(OH)2的混合物制取氨气的原因
D.NH3•H2O的热不稳定性可以解释实验室中用加热氨水的方法制取氨气难度: 中等查看答案及解析
-
下列说法中,正确的是( )
A.氧化还原反应一定有氧气参加
B.工业上制漂白粉,若有2molCl2参加反应,则转移电子的数目为4mol
C.Cl2与KBr反应中,KBr为氧化剂
D.判断氧化还原反应的方法是看反应中是否存在变价元素难度: 中等查看答案及解析
-
某混合气体中可能含有Cl2、O2、SO2、NO、NO2 中的两种或多种气体.现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色.对于原混合气体成分的判断中不正确的是( )
A.肯定只有NO
B.肯定没有Cl2、O2和NO2
C.肯定无Cl2和O2
D.肯定有SO2和NO难度: 中等查看答案及解析
-
将一定量Mg、Al合金溶于1mol•L-1的HCl溶液中,进而向所得溶液中滴加1mol•L-1的NaOH溶液,产生沉淀的物质的量(n)与滴加的NaOH溶液体积(mL)的图示如下.下列分析的结论中正确的是( )
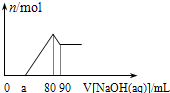
A.溶解“一定量Mg、Al合金”的HCl溶液的体积小于80mL
B.由题中数据,无法求出实验中产生H2的物质的量
C.无法确定Mg、Al合金中n(Mg)/n(Al)的最大值
D.欲求出a的取值范围尚缺少一个条件难度: 中等查看答案及解析
