-
酸雨是大气污染物之一,二氧化硫(SO2)的含量是空气质量监测的一个重要指标.某兴趣小组同学取刚降落在热电厂附近的雨水进行实验:
①测得该雨水样品的pH为4.73;
②向雨水样品中滴加BaCl2溶液,有白色沉淀生成;
③每隔1h,通过pH计测定雨水样品的pH,测得的结果如下表:
根据以上信息,回答下列问题:测定时间/h 1 2 3 4 雨水样品的pH 4.73 4.62 4.56 4.55 4.55
(1)正常雨水的pH为5.6,偏酸性,这是因为______.
(2)分析上述数据变化,你认为形成这一变化的原因是______.
(3)兴趣小组同学取某一时段的这种雨水V L,加入0.5mol•L-1的Ba(OH)2溶液至不再产生沉淀时,恰好消耗60.00mL Ba(OH)2溶液.
请计算:①该V L雨水中溶解SO2的体积(标准状况)
②生成沉淀物的质量范围(写出计算过程).高二化学解答题中等难度题查看答案及解析
-
酸雨是大气污染的危害之一,二氧化硫(SO2)的含量是空气质量监测的一个重要指标。某兴趣小组同学取刚降落在热电厂附近的雨水进行实验。
① 测得该雨水样品的pH为4.73;② 向雨水样品中滴加BaCl2溶液,有白色沉淀生成;③ 每隔1 h,通过pH计测定雨水样品的pH,测得的结果如下表:
测定时间/h
0
1
2
3
4
雨水样品的pH
4.73
4.62
4.56
4.55
4.55
根据以上信息,回答下列问题:
(1)正常雨水的pH为5.6,偏酸性,这是因为_________________________________。
(2)分析上述数据变化,你认为形成这一变化的原因是_____________________。
(3)兴趣小组同学取某一时段的这种雨水V L,加入0.5mol·L-1的Ba(OH)2溶液至不再产生沉淀时,恰好消耗40.00 mL Ba(OH)2溶液。请计算(列出计算过程):
① 该V L雨水中溶解SO2的体积(标准状况)为______________mL。
计算过程:
② 生成沉淀物的质量范围为________________________。计算过程:
高二化学填空题简单题查看答案及解析
-
酸雨是大气污染的危害之一,二氧化硫(SO2)的含量是空气质量监测的一个重要指标。某兴趣小组拟用下列装置定量分析空气中SO2的含量:

(1)该组同学查资料得到的反应原理为:SO2与酸性KMnO4溶液反应的离子方程式为5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+,SO2在该反应中是___________(填“氧化剂”或“还原剂”)。
(2)通入空气前应进行的实验操作是___________。
(3)该实验中已经知道的数据有气体流速a L/min、酸性KMnO4溶液的体积b L,其浓度为c mol/L。若从气体通入到紫色恰好褪去,用时5分钟。则此次取样处的空气中二氧化硫含量为____________g/L。(写出计算过程)
高二化学简答题困难题查看答案及解析
-
SO2 是危害最为严重的大气污染物之一,SO2 的含量是衡量大气污染的一个重要指标。工业上常采用催化还原法或吸收法处理 SO2。催化还原 SO2 不仅可以消除 SO2 污染,而且可得到有价值的单质S。
(1)在复合组分催化剂作用下,CH4 可使 SO2 转化为 S,同时生成 CO2 和 H2O。已知 CH4 和 S的燃烧热分别为 890.3 kJ /mol 和 297.2 kJ /mol , CH4 和 SO2 反应的热化学方程式为__________。
(2)用 H2 还原 SO2 生成S 的反应分两步完成,如图 1 所示,该过程中相关物质的物质的量浓度随时间的 变化关系如图 2 所示:
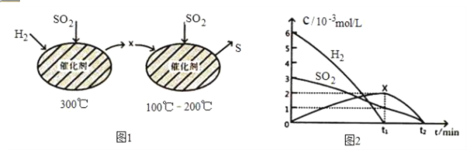
①分析可知X 为______写化学式),0~t1 时间段的温度为_____,0~t1 时间段用SO2 表示的化学反应速率为_____。
②总反应的化学方程式为____________。
高二化学综合题中等难度题查看答案及解析
-
SO2是危害最为严重的大气污染物之一,SO2的含量是衡量大气污染的一个重要指标。工业上常采用催化还原法或吸收法处理SO2。催化还原SO2不仅可以消除SO2污染,而且可得到有价值的单质S。
(1)在复合组分催化剂作用下,CH4可使SO2转化为S,同时生成CO2 和H2O。已知CH4 和S的燃烧热分别为890.3 kJ /mol 和297.2 kJ /mol,CH4和SO2反应的热化学方程式为______________________。
(2)用H2还原SO2生成S的反应分两步完成,如图1所示,该过程中相关物质的物质的量浓度随时间的变化关系如图2 所示:
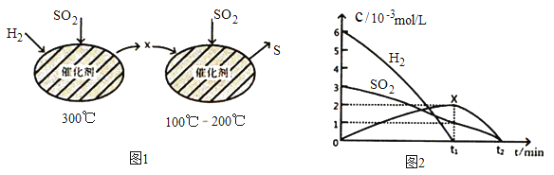
①分析可知X为____________(写化学式),0~t1时间段的温度为_________,0~t1时间段用SO2 表示的化学反应速率为________________________________。
②总反应的化学方程式为_______________________________。
(3)工业上可用Na2SO3溶液吸收SO2,该反应的离子方程式为__________________________,比较Na2SO3 溶液中各离子浓度的大小关系为__________________。
高二化学综合题困难题查看答案及解析
-
SO2是危害最为严重的大气污染物之一,SO2的含量是衡量大气污染的一个重要指标。工业上常采用催化还原法或吸收法处理SO2。催化还原SO2不仅可以消除SO2污染,而且可得到有价值的单质S。
(1)在复合组分催化剂作用下,CH4可使SO2转化为S,同时生成CO2 和H2O。已知CH4 和S的燃烧热分别为890.3 kJ /mol 和297.2 kJ /mol,CH4和SO2反应的热化学方程式为______________________。
(2)用H2还原SO2生成S的反应分两步完成,如图1所示,该过程中相关物质的物质的量浓度随时间的变化关系如图2 所示:
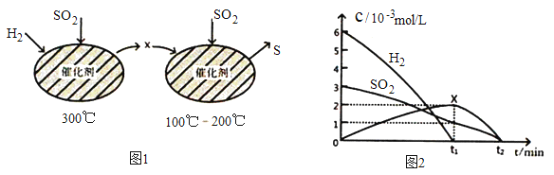
①分析可知X为____________(写化学式),0~t1时间段的温度为_________,0~t1时间段用SO2 表示的化学反应速率为________________________________。
②总反应的化学方程式为_______________________________。
(3)工业上可用Na2SO3溶液吸收SO2,该反应的离子方程式为__________________________,比较Na2SO3 溶液中各离子浓度的大小关系为__________________。
高二化学综合题困难题查看答案及解析
-
(10分)二氧化硫是造成大气污染的主要有害气体之一,某合作学习小组的同学拟测定某地大气中SO2的含量,实验步骤及装置如下:
步骤①:称取a g I2,(加少量KI助溶),配成1L 5×10-3mol·L-1溶液;
步骤②:取步骤①中溶液10mL,稀释至100mL;
步骤③:量取步骤②中溶液5.00mL于试管2中,加入2~3滴淀粉溶液;
步骤④:如图抽气N次至溶液蓝色刚好褪去。
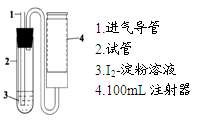
(1)步骤①中配制1L溶液时,除用到天平、药匙、烧杯、量筒、玻璃棒、胶头滴管外,还用到的玻璃仪器有 ;需称量单质碘的质量a为 (保留小数点后两位)。
(2)SO2与碘水反应的离子方程式为 。
(3)实验时,注射器每次缓缓抽气100mL。
①若抽气太快,将导致结果 (选填:“偏大”、“偏小”、“不变”)。
②若某次实验时抽气共80次,试计算该地空气中SO2的含量(mg/L) (写出计算过程)。
高二化学填空题困难题查看答案及解析
-
节日期间因燃放鞭炮会引起空气中SO2含量增高.造成大气污染。某实验小组同学欲探究SO2的性质,并测定空气中SO2的含量
(1)他们设计如下实验装置,请你参与探究并回答问题
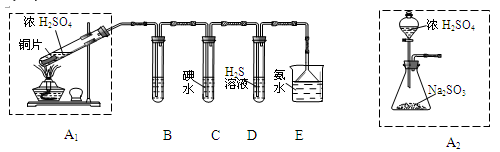
①装置A1中发生反应的化学方程式为________________________。
②装置B用于检验SO2的漂白性,其中所盛试剂为_________,装置D中实验现象为_______________。
③装置C中反应的离子方程式为___________________________________。
④为了实现绿色环保的目标。 甲同学欲用装置A2代替装置A1,你认为装置A2的优点是(写两点)________________________________________________________________。
(2)他们拟用以下方法测定空气中SO2含量(假设空气中无其他还原性气体)
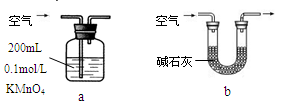
你认为哪个装置可行(填序号)__________,使用你所选用的装置测定SO2含量时,还需要测定的物理量是______________________________;不可行的请说明理由___________________________。
高二化学实验题困难题查看答案及解析
-
化学与环境密切相关,下列说法正确的是
A.CO2属于大气污染物
B.酸雨是pH小雨7的雨水
C.CO2、NO2或SO2都会导致酸雨的形成
D.大雾是一种胶体,能发生丁达尔效应
高二化学选择题简单题查看答案及解析
-
下列说法正确的是( )
①正常雨水的pH为7.0,酸雨的pH小于7.0
②严格执行机动车尾气排放标准有利于防止大气污染
③使用二氧化硫和某些含硫化合物进行增白的食品会对人体健康产生损害
④使用氯气对自来水消毒过程中,生成的有机氯化物可能对人体有害
⑤食品厂产生的含丰富氮、磷营养素的废水可长期排向水库养鱼
A.①②③ B.①④⑤ C.②③④ D.③④⑤
高二化学选择题中等难度题查看答案及解析