-
NA代表阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,1mol P4中所含P-P键数目为4NA
B.100mL 1mol·L−1FeCl3溶液中所含Fe3+的数目为0.1NA
C.标准状况下,11.2L甲烷和乙烯混合物中含氢原子数目为4NA
D.0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2NA
高二化学单选题困难题查看答案及解析
-
验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
①
②
③
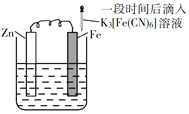
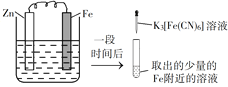
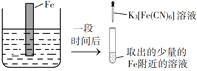
在Fe表面生成蓝色沉淀
试管内无明显变化
试管内生成蓝色沉淀
下列说法不正确的是
A.对比②③,可以判定Zn保护了Fe
B.对比①②,K3[Fe(CN)6]可能将Fe氧化
C.验证Zn保护Fe时不能用①的方法
D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼
高二化学单选题困难题查看答案及解析
-
在密闭容器中,对于可逆反应:A(?)+3B(?)
 2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是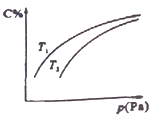
A.若正反应方向△H<0,则T1>T2 B.压强增大时,混合气体的平均相对分子质量减小
C.A一定为气体 D.B一定为气体
高二化学单选题困难题查看答案及解析
-
工业以铬铁矿(主要成分为FeO和Cr2O3,含有Al2O3、SiO2等杂质)为原料冶炼铬及获得化工原料红矾钠(Na2Cr2O7·2H2O),工艺流程如图:
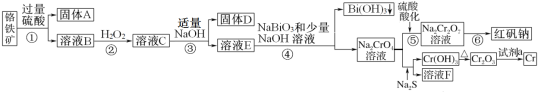
已知:常温下NaBiO3不溶于水,有强氧化性,在碱性条件下能将Cr3+转化为
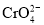 。
。(1)反应之前先将矿石粉碎的目的是________,固体D的主要成分为________。
(2)写出反应④的离子方程式________。
(3)步骤⑤中不能用盐酸代替硫酸的原因是________;将Na2Cr2O7溶液经过________,过滤,洗涤,干燥即得红矾钠粗晶体。
(4)工业上常用电解铬酐(CrO3,遇水生成H2Cr2O7和H2CrO4)水溶液的方法镀铬,电镀液中需加入适量的催化剂和添加剂,并通过加入H2O2提高或降低电镀液中Cr(Ⅲ)的含量,发生的部分反应有:
a.2H++2e-=H2
b.2H2O−4e-=O2+4H+
c.2
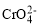 +2H+⇌
+2H+⇌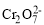 +H2O
+H2Od.
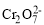 +14H++6e−=2Cr3++7H2O
+14H++6e−=2Cr3++7H2Oe.2Cr3++7H2O−6e-=
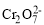 +14H+
+14H+①镀件上发生的反应有________(填上述序号)
②电极上
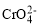 放电生成铬的电极反应式为________。
放电生成铬的电极反应式为________。③镀铬过程中H2O2体现的化学性质________。
A.仅氧化性 B.仅还原性 C.氧化性和还原性
高二化学工业流程题困难题查看答案及解析
-
锰酸锂(LiMn2O4)是最早制得的具有三维锂离子通道的正极材料。以MnSO4和LiFePO4为原料制备锰酸锂的流程如图:
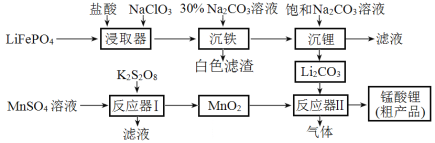
下列说法错误的是
A.NaClO3的作用是将二价铁氧化为三价铁
B.“沉铁”过程所得滤渣的主要成分是FePO4
C.反应器Ⅱ中产生的气体是CO2
D.已知K2S2O8中S的化合价为+6价,则
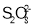 中存在“—O—O—”键
中存在“—O—O—”键高二化学单选题困难题查看答案及解析
-
我国科学家研制一种新型化学电池成功实现废气的处理和能源的利用,用该新型电池电解CuSO4溶液,装置如下(H2R和R都是有机物)。下列说法正确的是
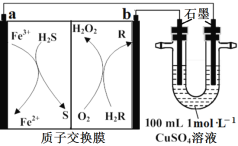
A.b电极反应式为R+2H++2e-=H2R
B.电池工作时,负极区要保持呈酸性
C.工作一段时间后,正极区的pH变大
D.若消耗标准状况下112mLO2,则电解后的CuSO4溶液pH约为2
高二化学多选题困难题查看答案及解析
-
用一定浓度NaOH溶液滴定某一元酸HA溶液。滴定终点附近溶液pH和导电能力的变化分别如图所示。下列说法正确的是
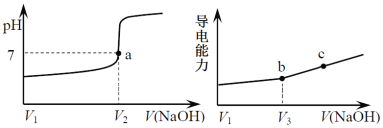
A.HA为一元弱酸
B.b点对应的溶液中:c(A-)>c(Na+)
C.根据溶液pH和导电能力的变化可判断V2<V3
D.a、b、c三点对应的溶液中水的电离程度依次减小
高二化学多选题困难题查看答案及解析
-
下列关于溶液的说法中错误的是
A.常温下,NH4Cl溶液加水稀释后,n(H+)与n(OH-)的乘积变大
B.NaF和氢氟酸的混合液中存在:c(Na+)>c(F-)>c(H+)>c(OH-)
C.25℃测得0.1mol·L-1醋酸钠溶液pH=8.9,说明醋酸是弱电解质
D.0.1mol·L-1Na2CO3溶液与0.1mol·L-1NaHCO3溶液等体积混合:c(
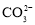 )+c(OH-)=c(H2CO3)+c(H+)+0.05mol·L-1
)+c(OH-)=c(H2CO3)+c(H+)+0.05mol·L-1高二化学单选题困难题查看答案及解析
-
Fe、Co、Ni均为第Ⅷ族元素,它们的化合物在生产生活中有着广泛的应用。
(1)基态Co原子的价电子排布式为____________
(2)已知HN3是一种弱酸,其在水溶液中的电离方程式为HN3
 H++N3-,与N3-互为等电子体的一种分子为:_______,N3-离子杂化类型为___________。
H++N3-,与N3-互为等电子体的一种分子为:_______,N3-离子杂化类型为___________。(3)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+ 的配位数是___________,1mol该配离子中所含σ键的数目为____,配位体NH3的空间构型为:___________ 。
(4)某蓝色晶体中,Fe2+、Fe3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个CN-,K+位于立方体的某恰当位置上。据此可知该晶体的化学式为____________,立方体中Fe2+间连接起来形成的空间构型是_____________。
(5)NiO的晶体结构如下图所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为_______________。
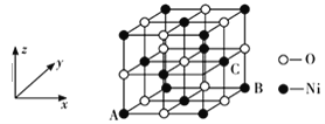
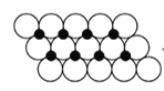
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如下图),已知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为__________g(用含a、NA的代数式表示)。
高二化学填空题困难题查看答案及解析
-
25℃时,几种弱酸的电离常数如下,下列说法正确的是
弱酸
CH3COOH
H2SO3
H2CO3
电离常数(25℃)
1. 8×10-5
K1=1.5×10-2
K2=1.0×10-7
K1=4.3×10-7
K2=5.6×10-11
A.物质的量浓度相同的CH3COONa、NaHSO3、NaHCO3三种溶液中,pH顺序为NaHCO3>CH3COONa>NaHSO3
B.将NaHCO3溶液与NaHSO3溶液混合可以发生化学反应
C.常温下,加水稀释醋酸,
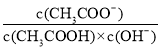 增大
增大D.Na2CO3溶液中一定存在c(Na+)=2[c(
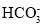 )]+c(
)]+c(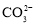 )]
)]高二化学单选题困难题查看答案及解析