验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
| ① | ② | ③ |
|
|
|
|
| 在Fe表面生成蓝色沉淀 | 试管内无明显变化 | 试管内生成蓝色沉淀 |
下列说法不正确的是
A.对比②③,可以判定Zn保护了Fe
B.对比①②,K3[Fe(CN)6]可能将Fe氧化
C.验证Zn保护Fe时不能用①的方法
D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼
高二化学单选题困难题
验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
| ① | ② | ③ |
|
|
|
|
| 在Fe表面生成蓝色沉淀 | 试管内无明显变化 | 试管内生成蓝色沉淀 |
下列说法不正确的是
A.对比②③,可以判定Zn保护了Fe
B.对比①②,K3[Fe(CN)6]可能将Fe氧化
C.验证Zn保护Fe时不能用①的方法
D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼
高二化学单选题困难题
验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
| ① | ② | ③ |
|
|
|
|
| 在Fe表面生成蓝色沉淀 | 试管内无明显变化 | 试管内生成蓝色沉淀 |
下列说法不正确的是
A.对比②③,可以判定Zn保护了Fe
B.对比①②,K3[Fe(CN)6]可能将Fe氧化
C.验证Zn保护Fe时不能用①的方法
D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼
高二化学单选题困难题查看答案及解析
验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
| ① | ② | ③ |
|
|
|
|
| 在Fe表面生成蓝色沉淀 | 试管内无明显变化 | 试管内生成蓝色沉淀 |
下列说法不正确的是
A. 对比②③,可以判定Zn保护了Fe
B. 对比①②,K3[Fe(CN)6]可能将Fe氧化
C. 验证Zn保护Fe时不能用①的方法
D. 将Zn换成Cu,用①的方法可判断Fe比Cu活泼
高二化学单选题困难题查看答案及解析
如图是金属牺牲阳极的阴极保护法的实验装置,有关说法正确的是
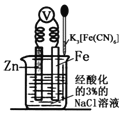
A. 若加入K3[Fe(CN)6]溶液后,Fe电极附近不会产生特征蓝色的沉淀
B. 本实验牺牲了金属Fe来保护金属Zn
C. 该装置为电解池
D. 远洋货轮上镶嵌的金属Zn长时间没有什么变化,不需要更换
高二化学单选题中等难度题查看答案及解析
利用右图装置,完成很多电化学实验。下列有关此装置的叙述中,不正确的是
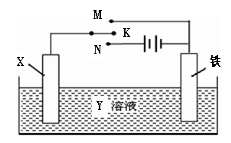
A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阳离子向铁电极移动
C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小
高二化学选择题困难题查看答案及解析
利用如图装置,完成很多电化学实验。下列有关此装置的叙述中,不正确的是
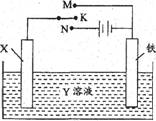
A、若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
B、若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阳离子向铁电极移动
C、若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D、若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小
高二化学选择题简单题查看答案及解析
利用图装置,可以完成很多电化实验。下列有关此装置的叙述中,不正确的是( )
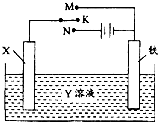
A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阳离子向铁电极移动
C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小
高二化学选择题中等难度题查看答案及解析
利用下图装置,能完成很多电化学实验。下列有关此装置的叙述中,错误
的是:( )
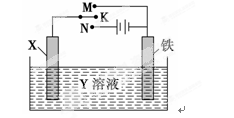
A、若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
B、若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,这种方法称为外加电流的阴极保护法
C、若X为铜棒,Y为硫酸铜溶液,开关K置于M处时,铁电极上的电极反应式为Cu2++2e-===Cu
D、若X为铜棒,Y为硫酸铜溶液,开关K置于N处时,溶液中各离子浓度都不会发生变化
高二化学选择题困难题查看答案及解析
下列图示装置和对应实验原理的描述均正确的是
| A | B | C | D |
|
|
|
|
|
| 根据温度计读数的变化测定浓硫酸和NaOH溶液反应的反应热 | 加热固体NaHCO3制备少量的Na2CO3 | 验证牺牲阳极的阴极保护法,可证明铁被保护 | 根据小试管中液面的变化可判断铁钉发生了析氢腐蚀 |
A. A B. B C. C D. D
高二化学单选题中等难度题查看答案及解析
(12分)
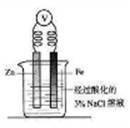
1.下图为牺牲阳极的阴极保护法的实验装置,此装置 中Zn电极上的电极反应为;如果将Zn换成Pt,一段时间后,在铁电极区滴入2滴黄色K3[Fe(CN)6](铁氰化钾)溶液时,烧杯中的现象是________,发生的反应的离子方程式是________。
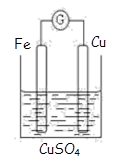
2.CuI是一种不溶于水的白色固体,它可以由反应:2Cu2+ + 4I- = 2CuI↓ + I2而得到。现以石墨为阴极,以Cu为阳极电解KI溶液,通电前向电解液中加入少量酚酞和淀粉溶液。①电解开始不久,阴极产生的实验现象有________,阴极的电极反应是________。
②阳极区溶液变蓝色,同时伴随的现象还有________,对阳极区溶液
呈蓝色的正确解释是________。
A. 2I- - 2e- = I2 ;碘遇淀粉变蓝
B. Cu - 2e- = Cu2+;Cu2+显蓝色
C. 2Cu + 4I-- 4e- = 2CuI↓ + I2; 碘遇淀粉变蓝
D. 4OH-- 4e- = 2H2O + O2 ;O2将I-氧化为I2,碘遇淀粉变蓝
高二化学填空题简单题查看答案及解析
下列关于金属的腐蚀与防护的说法正确的是( )
A. 金属发生吸氧腐蚀时,被腐蚀的速率与氧气浓度无关
B. 验证铁的吸氧腐蚀,可以将铁钉放入试管中,用盐酸浸没
C. 钢铁水闸可用牺牲阳极或外加电流的阴极保护法防止其腐蚀
D. 钢铁发生析氢腐蚀时,负极反应Fe-3e-= Fe3+
高二化学选择题中等难度题查看答案及解析