如图是金属牺牲阳极的阴极保护法的实验装置,有关说法正确的是
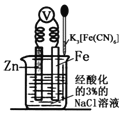
A. 若加入K3[Fe(CN)6]溶液后,Fe电极附近不会产生特征蓝色的沉淀
B. 本实验牺牲了金属Fe来保护金属Zn
C. 该装置为电解池
D. 远洋货轮上镶嵌的金属Zn长时间没有什么变化,不需要更换
高二化学单选题中等难度题
如图是金属牺牲阳极的阴极保护法的实验装置,有关说法正确的是

A. 若加入K3[Fe(CN)6]溶液后,Fe电极附近不会产生特征蓝色的沉淀
B. 本实验牺牲了金属Fe来保护金属Zn
C. 该装置为电解池
D. 远洋货轮上镶嵌的金属Zn长时间没有什么变化,不需要更换
高二化学单选题中等难度题
如图是金属牺牲阳极的阴极保护法的实验装置,有关说法正确的是

A. 若加入K3[Fe(CN)6]溶液后,Fe电极附近不会产生特征蓝色的沉淀
B. 本实验牺牲了金属Fe来保护金属Zn
C. 该装置为电解池
D. 远洋货轮上镶嵌的金属Zn长时间没有什么变化,不需要更换
高二化学单选题中等难度题查看答案及解析
下列图示内容的对应说明正确的是
| 编号 | A | B | C | D |
| 图示 |
食盐水 |
片刻后在Fe 电极附近滴入K3[Fe(CN)6]溶液 |
|
|
| 说明 | 验证铁钉发生 吸氧腐蚀 | 验证 Fe 电极被保护 | 该装置是牺牲阳极的阴极保护法 | 该化学反应为放热反应 |
A.A B.B C.C D.D
高二化学单选题困难题查看答案及解析
(12分)
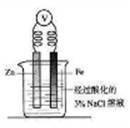
1.下图为牺牲阳极的阴极保护法的实验装置,此装置 中Zn电极上的电极反应为;如果将Zn换成Pt,一段时间后,在铁电极区滴入2滴黄色K3[Fe(CN)6](铁氰化钾)溶液时,烧杯中的现象是________,发生的反应的离子方程式是________。
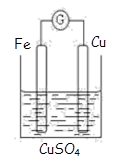
2.CuI是一种不溶于水的白色固体,它可以由反应:2Cu2+ + 4I- = 2CuI↓ + I2而得到。现以石墨为阴极,以Cu为阳极电解KI溶液,通电前向电解液中加入少量酚酞和淀粉溶液。①电解开始不久,阴极产生的实验现象有________,阴极的电极反应是________。
②阳极区溶液变蓝色,同时伴随的现象还有________,对阳极区溶液
呈蓝色的正确解释是________。
A. 2I- - 2e- = I2 ;碘遇淀粉变蓝
B. Cu - 2e- = Cu2+;Cu2+显蓝色
C. 2Cu + 4I-- 4e- = 2CuI↓ + I2; 碘遇淀粉变蓝
D. 4OH-- 4e- = 2H2O + O2 ;O2将I-氧化为I2,碘遇淀粉变蓝
高二化学填空题简单题查看答案及解析
用如图装置研究电化学原理,下列分析中错误的是
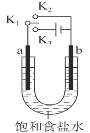
| 选项 | 连接 | 电极材料 | 分析 | |
| a | b | |||
| A | K1K2 | 石墨 | 铁 | 模拟铁的吸氧腐蚀 |
| B | K1K2 | 锌 | 铁 | 模拟钢铁防护中牺牲阳极的阴极保护法 |
| C | K1K3 | 石墨 | 铁 | 模拟电解饱和食盐水 |
| D | K1K3 | 铁 | 石墨 | 模拟钢铁防护中外加电流的阴极保护法 |
A.A B.B C.C D.D
高二化学单选题中等难度题查看答案及解析
下列有关电化学装置的说法正确的是

A. 图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀
B. 图c中的X极若为负极,则该装置可实现粗铜的精炼
C. 图b电解一段时间,铜电极溶解,石墨电极上有亮红色物质析出
D. 利用图a装置处理银器表面的黑斑Ag2S,银器表面发生的反应为Ag2S+2e-= 2Ag+S2-
高二化学单选题中等难度题查看答案及解析
结合下图判断,下列叙述正确的是
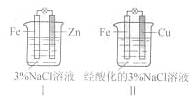
A.Ⅰ是验证牺牲阳极的阴极保护法的实验装置
B. Ⅰ和Ⅱ中负极反应均是Fe-2e-=Fe2+
C. Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e-=4OH-
D. Ⅰ和Ⅱ中分别加入少量K3Fe(CN)6溶液,均有蓝色沉淀
高二化学选择题简单题查看答案及解析
下列说法错误的是
A. 在日常生活中,化学腐蚀是造成钢铁腐蚀的主要原因
B. 人们常采用牺牲阳极的阴极保护法防止金属腐蚀
C. 在电镀槽中,一般镀件做阴极,阳极选用镀层金属
D. 用惰性电极电解某硫酸铜溶液一段时间后,加入一定量的氧化铜可能会恢复原溶液的成分和浓度
高二化学单选题简单题查看答案及解析
下列有关金属腐蚀与防护的说法正确的是( )
A.铜铁接触处,在潮湿的空气中直接发生反应: Fe-3e-=Fe3+,继而形成铁锈
B.轮船的船壳水线以下常装有一些锌块,这是利用了牺牲阳极的阴极保护法
C.金属腐蚀的实质是金属失去电子被还原的过程
D.在酸性环境下,钢铁只能发生析氢腐蚀
高二化学单选题中等难度题查看答案及解析
下列关于电化学的叙述正确的是

A.图①两极均有气泡产生,滴加酚酞溶液时石墨一极变红
B.图②装置可以验证牺牲阳极的阴极保护法
C.图③可以模拟钢铁的吸氧腐蚀,碳棒一极的电极反应式:O2+2H2O+4e-=4OH-
D.分别给上述4个装置的铁电极附近滴加少量K3[Fe(CN)6]溶液,②④出现蓝色沉淀
高二化学单选题中等难度题查看答案及解析
下列有关金属腐蚀与防护的说法正确的是( )
A. 铜铁接触处,在潮湿的空气中直接发生反应: Fe-3e-=Fe3+,继而形成铁锈
B. 轮船的船壳水线以下常装有一些锌块,这是利用了牺牲阳极的阴极保护法
C. 金属腐蚀的实质是金属失去电子被还原的过程
D. 在酸性环境下,钢铁只能发生析氢腐蚀
高二化学单选题中等难度题查看答案及解析