-
痕检是公安机关提取犯罪嫌疑人指纹的一种重要的方法,AgNO3显现法就是其中的一种:人的手上有汗渍,用手动过白纸后,手指纹线就留在纸上.如果将溶液①小心地涂到纸上,溶液①中的溶质就跟汗渍中的物质②作用,生成物质③,物质③在光照下,分解出的银粒呈灰褐色,随着反应的进行,银粒逐渐增多,由棕色变成黑色的指纹线.用下列化学式表示这3种物质都正确的是( )
A.①AgNO3②NaBr③AgBr
B.①AgNO3②NaCl③AgCl
C.①AgCl②AgNO3③NaCl
D.①AgNO3②NaI③AgI高二化学选择题中等难度题查看答案及解析
-
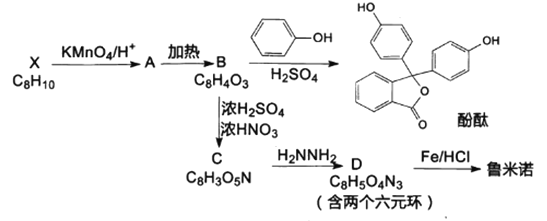
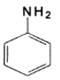
鲁米诺又名发光氨,是一种在犯罪现场检验肉眼无法观察到的血液,可以显现出极微量的血迹形态的重要刑侦用有机物。有机物B是一种常用工业原料,俗称苯酐,以其为原料可以合成酚酞、鲁米诺等物质。有机化合物C的苯环上有三个相邻的基团。
已知:①
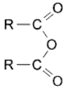 +R’NH2
+R’NH2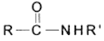 +RCOOH
+RCOOH②
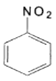
请回答以下问题:
(1)关于酚酞的下列说法,正确的是___________
A.酚酞的分子式为C20H14O4
B.酚酞遇FeCl3溶液显紫色
C.1mo1酚酞最多可与4 molNaOH反应
D.酚酞中有三种官能团
(2)请写出下列化合物的结构简式:有机物B___________;鲁米诺___________。
(3)请写出C—D的方程式_________________________________。
(4)有机物G的分子式为C9H8O4,它是有机物A的最简单的同系物,请写出符合下列要求的G的所有同分异构体的结构简式______________________
a.含有羧基和酯基官能团 b.苯环上有两个对位取代基
(5)设计以邻甲基苯甲酸为原料合成
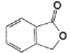 的流程图(无机试剂任选)_________________。
的流程图(无机试剂任选)_________________。高二化学推断题中等难度题查看答案及解析
-
(1)空气质量报告的各项指标可以反映出各地的空气质量。
①下列各项中目前未列入我国空气质量报告的是__________(填字母)。
a.SO2 b.NO2 c.CO2 d.PM2.5
②近日,公安机关成功破获了一起特大利用“地沟油”制售食用油案件。综合利用“地沟油”的一种方法,通常将“地沟油”进行简单加工提纯后,水解分离可获取________和_________ (填名称)。
(2)人体健康与食品、药物等关系密切。
①合理搭配饮食是我们的健康理念。比如早餐搭配:牛奶、面包、黄油、水果等,其中含有的营养素有油脂、糖类、___________、____________、无机盐和水。
②生活中应合理地摄取人体必需的元素,体内__________元素含量过高或过低,会引起甲状腺疾病;当人体内缺钙时,可能患有的疾病是__________(填字母)。
a.贫血 b.骨质疏松 c.夜盲症
③氢氧化铝可以用来治疗胃酸过多,请写出该反应的离子方程式:________________________。
④青霉素可用于__________(填字母)。
a.解热镇痛 b.止咳平喘 c.胃酸过多 d.抗菌消炎
(3)材料是人类赖以生存和发展的重要物质基础。
①在下列材料中,属于有机高分子材料的是__________ (填字母,下同);属于复合材料的是______。
a.硬币 b.聚氯乙烯塑料 c.氮化硅陶瓷 d.玻璃钢
②硅酸盐水泥是常用的建筑材料,它主要是以__________和黏土为原料制成。
③钢铁在潮湿的空气中主要发生的电化学腐蚀是_______腐蚀,其正极电极反应式为_________________;通常用钝化、涂漆、电镀筝方法来防止腐蚀。
高二化学填空题中等难度题查看答案及解析
-
海洋是生命的摇篮,海水不仅是宝贵的水资源,而且蕴藏着丰富的化学资源。从海水中提取一些重要的化工产品的工艺流程如图所示。
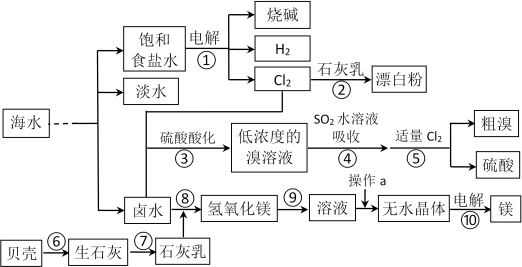
根据上述流程图回答下列问题:
(1)海水淡化处理的方法有蒸馏法、冷冻法、_____________。(写出1种即可)
(2)写出反应①化学反应方程式_______________________________________。
(3)标准状况下22.4 L Cl2气体发生反应②,转移的电子数是________NA。
(4)反应③中硫酸酸化可提高Cl2的利用率,理由是____________________________。
(5)过程③到过程⑤的变化为“Br-→Br2→Br-→Br2”,其目的是_______________。
(6)浓缩氯化镁溶液后冷却可以得到MgCl2﹒6H2O,该晶体受热时会发生如下变化:MgCl2﹒6H2O== Mg(OH)Cl + HCl↑+ 5H2O。则,从溶液制备无水晶体的“操作a”可以采取的措施是__________________________________________。
高二化学简答题中等难度题查看答案及解析
-
(10分)在课外实验中,某学生用蔗糖、碳铵、生石灰、硫酸四种药品,从AgNO3(内含少量Fe3+和Al3+),废液中提取单质银,其流程图如下图所示:
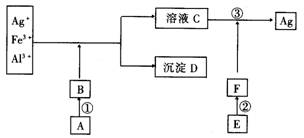
(1)写出沉淀D的成分____________,A的成分____________
(2)写出反应②的化学方程式:________________________________
(3)写出生成C的离子方程式:________________________________
(4)写出③的离子方程式________________________________
高二化学填空题简单题查看答案及解析
-
(18分)邻苯二甲酸二乙酯
 是一种重要的工业塑化剂,其合成路线很多,下图就是其中的一种合成方法:
是一种重要的工业塑化剂,其合成路线很多,下图就是其中的一种合成方法:
已知以下信息:
①有机化合物A可用来催熟水果。
②有机化合物C的核磁共振氢谱显示其有3种不同化学环境的氢原子。
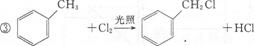
(1)A的结构简式是_________,B的化学名称为__________。
(2) 反应Ⅱ的试剂是________,该反应类型为__________。
(3)C生成D的化学方程式为__________________。
(4)G和B的化学方程式为_______________________。
(5)在G的同分异构体中,
A.能与新制的Cu(OH)2悬浊液在加热条件下反应生成砖红色沉淀
B.能与碳酸钠反应生成二氧化碳
C.能使FeCl3溶液显色
满足上述三个条件的同分异构体有_____种,写出符合上述条件的物质可能的结构简式(只写一种)________,每种同分异构体中,化学环境不同的氢原子都是______种。
高二化学实验题简单题查看答案及解析
-
(共14分)实现 “节能减排” 和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:
CO2(g)+3H2(g)
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
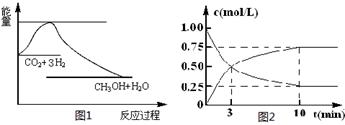
(1)关于该反应的下列说法中,正确的是____________(填字母)。
A.DH>0,DS>0 B.DH>0,DS<0 C.DH<0,DS<0 D.DH<0,DS>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
①从反应开始到平衡,CH3OH的平均反应速率v(CH3OH) =________ mol·(L·min)-1;
H2的转化率w(H2) =________
②该反应的平衡常数表达式K= ________________
③下列措施中能使化学平衡向正反应方向移动的是________ (填字母)。
A.升高温度 B.将CH3OH(g)及时液化抽出
C.选择高效催化剂 D.再充入l molCO2和3 molH2
(3)25℃,1.01×105Pa时,16g 液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出表示CH3OH燃烧热的热化学方程式:________
(4)选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此电池的负极电极反应式________
高二化学填空题简单题查看答案及解析
-
(12分)实现 “节能减排” 和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:
CO2(g)+3H2(g)
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
(1)关于该反应的下列说法中,正确的是____________(填字母)。
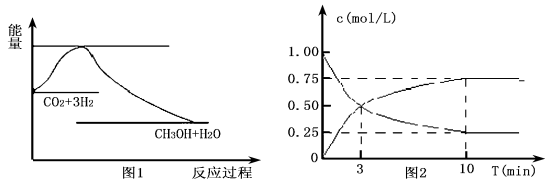
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和4mol H2,一定条件下发生反应:CO2(g)+3H2(g)
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2) = ;H2的转化率w(H2) = 。
②该反应的平衡常数表达式K= 。
③下列措施中能使化学平衡向正反应方向移动的是 (填字母)。
A.升高温度
B.将CH3OH(g)及时液化抽出
C.选择高效催化剂
D.再充入l molCO2和4 molH2
(3)25℃,1.01×105Pa时,16g 液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出该反应的热化学方程式: 。
高二化学填空题困难题查看答案及解析
-
(15分)实现 “节能减排” 和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化。
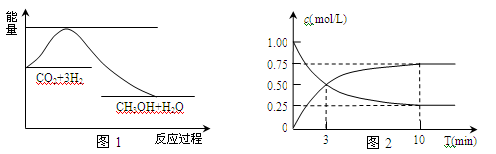
(1)关于该反应的下列说法中,正确的是_________(填字母)。
A.ΔH<0,ΔS<0 B.ΔH>0,ΔS<0
C.ΔH>0,ΔS>0 D.ΔH<0,ΔS>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和4 mol H2,一定条件下发生反应:CO2(g)+3H2(g)
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
①从反应开始到平衡,H2的平均反应速率v(H2)= ;CO2的转化率w(CO2)= 。
②该反应的平衡常数K= 。(只列表达式和计算式,不必计算出结果)
③下列措施中能使化学平衡向正反应方向移动的是 (填字母)。
A.将CH3OH(g)及时液化抽出 B.升高温度
C.选择高效催化剂 D.再充入l molCO2和4 molH2
(3)25℃,1.01×105Pa时,16 g 液态甲醇完全燃烧,当恢复到原状态时,放出350.8kJ的热量,写出该反应的热化学方程式: 。
(4)选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,其负极的电极反应式是: 。
高二化学填空题困难题查看答案及解析
-
实现 “节能减排” 和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:
CO2(g)+3H2(g)
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
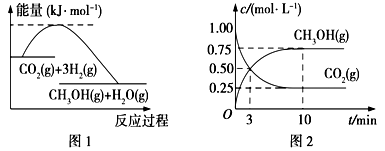
(1)关于该反应的下列说法中,正确的是____________(填字母)。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和4mol H2,一定条件下发生反应:CO2(g)+3H2(g)
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=_________;
②下列措施中能使化学平衡向正反应方向移动的是___________(填字母)。
A.升高温度B.将CH3OH(g)及时液化抽出C.选择高效催化剂D.再充入l molCO2和4 molH2
(3)25℃,1.01×105Pa时,16g 液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出该反应的热化学方程式:_____________。
(4)选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此电池的负极的电极反应式是:______________。
高二化学简答题中等难度题查看答案及解析