-
已知某可逆反应:2M(g)
N(g) △H<0。现将M和N的混和气体通入容积为l L的恒温密闭容器中,反应体系中各物质浓度随时间变化关系如图所示。下列说法中,正确的是
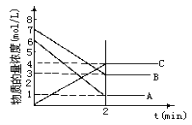
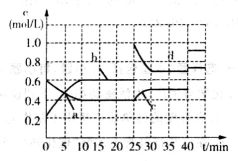
A.a、b、c、d四个点中处于平衡状态的点是a、b
B.反应进行至25 min时,曲线发生变化的原因是加入了0.4 mol N
C.若调节温度使35 min时体系内N的体积分数与15 min时相等,应升高温度
D.若在40 min时出现如图所示变化,则可能是因为加入催化剂引起的
高二化学选择题极难题查看答案及解析
-
现有200 mL含KNO3和Cu(NO3)2的混合溶液,其中c(NO3- )=3 mol·L-l,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2. 24 L气体(标准状况)。假定电解后溶液体积仍为200 mL),下列说法不正确的是( )
A.电解过程中共转移0.4 mol电子 B.原混合液中c(K+)为2.0 mol·L-l
C.电解得到的Cu的质量为6.4 g D.电解后溶液中c(H+)为0.1 mol·L-l
高二化学选择题极难题查看答案及解析
-
图Ⅰ是NO2(g)+CO(g)
CO2(g)+NO(g)反应过程中能量变化示意图.一定条件下,在固定容积的密闭容器中该反应达到平衡状态.当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ,下列有关说法正确的是
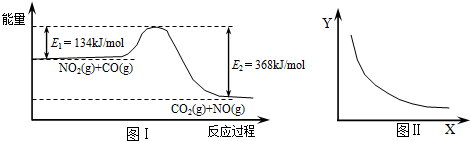
A.一定条件下,向密闭容器中加入1molNO2(g)与1molCO(g)反应放出234 kJ热量
B.若X表示CO的起始浓度,则Y表示的可能是NO2的转化率
C.若X表示反应时间,则Y表示的可能是混合气体的密度
D.若X表示温度则Y表示的可能是CO2物质的量浓度
高二化学选择题极难题查看答案及解析
-
一定条件下,在体积为10L的固定容器中发生的反应:N2+3H2
2NH3,反应过程如下图所示,下列说法正确的是
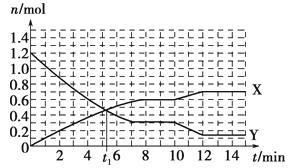
A.t1 min时正、逆反应速率相等
B.X曲线表示NH3的物质的量随时间变化的关系
C.0~8 min,H2的平均反应速率v(H2)=0.75 mol·L-1·min-1
D.10~12 min,N2的平均反应速率为v(N2)=0.25mol·L-1·min-1
高二化学选择题极难题查看答案及解析
-
下列图像与对应的叙述相符的是
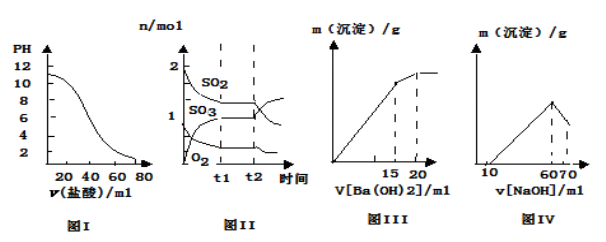
A、图I表示盐酸滴加到0.1mol/L某碱溶液中得到的滴定曲线,有图I可知二者恰好中和时,所得溶液的pH=7
B、图II表示一定条件下进行的反应2SO2+O2
2SO3 ΔH<0各成分的物质的量变化,t2时刻改变的条件可能是加压或降低温度
C、图III表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20mlBa(OH)2溶液时,沉淀是Al(OH)3和BaSO4的混合物
D、图IV表示向一定体积含等浓度NH4Cl、AlCl3、MgCl2混合溶液中逐渐加入NaOH溶液至过量的过程中,生成沉淀的质量与加入NaOH溶液的体积之间的关系
高二化学选择题极难题查看答案及解析
-
下列图示与对应的叙述不相符的是
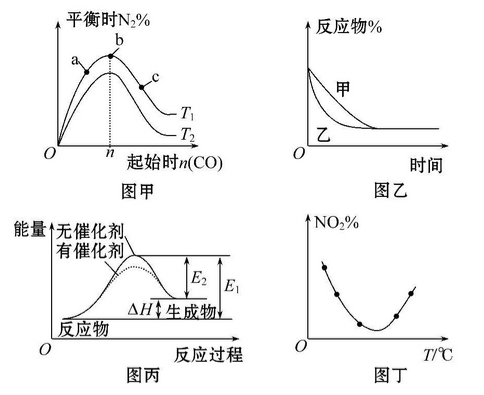
A.图甲表示反应:4CO(g)+2NO2(g)
N2(g)+4CO2(g) ΔH <0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2
B.图乙表示压强对可逆反应2A(g)+2B(g)
3C(g)+D(g)的影响,乙的压强比甲的压强大
C.图丙表示的反应是吸热反应,该图表明催化剂不能改变化学反应的焓变
D.图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
高二化学选择题极难题查看答案及解析
-
在容积固定不变的密闭容器中,可逆反应:A2(g)+B2(g)
nC(g)符合下列图1所示关系。由此推断,对图Ⅱ的说法不正确的是( )
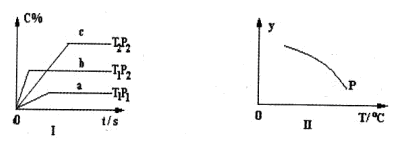
A.Y轴表示A2的转化率 B.Y轴表示C的浓度
C.Y轴表示混合气体的密度 D.Y轴表示混合气体的平均摩尔质量
高二化学选择题极难题查看答案及解析
-
在体积均为1.0 L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应CO2(g)+C(s)
2CO(g)达到平衡,平衡时c(CO2) 随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
A.该反应的ΔH>0、ΔS<0
B.体系的总压强p:p(Ⅰ)>p(Ⅲ)
C.平衡常数:K(Ⅰ)>K(Ⅱ)
D.T1K时,Ⅳ点所处的状态中v(正)<v(逆)
高二化学选择题极难题查看答案及解析
-
在标准状况下,进行甲、乙、丙三组实验:三组各取60 mL同浓度盐酸,加入同一种镁铝合金粉末,产生气体,有关数据列表如下:
实验序号
甲
乙
丙
合金质量/mg
510
770
918
气体体积/mL
560
672
672
则下列说法正确的是
A.甲组和乙组的实验中,盐酸均是过量的 B.盐酸的物质的量浓度为0.8 mol/L
C.合金中镁铝的物质的量之比为1∶1 D.丙组中铝的物质的量为0.009 mol
高二化学选择题极难题查看答案及解析
-
下列溶液中有关物质的量浓度关系正确的是
A.pH=2的HA溶液与pH=12的MOH溶液任意比混合:c(M+)>c(H+)>c(OH﹣)>c(A﹣)
B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(Na2CO3)<c(CH3COONa)<c(NaOH)
C.物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:c(CH3COO﹣)+2c(OH﹣)=2c(H+)+c(CH3COOH)
D.0.1mol•L﹣1的NaHA溶液,其pH=4:c(HA﹣)>c(H+)>c(H2A)>c(A2﹣)
高二化学选择题极难题查看答案及解析