-
关于CO2和CO的比较错误的是
A.组成:都是由碳元素和氧元素组成
B.性质:CO2能溶于水;CO难溶于水
C.用途:CO2可用作气体肥料;CO可用作气体燃料
D.危害:CO2会导致“温室效应”增强;CO会形成酸雨
难度: 中等查看答案及解析
-
成语涉及化学变化的是
A.绳锯木断 B.滴水成冰 C.死灰复燃 D.聚沙成塔
难度: 中等查看答案及解析
-
调味品加入适量水后不能形成溶液的是
A.食用油 B.食盐 C.味精 D.蔗糖
难度: 简单查看答案及解析
-
食物中含钙量最低的是




A.牛奶
B.青菜
C.豆类
D.虾皮
难度: 简单查看答案及解析
-
.关于“化学”的认识,错误的是
A.化学能创造自然界不存在的新型材料 B.化学能为人们战胜疾病,合成新药
C.化学在环境保护中起着重要作用 D.化学发展必然带来人类生存环境的恶化
难度: 简单查看答案及解析
-
“一滴水中约有1.67×1021个水分子”说明了
A.分子很小 B.分子间可以再分
C.分子之间有间隔 D.分子在不断地运动
难度: 中等查看答案及解析
-
用铂丝蘸取下列溶液在火焰上灼烧,可以观察到火焰呈紫色的是
A.Ca(OH)2 B.CaCl2 C.Na2CO3 D.KNO3
难度: 中等查看答案及解析
-
生活之中处处有化学,下列说法错误的是
A.干冰可用于人工降雨 B.硫酸铵[(NH4)2SO4]属于复合肥
C.用天然气代替煤可以减少酸雨的形成 D.生活中的垃圾用分类回收
难度: 中等查看答案及解析
-
名称、俗称、化学式不一致的是
A.银 水银 Ag B.碳酸钠 纯碱 Na2CO3
C.氧化钙 生石灰 CaO D.氢氧化钠 苛性钠 NaOH
难度: 困难查看答案及解析
-
肉桂酸的分子式为C9H8O2,关于肉桂酸的说法正确的是
A.有3种元素组成 B.摩尔质量为148
C.氧元素的质量分数最少 D.1mol分子中含有19个原子
难度: 中等查看答案及解析
-
硫粉在氧气中燃烧产生火焰的颜色是
A.黄色 B.白色 C.蓝紫色 D.砖红色
难度: 中等查看答案及解析
-
右图是用排空气法收集气体的装置,可用来收集H2、O2、CO2中的
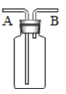
A.H2 B.H2和CO2
C.O2和CO2 D.H2、CO2、O2均可
难度: 中等查看答案及解析
-
一般食物的近似pH值如下:
食物
葡萄汁
苹果汁
牛奶
鸡蛋清
pH
3.5~4.5
2.9~3.3
6.3~6.6
7.6~8.0
说法错误的是
A.鸡蛋清和牛奶是显碱性 B.苹果汁和葡萄汁显酸性
C.苹果汁比葡萄汁的酸性强 D.胃酸过多的人应少饮葡萄汁和苹果汁
难度: 中等查看答案及解析
-
如图所示两种气体发生的化学反应,其中相同的球代表同种原子。根据图示信息,说法正确的是

A.该反应生成两种物质 B.该反应是复分解反应
C.化学反应前后原子的种类不变 D.分子在化学变化中是不可分的
难度: 中等查看答案及解析
-
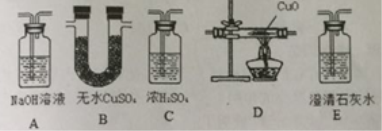
实验操作符合要求的是
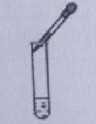
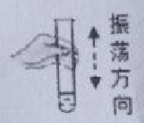
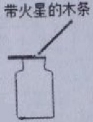
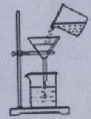
A.滴加液体
B.振荡试管
C.氧气验满
D.过滤
难度: 中等查看答案及解析
-
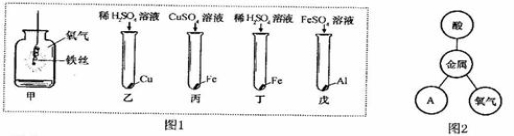
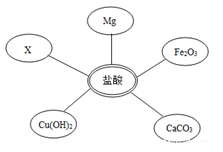
运用图示法可以帮助我们巧学化学。化学知识用相应图示表示正确的是
A.

B.

C.

D.

难度: 困难查看答案及解析
-
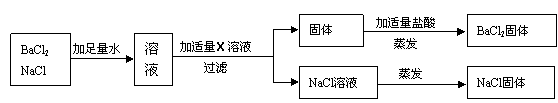
物质中的少量杂质(括号内为杂质),只需适量NaOH的固体或溶液就能除去的是
A.CO2(H2O) B.CO2(HCl)
C.NaCl溶液(MgCl2) D.KNO3溶液(H2SO4)
难度: 简单查看答案及解析
-
“法老之蛇”是网络上非常流行的化学兴趣实验,其实验原理如下:
4Hg(SCN)2→4HgS+2CS2+3(CN)2↑+N2↑该反应属于
A.化和反应 B.分解反应 C.置换反应 D.复分解反应
难度: 中等查看答案及解析
-
世界上最轻材料“碳海绵”的主要成分是石墨烯和碳纳米管(两者都是碳单质),具备高弹性和疏松多孔的结构,它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状。关于“碳海绵”的说法错误的是
A.常温下化学性质活泼 B.可燃烧
C.可重复使用 D.可处理海上石油泄漏
难度: 中等查看答案及解析
-
向一定量的氢氧化钠溶液中逐滴加入pH=2的稀盐酸至过量。图像中能反映对应变化关系的是
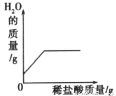


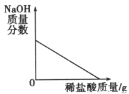
A.
B.
C.
D.
难度: 中等查看答案及解析
-
实验室配制50 g溶质质量分数为15 %的氯化钠溶液,说法错误的是
A.实验的的步骤为计算、称取、量取、溶解、转移
B.量取水时,用规格为50 mL的量筒量取42.5 mL
C.蒸馏水溶解过程中玻璃棒的作用是搅拌,以加快氯化钠的溶解速率
D.把配制好的氯化钠溶液倒入刚用蒸馏水洗过的试剂瓶中,并贴上标签
难度: 中等查看答案及解析
-
不用其他试剂无法鉴别的是
A.H2SO4 NaCl Na2CO3 CaCl2 B.HCl NaOH CuSO4 MgSO4
C.Na2CO3 K2SO4 BaCl2 HCl D.NaNO3 HCl CaCl2 KOH
难度: 中等查看答案及解析
-
在AgNO3、Zn(NO3) 2和Cu(NO3) 2的混合溶液中加入一定量的铁粉,充分反应后过滤。向滤渣中加入稀盐酸,有气泡产生。根据上述现象,结论正确的是
A.滤渣中一定有Zn B.滤渣中可能有Ag、Cu
C.滤渣中一定有Fe(NO3) 2、Zn(NO3) 2 D.滤渣中可能有AgNO3和Cu(NO3) 2
难度: 中等查看答案及解析
-
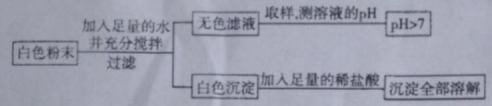
某固体粉末可能由氢氧化钠、氢氧化钙、碳酸钠和碳酸钙中的一种或几种组成,进行如下实验:①取少量固体加入足量的水,搅拌,有不溶物;②过滤,向滤液中加入盐酸,有气泡产生。对固体粉末成分的判断错误的是
A.一定有碳酸钠 B.可能有氢氧化钠
C.一定有碳酸钙 D.可能有氢氧化钙
难度: 中等查看答案及解析