海水中含有大量的NaCl,可用于制备钠及其化合物,其流程如下图:
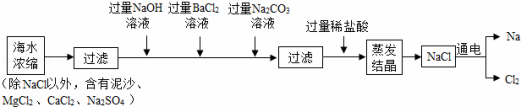
(1)过滤是将难溶性固体与 分离的一中实验操作。在上述蒸发结晶的过程中发生了 变化。
(2)加入过量Na2CO3溶液目的是除去CaCl2和 ,流程中不能用过量稀硫酸代替过量稀盐酸的原因是 ,请写出Na2CO3与CaCl2反应的化学方程式 。
(3)我国古代湿法炼铜是将铁放入硫酸铜溶液中,请用化学方程式表示 。依据炼铜与炼钠的反应条件不同,判断金属钠比铜获得 (填“更早”或“更晚”)。
九年级化学填空题困难题
海水中含有大量的NaCl,可用于制备钠及其化合物,其流程如下图:

(1)过滤是将难溶性固体与 分离的一中实验操作。在上述蒸发结晶的过程中发生了 变化。
(2)加入过量Na2CO3溶液目的是除去CaCl2和 ,流程中不能用过量稀硫酸代替过量稀盐酸的原因是 ,请写出Na2CO3与CaCl2反应的化学方程式 。
(3)我国古代湿法炼铜是将铁放入硫酸铜溶液中,请用化学方程式表示 。依据炼铜与炼钠的反应条件不同,判断金属钠比铜获得 (填“更早”或“更晚”)。
九年级化学填空题困难题
海水中含有大量的NaCl,可用于制备钠及其化合物,其流程如下图:
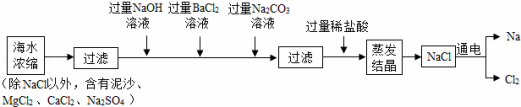
(1)过滤是将难溶性固体与 分离的一中实验操作。在上述蒸发结晶的过程中发生了 变化。
(2)加入过量Na2CO3溶液目的是除去CaCl2和 ,流程中不能用过量稀硫酸代替过量稀盐酸的原因是 ,请写出Na2CO3与CaCl2反应的化学方程式 。
(3)我国古代湿法炼铜是将铁放入硫酸铜溶液中,请用化学方程式表示 。
依据炼铜与炼钠的反应条件不同,判断金属钠比铜获得 (填“更早”或“更晚”)。
九年级化学填空题中等难度题查看答案及解析
海水中含有大量的NaCl,可用于制备钠及其化合物,其流程如下图:

(1)过滤是将难溶性固体与 分离的一中实验操作。在上述蒸发结晶的过程中发生了 变化。
(2)加入过量Na2CO3溶液目的是除去CaCl2和 ,流程中不能用过量稀硫酸代替过量稀盐酸的原因是 ,请写出Na2CO3与CaCl2反应的化学方程式 。
(3)我国古代湿法炼铜是将铁放入硫酸铜溶液中,请用化学方程式表示 。依据炼铜与炼钠的反应条件不同,判断金属钠比铜获得 (填“更早”或“更晚”)。
九年级化学填空题困难题查看答案及解析
地球是一颗美丽的蓝色星球,海水占了全球水资源的97%。海水资源的开发和利用具有非常广阔的前景。
(1)海水中含有大量的NaCl,可用于制备钠及其化合物,其流程如图:
①加入过量Na2CO3溶液目的是除去CaCl2和 ,流程中不能用过量稀硫酸代替过量稀盐酸的原因是 ;
②提纯过程中使用了过滤和蒸发操作,实验室过滤和蒸发操作均使用到的玻璃仪器是 ;
③流程图中制备金属钠的化学方程式为 。
(2)工业上利用电解饱和食盐水的方法制备NaOH,并同时获得两种单质。补充并配平化学方程式:
□NaCl+□H2O□ +□ +□Cl2↑
九年级化学填空题中等难度题查看答案及解析
通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:

(1)在第⑤步粗盐过滤操作中要用到玻璃棒,玻璃棒的作用是_____________。
(2)第⑥步操作的目的是除去滤液中Na2CO3、_________(填化学式)。
(3)第④步操作的目的是除去滤液中CaCl2、_________(填化学式)。
九年级化学简答题中等难度题查看答案及解析
氯化亚铜用途广泛,在潮湿的空气中易变质。制备反应方程式:2CuCl2+Na2SO3=2CuCl↓+2NaCl+SO3,工业制备流程如下:

下列说法不合理的是( )
A. “过滤”得硫酸钠固体,说明常温下硫酸钠的溶解度比氯化铜小
B. CuCl难溶于水和乙醇
C. “反应”中产生的三氧化硫会迅速和水化合生成H2SO3
D. “滤液2”中的氯化钠可循环利用
九年级化学单选题困难题查看答案及解析
海水晒制可得粗盐,粗盐除NaCl 外,还含有CaCl2、NaSO4以及泥沙等杂质。现设计一种制备精盐的实验流程,步骤如下。
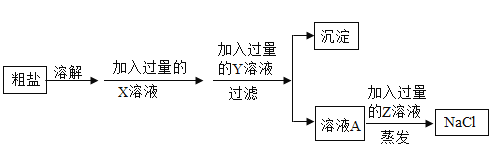
①实验流程中加入过量x、y溶液中的溶质分别是_______。
|
| Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| X | Na2CO3 | Na2CO3 | BaCl2 | Ba(NO3)2 |
| Y | BaCl2 | Ba(NO3)2 | Na2CO3 | Na2CO3 |
请简述选择该选项的理由__________。
②判断Y溶液过量的方法是__________。
I 取少量溶液A滴入硝酸银溶液,出现白色沉淀
II 取少量沉淀滴入盐酸,有气泡产生
III 取少量溶液A,滴入紫色石蕊,溶液变蓝
IV 取少量溶液A滴入石灰水,出现白色沉淀
③沉淀中除了泥沙等难溶杂质,还主要有_________物质。加入Z溶液过量,但对精盐制备没有影响不必除去,这是利用Z溶液的_______性质。
九年级化学流程题中等难度题查看答案及解析
(5分)用如图实验方法分离NaCl和CaCl2两种固体的混合物A,根据操作流程完成下列问题:
(1)B物质是 .
(2)过滤操作中玻璃棒的作用是 .
(3)经分析上述方法分离出的F含杂质,请对该设计方案加以完善 .
(4)若用原操作方法,要测出混合物A中NaCl和CaCl2的质量比,不称量D,可通过称量 和 的质量求解.
九年级化学填空题困难题查看答案及解析
海水可制备纯碱和金属镁,其流程如图1所示:
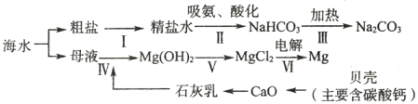
(1)粗盐中含有硫酸钠、氯化镁、氯化钙等可溶性杂质,为除去这些杂质而得到精盐,进行如下操作:①溶解;②加过量的 溶液;③加过量的
溶液;④加过量的
溶液;⑤过滤;⑥加适量的盐酸;⑦蒸发结晶。加过量的
溶液的作用是__________,加适量的盐酸的作用是__________。步骤Ⅴ所加的酸是______。
(2)某化学兴趣小组的同学对我市制碱厂进行了调查。该厂利用的是侯氏制碱法,侯氏制碱法的关键步骤是先向饱和食盐水中通入氨气,制成饱和氨盐水,氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,______先析出。
①工厂用的锅炉用酸洗去水垢。水垢的主要成分是碳酸钙和氢氧化镁,酸洗时用稀盐酸而不用稀硫酸的原因是__________。
②该厂某车间的废液中,可能含有盐酸、硫酸、碳酸钠、氯化钠、氯化镁中的一种或几种,为了探究其组成,做了如下实验:
步骤一:取废液少许测其;
步骤二:向一定质量的该废液中逐滴加入氢氧化钡溶液,开始没有沉淀,过一会儿,有沉淀产生。生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系如图2步骤二所示。
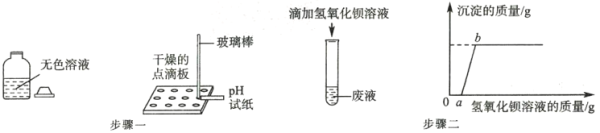
该废液的组成是______(填序号)。
A 一定含有盐酸、氯化镁,一定没有硫酸,可能含有氯化钠
B 一定含有盐酸、氯化镁,一定没有硫酸、碳酸钠,可能含有氯化钠
C 一定含有硫酸、氯化镁,一定没有盐酸、碳酸钠,可能含有氯化钠
九年级化学流程题中等难度题查看答案及解析
通过海水晒盐可以得到粗盐。某粗盐中除含有NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是某兴趣小组制备精盐的实验方案,其操作流程如下:
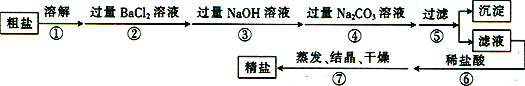
(1)步骤③的目的是除去粗盐中的杂质MgCl2,发生反应的化学方程式为_____________,其基本反应类型为__________________ 。
(2)步骤①、⑤、⑦都需要用到的玻璃仪器是_________;在进行操作⑤时有可能要重复进行,其原因是_______________。
(3)在步骤③中加入NaOH溶液的目的是除去MgCl2,不能用KOH溶液代替,其原因是______
(4)写出NaCl的一种用途:__________。
九年级化学流程题困难题查看答案及解析
海水中含有大量可以利用的化学资源。下图为综合利用海水制备金属镁的流程(贝壳的主要成分是碳酸钙):

该流程中没有涉及到的化学反应是( )
A.置换反应 B.分解反应 C.化合反应 D.复分解反应
九年级化学选择题简单题查看答案及解析