-
化学与生产、生活、社会密切相关。下列有关说法正确的是
A. 地沟油不宜食用,可分馏提取汽油
B. 二氧化硅可用于制取光导纤维
C. 为防止富脂食品氧化变质,在包装袋中放入生石灰
D. 钠、钾、铁等金属有绚丽的颜色,可用于制造焰火
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列叙述正确的是
A. 7.1 g 37Cl2含有的中子数为4NA
B. NA个Al(OH)3胶体粒子的质量为78 g
C. 7.8 g Na2O2晶体中阴阳离子总数为0.3NA
D. 标准状况下,2.24 L己烷含有的共价键数为1.9NA
难度: 中等查看答案及解析
-
下列关于有机化合物的说法正确的是
A. 淀粉、油脂、蛋白质都属于高分子化合物
B. 乙醇、乙酸、乙酸乙酯都能发生取代反应
C. 聚乙烯、苯乙烯都能使溴的四氯化碳溶液和酸性KMnO4溶液褪色
D. 硝基苯分子中苯环上的一个H被—C4H9取代后形成的有机物共有9种
难度: 简单查看答案及解析
-
下列实验操作、现象、结论和推理均正确的是
选项
实验操作
实验现象
实验结论
A
2 mL 0.1 mol/L的NaOH溶液中滴加2滴0.1 mol/L的MgCl2溶液,再滴加2滴0.1 mol/L的FeCl3溶液
白色沉淀变为红褐色
Ksp[Mg(OH)2]>Ksp[Fe(OH)3]
B
常温下,质量与表面积均相同的铝片分别投入足量的稀、浓硫酸中
浓硫酸中铝片先溶解完
反应物浓度越大,反应速率越快
C
将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡、静置
下层溶液显紫红色
氧化性:Fe3+>I2
D
向Na2SO3溶液加入稀盐酸酸化的Ba(NO3)2溶液
产生白色沉淀
Na2SO3溶液已变质
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
短周期主族元素X、Y、Z、R、T的原子半径与原子序数关系如下图所示。Y与Z能形成Z2Y、Z2Y2型离子化合物,R原子最外层电子数是电子层数的2倍,Z与T形成的化合物Z2T能破坏水的电离平衡。下列说法正确的是
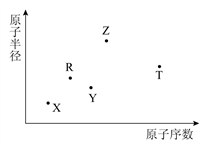
A. 最高价氧化物对应水化物的酸性R>T
B. 氢化物的沸点一定是Y>R
C. 原子半径和离子半径均满足Y<Z
D. 由X、Y、Z、T四种元素组成的化合物中既含有离子键又含有共价键。
难度: 中等查看答案及解析
-
微生物电池是指在微生物的作用下将化学能转化为电能的装置,下图是利用一种微生物将废水中的尿素[CO(NH2)2]转化为对环境无害物质的装置。下列叙述错误的是
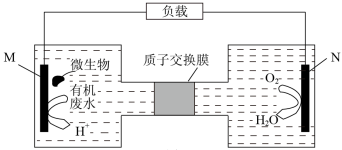
A. M电极有CO2和N2生成
B. H+透过质子交换膜由左向右移动
C. 微生物促进了反应中电子的转移
D. N电极反应式为O2 + 2H2O + 4e﹣= 4OH-
难度: 中等查看答案及解析
-
298K时,在100 mL 1 mol·L-1 H2R稀溶液中滴入1 mol·L-1 NaOH溶液,溶液中HR一、R2-的物质的量随pH变化的关系如下图所示。下列有关叙述正确的是
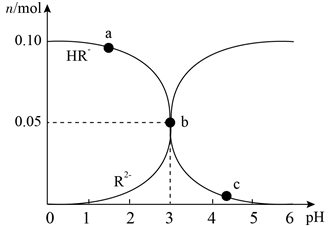
A. pH=4时,溶液中c(HR一)∶c(R2一)=l∶10
B. 滴入150 mL NaOH溶液时,溶液中c(Na+)>c(HR一)>c(R2一)
C. a点溶液中存在c(Na+) +c(H+) =c(HR一)+c(R2一)+c(OH一)
D. c点溶液中含R的微粒有HR-、H2R、R2-
难度: 困难查看答案及解析