-
甲醇(CH3OH)有很多用途。回答下列问题:
I.甲醇可用于制取甲醛(HCHO)。
(1)甲醇的沸点为64 ℃,甲醛的沸点为-21 ℃,甲醇的沸点较高的原因是__________。
(2)甲醇分子中采用sp3杂化的原子有____________(填元素符号);甲醛分子中σ键与π键之比为_______。
II.直接甲醇燃料电池(DMFC)因其具有质量轻、体积小、结构简单、比能量密度高、低温操作等优点,DMFC阳极普遍采用以铂(Pt)为基础 的二元催化剂,如Pt-Cr合金等。
(3)基态Cr原子的未成对电子数为______________。
(4)与铬同周期的所有元素中基态原子最外层电子数与铬原子相同的元素是_______。(填元素符号)
(5)已知金属铂晶胞结构如图所示。催化剂的XRD图谱分析认为:当铂中掺入Cr原子后,Cr替代了晶胞面心位置上的Pt,该催化剂的化学式为_______,晶体中与1个Pt原子相紧邻的Cr原子有_____个。
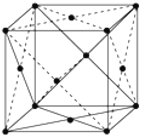
(6)若铂原子半径为r pm,铂摩尔质量为M g·mol-1,铂晶体的密度为ρ g·cm-3,则阿伏加德罗常数NA为_____mol-1(用有关字母列出计算式即可)。
-
甲醇(CH3OH)有很多用途。回答下列问题:
I.甲醇可用于制取甲醛(HCHO)。
(1)甲醇的沸点为64 ℃,甲醛的沸点为-21 ℃,甲醇的沸点较高的原因是__________。
(2)甲醇分子中采用sp3杂化的原子有____________(填元素符号);甲醛分子中σ键与π键之比为_____________。
II.直接甲醇燃料电池(DMFC)因其具有质量轻、体积小、结构简单、比能量密度高、低温操作等优点,DMFC阳极普遍采用以铂(Pt)为基础 的二元催化剂,如Pt-Cr合金等。
(3)基态Cr原子的未成对电子数为______________。
(4)与铬同周期的所有元素中基态原子最外层电子数与铬原子相同的元素是_______。(填元素符号)
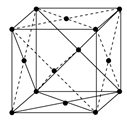
(5)已知金属铂晶胞结构如右图所示。催化剂的XRD图谱分析认为:当铂中掺入Cr原子后,Cr替代了晶胞面心位置上的Pt,该催化剂的化学式为_______,晶体中与1个Pt原子相紧邻的Cr原子有_____个。
(6)若铂原子半径为r pm,铂摩尔质量为M g·mol-1,铂晶体的密度为ρ g·cm-3,则阿伏加德罗常数NA为_____mol-1(用有关字母列出计算式即可)。
-
甲醇脱氢可制取甲醛CH3OH(g) HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。下列有关说法正确的是
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。下列有关说法正确的是

A.脱氢反应的△H<0
B.600K时,Y点甲醇的υ(正) <υ(逆)
C.从Y点到Z点可通过增大压强
D.在t1K时,该反应的平衡常数为8.1mol·L-1
-
甲醛(HCHO)是一种重要的化工产品,工业上可用甲醇脱氢法制备,相关反应方程式为:CH3OH(g)  HCHO(g)+H2(g) △H=+akJ/mol回答下列问题:
HCHO(g)+H2(g) △H=+akJ/mol回答下列问题:
(1)反应过程中需要向体系中通入空气,通过以下反应提供上述反应所需要的热量:H2(g)+ O2(g)=H2O(g) △H=-bkJ/mol
O2(g)=H2O(g) △H=-bkJ/mol
要使反应温度维持在650℃,则进料时,甲醇和空气的体积比应为___(已知空气中氧气的体积分数为20%,b>a)。
(2)Na2CO3是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下:
历程i:CH30H→・H+・CH2OH(・H叫做氢自由基,实际上就是H原子,有很高的反应活性,
“・”代表有一个单电子可以参与配对成键)
历程ii:・CH2OH→・H+HCHO
历程iii:・CH2OH→3•H+CO
历程iv:自由基发生碰撞形成新化学键而湮灭
如图1所示为在体积为2L的恒容容器中,投入1molCH3OH(g),在碳酸钠催化剂作用下开始反应,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)与温度的关系(副反应仅考虑CH3OH CO+2H2):
CO+2H2):
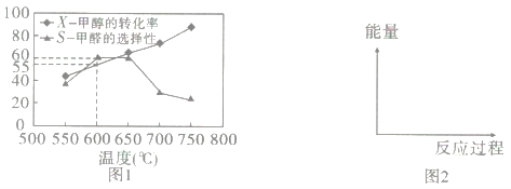
①请在图2所给坐标中,画出历程iv的反应过程一能量变化示意图___。
②下列说法合理的是__。
a.升高温度,甲醇转化率提高,平衡常数变大
b.当体系气体密度保持不变时,达到平衡状态
c.及时分离产品有利于提高甲醇生成甲醛的转化率
③600℃时,前20min甲醇的平均反应速率为__,此时生成甲醛的反应的Qp=___(Qp的表达式与平衡常数Kp相同,p为物质的分压,分压=总压×物质的量分数,体系初始压强为P0)
④650℃以后,甲醛的选择性降低,而甲醇的转化率升高的可能原因是___。
(3)氧化剂可处理甲醛污染,结合以下图像分析夏季(水温约20℃)应急处理甲醛污染的水源最好应选择的试剂为____。

-
甲醇脱氢可制取甲醛CH3OH(g) HCHO(g)+H2(g) +Q ,甲醇的平衡转化率随温度变化曲线如图所示。下列有关说法正确的是
HCHO(g)+H2(g) +Q ,甲醇的平衡转化率随温度变化曲线如图所示。下列有关说法正确的是
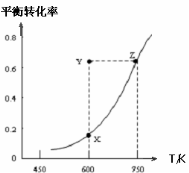
A.Q>0
B.600K时,Y点甲醇的υ(正) <υ(逆)
C.从Y点到Z点可通过增大压强实现
D.从Y点到X点可通过使用催化剂实现
-
甲醇脱氢可制取甲醛:CH3OH(g)  HCHO(g)+H2(g)∆H=-QkJ/mol,甲醇的平衡转化率随温度变化曲线如图所示。下列有关说法正确的是( )
HCHO(g)+H2(g)∆H=-QkJ/mol,甲醇的平衡转化率随温度变化曲线如图所示。下列有关说法正确的是( )
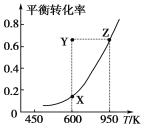
A.Q>0
B.600 K时,Y点甲醇的υ(正)<υ(逆)
C.从Y点到Z点可通过增大压强实现
D.从Y点到X点可通过使用催化剂实现
-
甲醇脱氢可制取甲醛CH3OH(g) HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示。下列有关说法正确的是
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示。下列有关说法正确的是
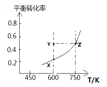
A. 该反应的正反应为放热反应
B. 600 K时,Y点甲醇的v(正)<v(逆)
C. 从Y点到Z点可通过增大压强实现
D. 从Y点到X点可通过使用催化剂实现
-
甲醇脱氢可制取甲醛CH3OH(g) HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示。下列有关说法正确的是
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示。下列有关说法正确的是
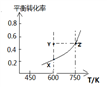
A. 该反应的正反应为放热反应
B. 600 K时,Y点甲醇的v(正)<v(逆)
C. 从Y点到Z点可通过增大压强实现
D. 从Y点到X点可通过使用催化剂实现
-
甲醛在木材加工、医药等方面有重要用途。甲醇直接脱氢是工业上合成甲醛的新方法,制备过程涉及的主要反应如下:
反应I:CH3OH(g) HCHO(g)+H2(g) △H1=+85.2kJ·mol-1
HCHO(g)+H2(g) △H1=+85.2kJ·mol-1
反应II:CH3OH(g)+1/2O2(1) HCHO(g)+H2O(g) △H2
HCHO(g)+H2O(g) △H2
反应III:H2(g)+1/2O2(g) H2O(g) △H3=-241.8kJ·mol-1
H2O(g) △H3=-241.8kJ·mol-1
副反应:
反应IV:CH3OH(g)+O2(g) CO(g)+2H2O(g) △H4=-393.0kJ·mol-1
CO(g)+2H2O(g) △H4=-393.0kJ·mol-1
(1)计算反应Ⅱ的反应热△H2=____________________________________________。
(2)750K下,在恒容密闭容器中,发生反应CH3OH(g) HCHO(g)+H2(g),若起始压强为P0,达到平衡转化率为α,则平衡时的总压强P平=___________(用含P0和α的式子表示);当P0=101kPa,测得α=50.0%,计算反应平衡常数Kp=___________kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,忽略其它反应)。
HCHO(g)+H2(g),若起始压强为P0,达到平衡转化率为α,则平衡时的总压强P平=___________(用含P0和α的式子表示);当P0=101kPa,测得α=50.0%,计算反应平衡常数Kp=___________kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,忽略其它反应)。
(3)Na2CO3是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下:
历程i:CH3OH→H+·CH2OH
历程ⅱ:·CH2OH→·H+HCHO
历程ⅲ:·CH2OH→3·H+CO
历程iv:·H+·H→H2
下图表示一定条件下温度对碳酸钠催化脱氢性能的影响,回答下列问题:
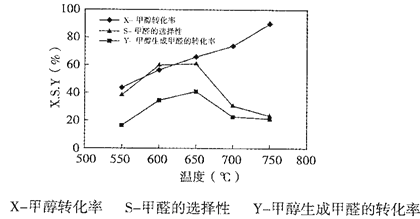
①从平衡角度解析550℃-650℃甲醇生成甲醛的转化率随温度升高的原因___________;
②反应历程i的活化能___________(填“>、“<”或“=”)CH3OH(g) HCHO(g)+H2(g)活化能。
HCHO(g)+H2(g)活化能。
③650℃~750℃,反应历程ii的速率___________(填“>”、“<”或“=”)反应历程ⅲ的速率。
(4)吹脱是处理甲醛废水的一种工艺,吹脱速率可用方程v=0.0423c(mg·L-1·h-1)表示(其中c为甲醛浓度),下表为常温下甲醛的浓度随吹脱时间变化数据。
| 浓度(mg/L) | 10000 | 8000 | 4000 | 2000 | 1000 |
| 吹脱时间(h) | 0 | 7 | 23 | 39 | 55 |
则当甲醛浓度为2000mg/L时,其吹脱速率v=___________ mg·L-1·h-1,分析上表数据,起始浓度为10000mg/L,当甲醛浓度降为5000mg/L,吹脱时间为___________h。
-
甲醛在木材加工、医药等方面有重要用途。甲醇直接脱氢是工业上合成甲醛的新方法,制备过程涉及的主要反应如下:
反应I:CH3OH(g) HCHO(g)+H2(g) △H1=+85.2kJ·mol-1
HCHO(g)+H2(g) △H1=+85.2kJ·mol-1
反应II:CH3OH(g)+1/2O2(1) HCHO(g)+H2O(g) △H2
HCHO(g)+H2O(g) △H2
反应III:H2(g)+1/2O2(g) H2O(g) △H3=-241.8kJ·mol-1
H2O(g) △H3=-241.8kJ·mol-1
副反应:
反应IV:CH3OH(g)+O2(g) CO(g)+2H2O(g) △H4=-393.0kJ·mol-1
CO(g)+2H2O(g) △H4=-393.0kJ·mol-1
(1)计算反应Ⅱ的反应热△H2=____________________________________________。
(2)750K下,在恒容密闭容器中,发生反应CH3OH(g) HCHO(g)+H2(g),若起始压强为P0,达到平衡转化率为α,则平衡时的总压强P平=___________(用含P0和α的式子表示);当P0=101kPa,测得α=50.0%,计算反应平衡常数Kp=___________kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,忽略其它反应)。
HCHO(g)+H2(g),若起始压强为P0,达到平衡转化率为α,则平衡时的总压强P平=___________(用含P0和α的式子表示);当P0=101kPa,测得α=50.0%,计算反应平衡常数Kp=___________kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,忽略其它反应)。
(3)Na2CO3是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下:
历程i:CH3OH→H+·CH2OH
历程ⅱ:·CH2OH→·H+HCHO
历程ⅲ:·CH2OH→3·H+CO
历程iv:·H+·H→H2
下图表示一定条件下温度对碳酸钠催化脱氢性能的影响,回答下列问题:
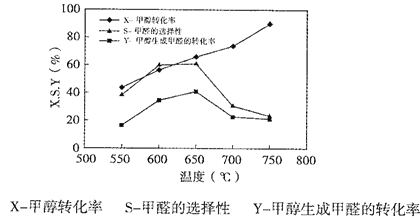
①从平衡角度解析550℃-650℃甲醇生成甲醛的转化率随温度升高的原因___________;
②反应历程i的活化能___________(填“>、“<”或“=”)CH3OH(g) HCHO(g)+H2(g)活化能。
HCHO(g)+H2(g)活化能。
③650℃~750℃,反应历程ii的速率___________(填“>”、“<”或“=”)反应历程ⅲ的速率。
(4)吹脱是处理甲醛废水的一种工艺,吹脱速率可用方程v=0.0423c(mg·L-1·h-1)表示(其中c为甲醛浓度),下表为常温下甲醛的浓度随吹脱时间变化数据。
| 浓度(mg/L) | 10000 | 8000 | 4000 | 2000 | 1000 |
| 吹脱时间(h) | 0 | 7 | 23 | 39 | 55 |
则当甲醛浓度为2000mg/L时,其吹脱速率v=___________ mg·L-1·h-1,分析上表数据,起始浓度为10000mg/L,当甲醛浓度降为5000mg/L,吹脱时间为___________h。










