-
某单官能团有机化合物,只含碳、氢、氧三种元素,相对分子质量为58,完全燃烧时产生等物质的量的CO2和H2O。它可能的结构共有(不考虑立体异构)
A. 4种 B. 5种 C. 6种 D. 7种
难度: 困难查看答案及解析
-
下列各组中的反应,属于同一反应类型的是( )
A.由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇
B.由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸
C.由氯代环己烷消去制环己烯;由丙烯加溴制1,2二溴丙烷
D.由溴丙烷水解制丙醇;由丙烯与水反应制丙醇
难度: 中等查看答案及解析
-
下列除去括号内杂质的有关操作方法不正确的是( )
A. 乙烷(乙炔):通过盛溴的四氯化碳溶液的洗气瓶
B. 乙酸乙酯(乙醇):加入乙酸和浓硫酸的混合液,然后加热
C. 苯(苯酚):加入氢氧化钠溶液,然后分液
D. 乙醇(水):加入生石灰,然后蒸馏
难度: 简单查看答案及解析
-
可以鉴别醋酸溶液、葡萄糖溶液、蔗糖溶液的试剂是
A. 银氨溶液 B. 新制氢氧化铜悬浊液
C. 石蕊试液 D. 碳酸钠溶液
难度: 中等查看答案及解析
-
下列叙述正确的是
A. 1molH2O的质量为18g/mol
B. CH4的摩尔质量为16g
C. 0.5NA个SO2分子的质量为32g
D. 标准状况下,1mol任何物质体积均为22.4L
难度: 中等查看答案及解析
-
质量相同的下列物质,含分子数最少的是
A. 氢气 B. 氧气 C. 氮气 D. 二氧化碳
难度: 简单查看答案及解析
-
下列溶液中,跟100 mL 0.5mol•L -1 NaCl溶液所含的Cl-物质的量浓度相同的是
A. 100 mL0.5mol•L-1 MgCl2溶液 B. 200 mL1mol•L-1 CaCl2溶液
C. 50 mL1mol•L-1 NaCl溶液 D. 25 mL0.5mol•L-1 HCl溶液
难度: 简单查看答案及解析
-
下列说法中不正确的是( )
A. 分子组成相差一个或几个
原子团的有机物不一定是同系物
B. 乙烯、聚氯乙烯结构中都含有碳碳双键
C.
只有一种结构说明甲烷分子是正四面体结构,而不是平面正方形结构
D. 分子中仅含有碳、氢元素的化合物是烃
难度: 中等查看答案及解析
-
六苯乙烷为白色固体,其结构如图所示。下列有关说法中正确的是
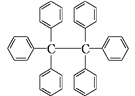
A. 它是一种苯的同系物,易溶于有机溶剂中
B. 它的分子式为C38H30,只含有非极性键
C. 它的一氯代物只有三种
D. 它的分子中所有原子共平面
难度: 中等查看答案及解析
-
鉴别二甲醚和乙醇可采用化学方法或物理方法,下列方法不能对二者进行鉴别的是( )
A. 利用金属钠或金属钾法 B. 利用红外光谱法
C. 利用质谱法 D. 利用核磁共振氢谱法
难度: 中等查看答案及解析
-
下列说法中错误的是
①有机物都是从有机体中分离出来的物质
②有机物都是含碳的共价化合物
③有机物都不溶于水,易溶于有机溶剂
④有机物不具备无机物的性质,都是非电解质
⑤当前在人类已知的化合物中,ⅣA族元素的化合物种类最多
⑥ⅢB族所含的元素种类最多。
A. ①③④ B. ③④⑤ C. ②③④⑥ D. ①②③④
难度: 中等查看答案及解析
-
中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用。若1 mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
A、2 mol Br2 2 mol NaOH
B、2 mol Br2 3 mol NaOH
C、3 mol Br2 4 mol NaOH
D、4 mol Br2 4 mol NaOH
难度: 中等查看答案及解析
-
下列所给出的化学式中,能够真实的表示分子的组成的是( )
A. SiO2 B. Ar C. NaOH D. CH3COONH4
难度: 简单查看答案及解析
-
下列物物质中,可证明某晶体是离子晶体的是 ( )
A.易溶于水 B.晶体不导电,熔化时能导电
C.熔点较高 D.晶体不导电,水溶液能导电
难度: 简单查看答案及解析
-
关于氢键的下列说法中正确的是( )
A. 每个水分子内含有两个氢键
B. 在单个水分子、水蒸气、液态水、冰中都存在氢键
C. 分子间能形成氢键使物质的熔沸点升高
D. HF的热稳定性很强,是因为其分子间能形成氢键
难度: 简单查看答案及解析
-
下列不属于配合物的是( )
A. [Cu(H2O)4]SO4·H2O B. [Ag(NH3)2]OH
C. KAl(SO4)2·12H2O D. Na[Al(OH)4]
难度: 中等查看答案及解析
-
能与Na反应放出H2,又能使溴水褪色,但不能使pH试纸变色的物质是
A. CH2=CH—COOH B. CH2=CH—CH2—OH
C. CH2=CH—CHO D. CH2=CH—COOCH3
难度: 中等查看答案及解析
-
某一溴代烷水解后的产物在红热铜丝催化下,最多可被空气氧化生成4种不同的醛,该一溴代烷的分子式可能是
A. C4H9Br B. C5H11Br C. C6H13Br D. C7H15Br
难度: 简单查看答案及解析
-
将
和
(甘油)以一定比例混合,测得混合物含碳51.3%,那么氧元素的质量分数是( )
A. 40% B. 35% C. 30% D. 无法计算
难度: 中等查看答案及解析
-
下面四个化学反应中,有一个化学反应与其他三个类型不同的是:
A. CH3CH2OH + CH3COOH
CH3COOCH2CH3+ H2O
B. CH3CH2OH
CH2=CH2↑+H2O
C. 2CH3CH2OH
CH3CH2OCH2CH3+ H2O
D. CH3CH2OH + HBr
CH3CH2Br + H2O
难度: 中等查看答案及解析