-
CO、CO2是化石燃料燃烧后的主要产物。
(1)将等体积的CO2和CO混合气体通入有足量Na2O2固体的密闭容器中,同时不断地用电火花点燃,将残留固体溶于水,所得溶质的化学式是___________________。
(2)已知:CO(g)+O2(g)  CO2 (g)+O(g) △H1=-33.5kJ·mol─1;
CO2 (g)+O(g) △H1=-33.5kJ·mol─1;
键能E(O=O)=499.0 kJ·mol─1
2CO(g)+O2(g) = 2CO2 (g)的△H2=_____________kJ·mol─1。
(3)在恒容密闭容器中,控制不同温度进行CO2分解实验:2CO2 (g) 2CO(g)+O2(g)。以CO2起始浓度均为c mol•L─1 测定CO2的转化率,结果如图所示。图中甲曲线表示CO2的平衡转化率与温度的关系,乙曲线表示不同温度下反应10min所测CO2的转化率。
2CO(g)+O2(g)。以CO2起始浓度均为c mol•L─1 测定CO2的转化率,结果如图所示。图中甲曲线表示CO2的平衡转化率与温度的关系,乙曲线表示不同温度下反应10min所测CO2的转化率。
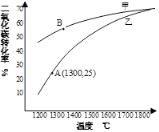
①在1300℃时反应10min到达A点,反应的平均速率v(O2)=________。随温度升高,曲线乙向曲线甲靠近的原因是________________________________________。要让B点CO2的转化率增大,除升高温度外,还可以采取_______________措施(任填一个)。
②下列不能说明上述反应达到平衡状态的是_______________。
a.单位时间内生成n mol O2的同时生成2n mol CO; b.混合气体的密度不再改变;
c.CO2的转化率不再变化; d.密闭容器中压强不再改变;
e.混合气体的平均相对分子质量不再改变。
(4)利用电化学还原CO2制取ZnC2O4的示意图如图所示,电解液不参加反应,则Zn与电源的_____极相连,Pb极上的电极反应式是_____________________________。

-
CO、CO2是化石燃料燃烧的主要产物。
(1)将含0.02 molCO2和0.01molCO的混合气体通入有足量Na2O2固体的密闭容器中,同时不断地用电火花点燃,充分反应后,固体质量增加_________g。
(2)已知1500℃时,在密闭容器中发生反应:CO2(g) CO(g)+O(g)。反应过程中O(g)的物质的量浓度随时间的变化如图1 所示,则0~2 min 内,CO2的平均反应速率 υ(CO2)=_________。
CO(g)+O(g)。反应过程中O(g)的物质的量浓度随时间的变化如图1 所示,则0~2 min 内,CO2的平均反应速率 υ(CO2)=_________。

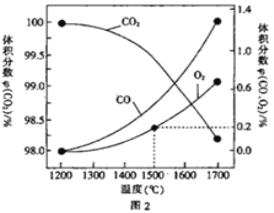
(3)在某密闭容器中发生反应:2CO2(g) 2CO(g)+O2(g),1molCO2在不同温度下的平衡分解量如图2 所示。
2CO(g)+O2(g),1molCO2在不同温度下的平衡分解量如图2 所示。
①恒温恒容条件下,能表示该可逆反应达到平衡状态的有_________ (填字母)。
A.CO 的体积分数保持不变
B.容器内混合气体的密度保持不变
C.容器内混合气体的平均摩尔质量保持不变
D.单位时间内,消耗CO 的浓度等于生成CO2的浓度
②分析图2,若1500℃时反应达到平衡状态,且容器体积为1L,则此时反应的平衡常数K=_________(计算结果保留1 位小数)。
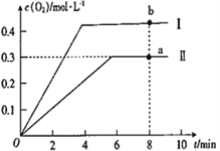
③向恒容密闭容器中充入2molCO2(g),发生反应:2CO2(g) 2CO(g) +O2(g),测得温度为T℃时,容器内O2的物质的量浓度随时间的变化如曲线II 所示。图中曲线I 是相对于曲线II仅改变一种反应条件后c(O2)随时间的变化,则改变的条件是________;a、 b两点用CO浓度变化表示的净反应速率关系为υa(CO)_________(填“>”“<”或“=”) υb( CO)。
2CO(g) +O2(g),测得温度为T℃时,容器内O2的物质的量浓度随时间的变化如曲线II 所示。图中曲线I 是相对于曲线II仅改变一种反应条件后c(O2)随时间的变化,则改变的条件是________;a、 b两点用CO浓度变化表示的净反应速率关系为υa(CO)_________(填“>”“<”或“=”) υb( CO)。
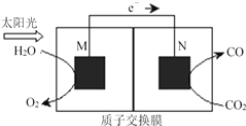
(4)科学家还研究了其它转化温室气体的方法,利用下图所示装置可以将CO2转化为气体燃料CO。该装置工作时,N电极的电极反应式为___________________________,若导线中通过电子为a mol,则M极电解质溶液中H+改变量为________mol。
-
一定体积的CH4在密闭容器中与一定量的氧气燃烧后得到的产物为CO、CO2和水蒸气,此混合气重4.96g,当其缓慢经过浓硫酸时,浓硫酸增重2.52g.原混合气体中CO2的质量为( )
A. 1.25g B. 1.32g C. 1.97g D. 2.44g
-
300℃时,将100mL由H2O、CO2和N2组成的混合气体通入盛有足量Na2O2的密闭容器中(容器体积保持不变),充分反应后恢复到原温度时容器内的压强变为原来的4/5,则原混合气体中N2的体积分数为
A. 33.3% B. 40% C. 60% D. 75%
-
300℃时,将100mL由H2O、CO2和N2组成的混合气体通入盛有足量Na2O2的密闭容器中(容器体积保持不变),充分反应后恢复到原温度时容器内的压强变为原来的4/5,则原混合气体中N2的体积分数为
A. 33.3% B. 40% C. 60% D. 75%
-
工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
Ⅰ.脱碳:
向2L密闭容器中加入2mol CO2、8mol H2,在适当的催化剂作用下,发生反应:CO2(g)+4H2(g)  CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
(1)该反应自发进行的条件是_______(填“低温”、“高温”或“任意温度”)
(2)下列叙述能说明此反应达到平衡状态的是_______________。
a、混合气体的平均相对分子质量保持不变
b、CO2和H2的体积分数比为1﹕4
c、CO2和H2的转化率相等
d、混合气体的密度保持不变
e、1mol CO2生成的同时有4mol H-H键断裂
Ⅱ.脱硝:
(3)催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的化学方程式为__________。
(4)温度为T1时,在三个容积均为1L的恒容密闭容器中仅发生反应:2NO2(g)  2NO(g)+O2(g)相关数据如下表所示。下列说法错误的是__________。
2NO(g)+O2(g)相关数据如下表所示。下列说法错误的是__________。
| 容器 编号 | 物质的起始浓度 (mol·L-1) | 物质的平衡浓度 (mol·L-1) |
| c(NO2) | c(NO) | c(O2) | c(O2) |
| 甲 | 0.6 | 0 | 0 | 0.2 |
| 乙 | 0.3 | 0.5 | 0.2 | |
| 丙 | 0 | 0.5 | 0.35 | |
A.容器甲中发生反应的平衡常数为0.8
B.容器乙中起始时反应正向进行
C.达到平衡时,容器丙中c(O2)/c(NO2)>1
D.达到平衡时,容器甲与容器丙中的总压强之比为16∶17
-
一直X是化石燃料燃烧的产物之一,有漂白作用,是形成酸雨的主要物质;Y是一种温室气体,固体Y可用于灭火;Z是硝酸工业和汽车尾气中的有害物质之一,是一种红棕色气体,能与水反应。请回答:
(1)请简述实验室检验X气体的方法为_____________________。
(2)固体Y俗称_______,将标准状况下,2.24L气体Y通入100mL1.5mol/L NaOH溶液中,充分反应后,溶液中的溶质及其物质的量浓度为(溶液体积变化忽略不计)__________________。
(3)X、Y、Z中属于酸性氧化物的是_______(填化学式),Z与水反应得到的酸的浓溶液通常保存在棕色试剂瓶中,用化学方程式表示其原因为_____________。
-
0.2moL有机物和0.4moLO2在密闭容器中燃烧后的产物为CO2、CO和水蒸气。产物经过浓硫酸后溶液增加10.8g;再经过灼热CuO充分反应后固体减轻3.2g;最后气体再通过碱石灰被完全吸收,碱石灰质量增加17.6g。
(1)燃烧后产物的物质的量分别为:CO2__________moL、 CO_____moL、H2O(g)____________moL。
(2)推断该有机物的化学式为 ______________________。
-
0.2mol有机物和0.4mol O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物经过浓硫酸后,浓硫酸的质量增加10.8g;再通过灼热CuO充分反应后,固体质量减轻了3.2g;最后气体再通过碱石灰被完全吸收,碱石灰的质量增加17.6g。
(1)判断该有机物的化学式;
(2)若0.2mol该有机物恰好与9.2g金属钠完全反应,试确定该有机物的结构简式;
(3)若0.2mol该有机物恰好与4.6g金属钠完全反应,试确定该有机物的结构简式。
-
0.2mol有机物和0.4mol O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g).产物经过浓硫酸后,浓硫酸的质量增加10.8g;再通过灼热CuO充分反应后,固体质量减轻3.2g;最后气体再通过碱石灰被完全吸收,碱石灰质量增加17.6g.
(1)燃烧后的产物的物质的量分别为CO2________mol、CO________mol、H2O(g)________mol.
(2)推断该有机物的化学式为________.
(3)若其核磁共振氢谱显示只有两种环境不同的H,试确定该有机物的结构简式为________.
CO2 (g)+O(g) △H1=-33.5kJ·mol─1;
2CO(g)+O2(g)。以CO2起始浓度均为c mol•L─1 测定CO2的转化率,结果如图所示。图中甲曲线表示CO2的平衡转化率与温度的关系,乙曲线表示不同温度下反应10min所测CO2的转化率。





